“碘钟”实验中,3I-+ =
= + 2
+ 2 的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
回答下列问题:
(1)该实验的目的是_______ 。
(2)显色时间t1=_______ 。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为_______ (填字母)。
A.<22.0s B.22.0~44.0s C.>44.0s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是_______ 。
 =
= + 2
+ 2 的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol·L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
| c(S2O82-)/mol·L-1 | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t /s | 88.0 | 44.0 | 22.0 | 44.0 | t1 |
(1)该实验的目的是
(2)显色时间t1=
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为
A.<22.0s B.22.0~44.0s C.>44.0s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是
9-10高二下·浙江·期末 查看更多[15]
(已下线)2.1.1 化学反应速率——同步学习必备知识吉林省长春外国语学校2021-2022学年高二上学期期初考试化学试题【全国百强校】江苏省启东中学2018-2019学年高二上学期期中考试化学试题(已下线)2018年10月22日 《每日一题》人教选修4--化学反应速率的实验探究【全国百强校】黑龙江省大庆实验中学2018-2019学年高二上学期开学考试化学试题(已下线)2012年苏教高中化学选修6 4.1硫代硫酸钠与酸反应速率的影响练习卷(已下线)2012年鲁科版高中化学必修2 2.2化学反应的快慢和限度练习卷(已下线)2010—2011学年辽宁省开原高中高一下学期第一次月考化学试卷2017届黑龙江双鸭山一中高三上学期期中化学试卷(已下线)2010年6月浙江省金温七校高二化学期末卷2015-2016学年湖南省衡阳一中高二上学期期中(理)化学试卷(已下线)2012-2013学年浙江省宁海县正学中学高二下学期第一次阶段性测试化学试卷(已下线)2012-2013学年安徽省铜陵一中高二10月月考化学试卷(已下线)2011-2012学年吉林长春市十一高高一下学期期中考试化学试卷(已下线)2011-2012年广东东莞南城中学高二上学期期中考试化学试卷
更新时间:2016-12-09 03:41:32
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】兴趣小组同学为探究影响化学反应速率及化学平衡的因素,设计以下实验:

(1)利用实验I探究锌与稀硫酸反应的速率,需要记录的实验数据有:___________ 。
(2)利用实验II探究浓度对化学平衡的影响。已知: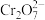 (橙色)
(橙色)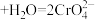 (黄色)
(黄色)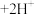 ,推测B试管中的实验现象为:
,推测B试管中的实验现象为:___________ ,用平衡移动原理解释其原因:___________ 。
(3)该小组同学继续用酸性 溶液和草酸(
溶液和草酸( )溶液进行实验,设计实验方案如表所示。请回答相关问题:
)溶液进行实验,设计实验方案如表所示。请回答相关问题:
①实验时,分别量取 溶液和酸性
溶液和酸性 溶液,迅速混合并开始计时,通过测定
溶液,迅速混合并开始计时,通过测定___________ 来判断反应的快慢。
②实验a、b、c所加的 溶液均要过量。理由是
溶液均要过量。理由是___________ 。
③实验a和b是探究___________ 对化学反应速率的影响。实验b和c是探究___________ 对化学反应速率的影响。
④实验a和b起初反应均很慢,过了一会儿速率突然增大,可能原因是___________ 。

(1)利用实验I探究锌与稀硫酸反应的速率,需要记录的实验数据有:
(2)利用实验II探究浓度对化学平衡的影响。已知:
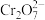 (橙色)
(橙色)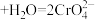 (黄色)
(黄色)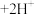 ,推测B试管中的实验现象为:
,推测B试管中的实验现象为:(3)该小组同学继续用酸性
 溶液和草酸(
溶液和草酸( )溶液进行实验,设计实验方案如表所示。请回答相关问题:
)溶液进行实验,设计实验方案如表所示。请回答相关问题:| 编号 | 温度℃ |  溶液 溶液 | 酸性 溶液 溶液 | ||
浓度/( ) ) | 体积/mL | 浓度/( ) ) | 体积/mL | ||
| a | 25 | 0.10 | 2.0 | 0.010 | 4.0 |
| b | 25 | 0.20 | 2.0 | 0.010 | 4.0 |
| c | 50 | 0.20 | 2.0 | 0.010 | 4.0 |
 溶液和酸性
溶液和酸性 溶液,迅速混合并开始计时,通过测定
溶液,迅速混合并开始计时,通过测定②实验a、b、c所加的
 溶液均要过量。理由是
溶液均要过量。理由是③实验a和b是探究
④实验a和b起初反应均很慢,过了一会儿速率突然增大,可能原因是
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某实验小组用0.1 mol·L-1Na2S2O3 溶液和0.1 mol·L-1H2SO4溶液为反应物,探究外界条件对化学反应速率的影响,实验记录如下表。
资料:Na2S2O3+ H2SO4=Na2SO4+ SO2↑+ S↓+ H2O
根据表中信息回答下列问题:
(1)实验Ⅲ中 a =____ 。
(2) 对比实验Ⅰ、Ⅳ,得出的结论是_____ ;用文字表述得出该结论的依据是_____ 。
(3)可用于研究浓度对化学反应速率影响的实验组合是(任写一组)_____ 。
资料:Na2S2O3+ H2SO4=Na2SO4+ SO2↑+ S↓+ H2O
| 实验序号 | 温度 | Na2S2O3 | H2SO4 | H2O | 出现沉淀所需的时间 |
Ⅰ | 0℃ | 5 mL | 5 mL | 10 mL | 12s |
Ⅱ | 0℃ | 5 mL | 10 mL | 5 mL | 8s |
Ⅲ | 0℃ | 5 mL | 7mL | a mL | 10s |
Ⅳ | 30℃ | 5 mL | 5 mL | 10 mL | 4s |
(1)实验Ⅲ中 a =
(2) 对比实验Ⅰ、Ⅳ,得出的结论是
(3)可用于研究浓度对化学反应速率影响的实验组合是(任写一组)
您最近半年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】近年来,我国化工技术获得重大突破,利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇(CH3OH)是其中的一个研究项目。该研究发生的主要反应如下:
Ⅰ.CO与H2反应合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
Ⅱ.CO2与H2反应合成甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
(1)上述反应符合原子经济性的是反应___________ (I或II)。
(2)在某一时刻采取下列措施,能使反应I的反应速率减小的措施是___________。
(3)一定温度下,在容积固定的密闭容器中发生反应Ⅱ,下列说法可以表明反应达到化学平衡状态的是___________。
(4)H2还原CO电化学法制备甲醇(CO + 2H2 = CH3OH)的工作原理如图所示:
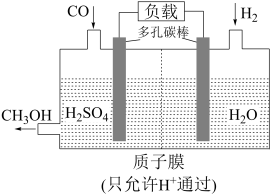
通入H2的一端是电池的___________ 极(填“正”或“负”),电池工作过程中H+通过质子膜向___________ (填“左”或者“右”)移动,通入CO的一端发生的电极反应式为___________ 。
Ⅰ.CO与H2反应合成甲醇:CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)Ⅱ.CO2与H2反应合成甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)(1)上述反应符合原子经济性的是反应
(2)在某一时刻采取下列措施,能使反应I的反应速率减小的措施是___________。
| A.恒温恒容下,再充入CO | B.升高温度 |
| C.恒温恒容下,向其中充入Ar | D.恒温恒压下,向其中充入Ar |
| A.单位时间内消耗3molH2,同时生成1mol的CH3OH |
| B.CH3OH的体积分数不再发生变化 |
| C.3v(CO2)=v(H2) |
| D.容器内气体密度不再改变 |

通入H2的一端是电池的
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】有硫酸酸化的草酸(H2C2O4,二元弱酸)溶液能将KMnO4溶液中的MnO4-转化为Mn2+。某化学小组研究发现,少量MnSO4可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)常温下,控制KMnO4溶液初始浓度相同,调节不同的初始pH和草酸溶液用量,做对比实验,完成实验设计表_______ 、______ 。
(2)该反应的离子方程式______________________________________________ 。
(3)若t1<t2,则根据实验①和②得到的结论是__________________________________ 。
(4)请你设计实验验证MnSO4对该反应起催化作用,实验方案(不要求写出具体操作过程):_______________________________________________________________________ ;
预期实验结果和结论:_____________________________________________________ 。
| 实验编号 | 温度 | 初始 pH | 0.1mol/L草酸溶液体积/mL | 0.01mol/LKMnO4溶液体积/mL | 蒸馏水体积/mL | 待测数据(反应混合液褪色时间/s) |
| ① | 常温 | 1 | 20 | 50 | 30 | t1 |
| ② | 常温 | 2 | 20 | 50 | 30 | t2 |
| ③ | 常温 | 2 | 40 | t3 |
(1)常温下,控制KMnO4溶液初始浓度相同,调节不同的初始pH和草酸溶液用量,做对比实验,完成实验设计表
(2)该反应的离子方程式
(3)若t1<t2,则根据实验①和②得到的结论是
(4)请你设计实验验证MnSO4对该反应起催化作用,实验方案(不要求写出具体操作过程):
预期实验结果和结论:
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(1)该实验探究的是____ 因素对化学反应速率的影响。
(2)若实验①在2min末收集了4.48mLCO2(标准状况下),则在2min末,c(MnO )=
)=___ mol·L-1。
(3)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定___ 来比较化学反应速率。
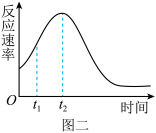
(4)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是①该反应放热、②____ 。
 +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):| 实验序号 | A溶液 | B溶液 |
| ① | 20mL0.1mol·L-1H2C2O4溶液 | 30mL0.01mol·L-1KMnO4溶液 |
| ② | 20mL0.2mol·L-1H2C2O4溶液 | 30mL0.01mol·L-1KMnO4溶液 |
(2)若实验①在2min末收集了4.48mLCO2(标准状况下),则在2min末,c(MnO
 )=
)=(3)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定
(4)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是①该反应放热、②

您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】为探究影响化学反应速率的因素,某研究小组设计了如下五个实验。已知:Cu2+、Fe3+对H2O2的分解起催化作用。请回答下列问题:

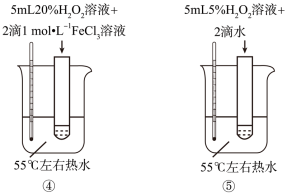
(1)为探究浓度对反应速率的影响,应选择实验_______ (填标号)。
(2)选择②③作对比试验,目的是探究_______ 因素对反应速率的影响。
(3)为探究催化剂对反应速率的影响,同时探究不同催化剂对同一反应的催化效果,应选择实验_______ (填序号)。
(4)根据上述实验,实验室若需用H2O2溶液快速制备少量O2,可采取的措施有_______ (写3条)。


(1)为探究浓度对反应速率的影响,应选择实验
(2)选择②③作对比试验,目的是探究
(3)为探究催化剂对反应速率的影响,同时探究不同催化剂对同一反应的催化效果,应选择实验
(4)根据上述实验,实验室若需用H2O2溶液快速制备少量O2,可采取的措施有
您最近半年使用:0次



