Ⅰ、含氮废水是造成水体污染的重要原因之一、研究含氮废水的处理对水体净化有重要意义。利用 O2 和 H2 可高效去除水体中同时存在的 NH 和 NO
和 NO 。
。
具体方法是:①先利用氧气将 NH 氧化成 NO
氧化成 NO ,
,
②再利用 H2 将 NO 还原为N2 (2NO
还原为N2 (2NO +5H2
+5H2 N2+2OH-+4H2O)。
N2+2OH-+4H2O)。
(1)反应①中氧化剂与还原剂物质的量之比为___________ 。
(2)若完全处理 100g 含 NH4NO3 4%的废水,至少需要标准状况下的 H2___________ L。
(3)该污水处理的好处是___________ (列举一条即可)
Ⅱ、焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、FeCl3、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是___________ (写化学式)。
(2)写出并配平该反应的化学方程式:___________ ;
(3)发生还原反应的物质是___________ ,反应中2mol氧化剂能___________ (填“失去”或“得到”)___________ mol电子。
(4)反应中产生5.6L(标准状况)的气体时,被还原的物质的质量为___________ 。
 和 NO
和 NO 。
。具体方法是:①先利用氧气将 NH
 氧化成 NO
氧化成 NO ,
,②再利用 H2 将 NO
 还原为N2 (2NO
还原为N2 (2NO +5H2
+5H2 N2+2OH-+4H2O)。
N2+2OH-+4H2O)。(1)反应①中氧化剂与还原剂物质的量之比为
(2)若完全处理 100g 含 NH4NO3 4%的废水,至少需要标准状况下的 H2
(3)该污水处理的好处是
Ⅱ、焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、FeCl3、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是
(2)写出并配平该反应的化学方程式:
(3)发生还原反应的物质是
(4)反应中产生5.6L(标准状况)的气体时,被还原的物质的质量为
更新时间:2021-07-28 12:52:56
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】亚铁氰化钾俗称黄血盐,化学式为K4[Fe(CN)6].3H2O.黄血盐毒性很低,在空气中稳定且具有防止细粉状食品板结的性能,故用作食盐的抗结剂.但是在400℃左右黄血盐分解生成剧毒的氰化钾(KCN),与强酸作用也会生成极毒的氰化氢(HCN)气体。
完成下列填空:
(1)剧毒的KCN可以用双氧水处理,得到一种碱性气体和一种酸式盐.请写出该反应的化学方程式______ 。
(2)若往KCN溶液中通入少量的CO2气体,其反应的离子方程式______ 。已知电离常数(25℃):H2CO3:Ki1=4.3×10﹣7 ,Ki2=5.6×10﹣11,HCN:Ki1=4.9×10﹣10
(3)常温下,测得等物质的量浓度的KCN与HCN混合溶液的pH>7,则溶液中K+、H+、CN﹣、HCN浓度大小顺序为______ 。
(4)黄血盐作为食盐的抗结剂,必须严格控制其使用量,原因是______ 。
(5)黄血盐常用于Fe3+检验。请再写出一种检验Fe3+的试剂______ ,其相应的现象是______ 。
(6)FeCl3与Na2S反应,生成的产物与溶液的酸碱性有关.当pH<7时,有淡黄色沉淀产生,当pH>7时,生成黑色沉淀(Fe2S3).请写出往FeCl3溶液中滴加少量Na2S溶液的离子方程式:______ 。
完成下列填空:
(1)剧毒的KCN可以用双氧水处理,得到一种碱性气体和一种酸式盐.请写出该反应的化学方程式
(2)若往KCN溶液中通入少量的CO2气体,其反应的离子方程式
(3)常温下,测得等物质的量浓度的KCN与HCN混合溶液的pH>7,则溶液中K+、H+、CN﹣、HCN浓度大小顺序为
(4)黄血盐作为食盐的抗结剂,必须严格控制其使用量,原因是
(5)黄血盐常用于Fe3+检验。请再写出一种检验Fe3+的试剂
(6)FeCl3与Na2S反应,生成的产物与溶液的酸碱性有关.当pH<7时,有淡黄色沉淀产生,当pH>7时,生成黑色沉淀(Fe2S3).请写出往FeCl3溶液中滴加少量Na2S溶液的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)X、Y、Z三种物质存在如图所示转化关系。
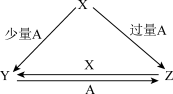
回答下列问题:
①若X为黑色固体单质,A为O2,写出Z→Y的化学方程式:___ 。
②若X为NaOH溶液,则写出Y→Z的离子方程式:___ 。
(2)已知常温下在溶液中可发生如下两个反应:
Ce4++Fe2+=Fe3++Ce3+
Sn2++2Fe3+=2Fe2++Sn4+
由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是___ 。
(3)Mn2+、Bi3+、BiO 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程。
→Bi3+的反应过程。
①该反应中,被氧化的元素是___ (填元素符号),氧化剂是___ (填化学式)。
②将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式:______+______+______→______+______+H2O。___
(4)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。
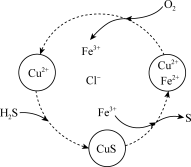
①写出CuCl2与H2S反应的离子方程式:___ 。
②通过上述流程图的分析,整个流程的总反应为___ 。
(1)X、Y、Z三种物质存在如图所示转化关系。

回答下列问题:
①若X为黑色固体单质,A为O2,写出Z→Y的化学方程式:
②若X为NaOH溶液,则写出Y→Z的离子方程式:
(2)已知常温下在溶液中可发生如下两个反应:
Ce4++Fe2+=Fe3++Ce3+
Sn2++2Fe3+=2Fe2++Sn4+
由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是
(3)Mn2+、Bi3+、BiO
 、MnO
、MnO 、H+、H2O组成的一个氧化还原反应体系中,发生BiO
、H+、H2O组成的一个氧化还原反应体系中,发生BiO →Bi3+的反应过程。
→Bi3+的反应过程。①该反应中,被氧化的元素是
②将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式:______+______+______→______+______+H2O。
(4)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图所示。

①写出CuCl2与H2S反应的离子方程式:
②通过上述流程图的分析,整个流程的总反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)现有以下物质:①Ba(OH)2晶体,②盐酸,③冰醋酸(固态醋酸),④石墨,⑤酒精(C2H5OH),请回答下列问题(填序号):
Ⅰ、以上物质中属于电解质的是_______ 。
Ⅱ、以上物质中属于非电解质的是_______ 。
Ⅲ、请写出①在水溶液中的电离方程式_______ 。
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有_______ (填“氧化性”或“还原性”)。
(3)当光束通过下列物质时,会出现丁达尔效应的是_______ 。
①Fe(OH)3胶体 ②水 ③蔗糖溶液 ④Ca(OH)2悬浊液
(4)用单线桥 标出下列反应中电子转移的情况:_______ 。
8NH3+6NO2 7N2+12H2O
7N2+12H2O
(5)请写出最恰当的试剂除去括号中的杂质:Cl2(HCl)_______ 。
(6)FeSO4可作补血剂,用于治疗缺铁性贫血症。用FeSO4溶液制备Fe(OH)2的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的原因是为了防止Fe(OH)2被氧化,写出其被氧化的化学反应方程式_______ 。
(1)现有以下物质:①Ba(OH)2晶体,②盐酸,③冰醋酸(固态醋酸),④石墨,⑤酒精(C2H5OH),请回答下列问题(填序号):
Ⅰ、以上物质中属于电解质的是
Ⅱ、以上物质中属于非电解质的是
Ⅲ、请写出①在水溶液中的电离方程式
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(3)当光束通过下列物质时,会出现丁达尔效应的是
①Fe(OH)3胶体 ②水 ③蔗糖溶液 ④Ca(OH)2悬浊液
(4)用
8NH3+6NO2
 7N2+12H2O
7N2+12H2O(5)请写出最恰当的试剂除去括号中的杂质:Cl2(HCl)
(6)FeSO4可作补血剂,用于治疗缺铁性贫血症。用FeSO4溶液制备Fe(OH)2的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的原因是为了防止Fe(OH)2被氧化,写出其被氧化的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】从化合价的角度分析氯及其化合物的性质,回答下列问题。
(1)氯化亚铜(CuCl)是重要的化工原料,工业上常通过下列反应制备CuCl:2CuSO4+Na2SO3+2NaCl+Na2CO3=2CuCl↓+3Na2SO4+CO2↑。CuCl可以溶解在FeCl3溶液中,请写出该反应的离子方程式___________ 。
(2)已知Cu2O在酸性溶液中发生歧化反应:Cu2O+2H+ =Cu2++Cu+H2O。现将一定量的混合物(Fe2O3、Cu2O、CuCl、Fe)溶解于过量稀盐酸中,反应完全后,得到W (包括溶液和少量剩余固体)。
①W的溶液中一定含有的阳离子为___________ (填离子符号)。
②向W中加入过量铁粉,过滤,调pH约为7,加入淀粉-KI溶液和H2O2溶液,溶液呈蓝色并有红褐色沉淀生成。已知:每消耗4molI-转移6mol电子,则加入淀粉-KI溶液和H2O2溶液后反应的离子方程式为_______ 。
(3)某工厂的废水中含KCN,现用氯氧化法处理,发生如下反应(化合物中N的化合价均为-3价):KCN+2KOH+Cl2= KOCN+2KCl+H2O。
①通入过量氯气,可将氰酸盐进一步氧化为氮气和二氧化碳, 请配平下列化学方程式:_________
__KOCN+__ KOH+__Cl2=__ CO2+__N2+__KCl+__H2O。
②若废水含KCN浓度为0.065 g/L,按上述反应将KCN氧化成N2和CO2,处理1 m3这样的废水,需要标准状况下的氯气的体积为___________ L。
(4)二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理为:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。
①该反应中,氧化剂和还原剂的物质的量之比为_______ 。
②ClO2在杀菌消毒过程中会产生副产物亚氯酸盐( ),需将其转化为Cl-除去,下列试剂中可将
),需将其转化为Cl-除去,下列试剂中可将 转化为Cl-的是
转化为Cl-的是_______ (填字母)。
A.FeSO4 B.O3 C. KMnO4 D.SO2
(1)氯化亚铜(CuCl)是重要的化工原料,工业上常通过下列反应制备CuCl:2CuSO4+Na2SO3+2NaCl+Na2CO3=2CuCl↓+3Na2SO4+CO2↑。CuCl可以溶解在FeCl3溶液中,请写出该反应的离子方程式
(2)已知Cu2O在酸性溶液中发生歧化反应:Cu2O+2H+ =Cu2++Cu+H2O。现将一定量的混合物(Fe2O3、Cu2O、CuCl、Fe)溶解于过量稀盐酸中,反应完全后,得到W (包括溶液和少量剩余固体)。
①W的溶液中一定含有的阳离子为
②向W中加入过量铁粉,过滤,调pH约为7,加入淀粉-KI溶液和H2O2溶液,溶液呈蓝色并有红褐色沉淀生成。已知:每消耗4molI-转移6mol电子,则加入淀粉-KI溶液和H2O2溶液后反应的离子方程式为
(3)某工厂的废水中含KCN,现用氯氧化法处理,发生如下反应(化合物中N的化合价均为-3价):KCN+2KOH+Cl2= KOCN+2KCl+H2O。
①通入过量氯气,可将氰酸盐进一步氧化为氮气和二氧化碳, 请配平下列化学方程式:
__KOCN+__ KOH+__Cl2=__ CO2+__N2+__KCl+__H2O。
②若废水含KCN浓度为0.065 g/L,按上述反应将KCN氧化成N2和CO2,处理1 m3这样的废水,需要标准状况下的氯气的体积为
(4)二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理为:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。
①该反应中,氧化剂和还原剂的物质的量之比为
②ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(
 ),需将其转化为Cl-除去,下列试剂中可将
),需将其转化为Cl-除去,下列试剂中可将 转化为Cl-的是
转化为Cl-的是A.FeSO4 B.O3 C. KMnO4 D.SO2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】中国疾控中心指出,消毒是疫情防控的重要措施。含氯消毒剂是一种高效、安全的杀菌消毒剂。
I.
(1)已知HClO的杀菌能力比ClO-强。25℃时将氯气溶于水形成氯气—氯水体系,该体系中Cl2(aq)、HClO和 ClO-的物质的量分数(α)随pH变化的关系如图所示。
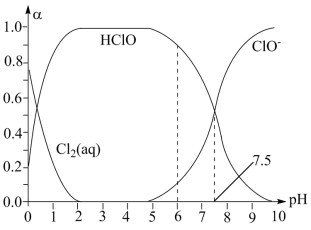
由图分析,用氯气处理饮用水时,pH=6与pH=7.5两种情况下,pH=___________ 时杀菌效果强;当pH=7.5时,氯水中含氯元素的微粒有HClO、ClO-和___________ 。
(2)84消毒液是一种家庭常用消毒剂,但不能用于钢制器具的消毒,原因是___________ ;在使用时不能与洁厕灵(主要成分为盐酸)混合使用,混合时会产生黄绿色的有毒气体,其反应的离子方程式为___________ 。
(3) 是国际上公认的高效、安全的杀菌消毒剂。工业制备ClO2的反应原理为:
是国际上公认的高效、安全的杀菌消毒剂。工业制备ClO2的反应原理为: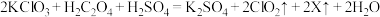 ,X的化学式为
,X的化学式为___________ ,每生成1mol ClO2,反应中转移电子___________ mol。
II.如图是实验室制备氯气并进行一系列相关实验的装置(部分夹持装置已略去)。
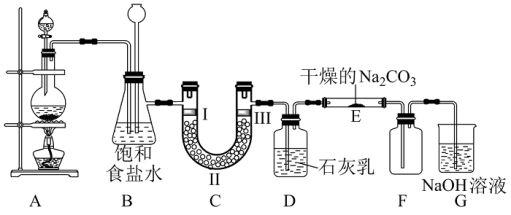
(4)装置B有安全瓶作用,监测实验进行时C中是否发生堵塞,发生堵塞时B中的现象为___________ 。
(5)装置E中潮湿的Cl2与Na2CO3以物质的量比2:1反应,生成Cl2O气体,试写出该反应的化学方程式:___________ 。
I.
(1)已知HClO的杀菌能力比ClO-强。25℃时将氯气溶于水形成氯气—氯水体系,该体系中Cl2(aq)、HClO和 ClO-的物质的量分数(α)随pH变化的关系如图所示。

由图分析,用氯气处理饮用水时,pH=6与pH=7.5两种情况下,pH=
(2)84消毒液是一种家庭常用消毒剂,但不能用于钢制器具的消毒,原因是
(3)
 是国际上公认的高效、安全的杀菌消毒剂。工业制备ClO2的反应原理为:
是国际上公认的高效、安全的杀菌消毒剂。工业制备ClO2的反应原理为: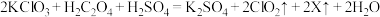 ,X的化学式为
,X的化学式为II.如图是实验室制备氯气并进行一系列相关实验的装置(部分夹持装置已略去)。

(4)装置B有安全瓶作用,监测实验进行时C中是否发生堵塞,发生堵塞时B中的现象为
(5)装置E中潮湿的Cl2与Na2CO3以物质的量比2:1反应,生成Cl2O气体,试写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)PCl3和PCl5都可通过磷和氯气化合得到。现有2.48g红磷(P),与一定量的氯气恰好完全反应,产物的总质量为14.55g,计算产物中PCl3的质量分数___________ 。
(2)已知:PCl3和PCl5能发生如下水解反应:
 ;
;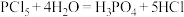
现将一定量的PCl3和PCl5混合物溶于足量水中,在加热条件下缓缓通入0.02molO2,恰好将H3PO3氧化为H3PO4,往反应后的溶液中加入15.725gCa(OH)2,充分反应后磷元素全部转化为Ca3(PO4)2沉淀,过滤后得到2.5L滤液,测得反应后溶液中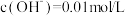 。计算:
。计算:
① (已知式量310)沉淀的质量
(已知式量310)沉淀的质量___________ ;
②滤液中各溶质的物质的量浓度___________ 。
(1)PCl3和PCl5都可通过磷和氯气化合得到。现有2.48g红磷(P),与一定量的氯气恰好完全反应,产物的总质量为14.55g,计算产物中PCl3的质量分数
(2)已知:PCl3和PCl5能发生如下水解反应:
 ;
;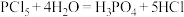
现将一定量的PCl3和PCl5混合物溶于足量水中,在加热条件下缓缓通入0.02molO2,恰好将H3PO3氧化为H3PO4,往反应后的溶液中加入15.725gCa(OH)2,充分反应后磷元素全部转化为Ca3(PO4)2沉淀,过滤后得到2.5L滤液,测得反应后溶液中
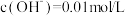 。计算:
。计算:①
 (已知式量310)沉淀的质量
(已知式量310)沉淀的质量②滤液中各溶质的物质的量浓度
您最近一年使用:0次
【推荐1】双氧水(H2O2)和水都是极弱电解质,但H2O2溶液显弱酸性,医疗上利用它有杀菌消毒作用来清洗伤口。请回答下列问题:
(1)若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:________ 。
(2)鉴于H2O2显弱酸性,它能同强碱作用形成“正盐”,在一定条件下也可形成“酸式盐”,请写出H2O2与Ba(OH)2作用形成的“正盐”的化学方程式:________ 。
(3)对于下列A→D涉及H2O2的反应,填写空白:
A.Na2O2+2HCl=2NaCl+H2O2
B.2H2O2=2H2O+O2↑
C.Ag2O+H2O2=2Ag+O2↑+H2O
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
E.MnO4-+H2O2+H+=Mn2-+O2↑+H2O(未配平)
①H2O2仅体现还原性的反应是________ (填代号)。
②配平E反应并用单线桥法表示电子转移的方向与数目________ 。
③上述反应说明H2O2、Ag2O、K2CrO4氧化性由弱到强的顺序是________ 。
(4)在H2O2的参与下, 可以与Fe2+反应制备Fe2O3纳米颗粒,若
可以与Fe2+反应制备Fe2O3纳米颗粒,若 与Fe2+的个数比为1:2,配平该反应的离子方程式:Fe2++
与Fe2+的个数比为1:2,配平该反应的离子方程式:Fe2++ +H2O2+OH-=Fe2O3+
+H2O2+OH-=Fe2O3+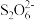 +H2O
+H2O________________ 。
(5)奥运会期间,由于工作人员将84消毒液与双氧水混用,导致游泳池藻类快速生长,池水变绿,一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长,该反应中氧化性:H2O2________ NaClO(填“>”或“<”),反应的离子反应方程式为________________ 。
(1)若把H2O2看成是二元弱酸,请写出它在水中的电离方程式:
(2)鉴于H2O2显弱酸性,它能同强碱作用形成“正盐”,在一定条件下也可形成“酸式盐”,请写出H2O2与Ba(OH)2作用形成的“正盐”的化学方程式:
(3)对于下列A→D涉及H2O2的反应,填写空白:
A.Na2O2+2HCl=2NaCl+H2O2
B.2H2O2=2H2O+O2↑
C.Ag2O+H2O2=2Ag+O2↑+H2O
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
E.MnO4-+H2O2+H+=Mn2-+O2↑+H2O(未配平)
①H2O2仅体现还原性的反应是
②配平E反应并用单线桥法表示电子转移的方向与数目
③上述反应说明H2O2、Ag2O、K2CrO4氧化性由弱到强的顺序是
(4)在H2O2的参与下,
 可以与Fe2+反应制备Fe2O3纳米颗粒,若
可以与Fe2+反应制备Fe2O3纳米颗粒,若 与Fe2+的个数比为1:2,配平该反应的离子方程式:Fe2++
与Fe2+的个数比为1:2,配平该反应的离子方程式:Fe2++ +H2O2+OH-=Fe2O3+
+H2O2+OH-=Fe2O3+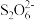 +H2O
+H2O(5)奥运会期间,由于工作人员将84消毒液与双氧水混用,导致游泳池藻类快速生长,池水变绿,一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长,该反应中氧化性:H2O2
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)请按要求写出下列反应的化学方程式或离子方程式:
①物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,写出该反应的化学方程式________ 。
②ClO2常用于水的净化,工业上可用Cl2氧化Na ClO2溶液制取ClO2.写出该反应的离子方程式:__________ 。
③Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为________ 。
④NaBH4是一种重要的储氢载体,能与水反应达到NaBO2,且反应前后B的化合价不变,该反应的化学方程式为_________ 。
(2)四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O32-+O2+xOH-═Fe3O4+S4O62-+2H2O。请回答下列问题。
①水热法制备Fe3O4纳米颗粒的反应中,还原剂是_________ 。反应的化学方程式中x=_________ 。
②每生成1 mol Fe3O4,反应转移的电子为________ mol,被Fe2+还原的O2的物质的量为________ mol。
①物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为N2O,反应结束后锌没有剩余,写出该反应的化学方程式
②ClO2常用于水的净化,工业上可用Cl2氧化Na ClO2溶液制取ClO2.写出该反应的离子方程式:
③Na2S2O3还原性较强,在溶液中易被Cl2氧化成SO42-,常用作脱氯剂,该反应的离子方程式为
④NaBH4是一种重要的储氢载体,能与水反应达到NaBO2,且反应前后B的化合价不变,该反应的化学方程式为
(2)四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O32-+O2+xOH-═Fe3O4+S4O62-+2H2O。请回答下列问题。
①水热法制备Fe3O4纳米颗粒的反应中,还原剂是
②每生成1 mol Fe3O4,反应转移的电子为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题。
Ⅰ.已知某容器中发生了一个化学反应,反应体系存在 、
、 、
、 、
、 、
、 、
、 六种粒子。在反应过程中,溶液紫红色逐渐褪去。
六种粒子。在反应过程中,溶液紫红色逐渐褪去。
(1)写出该反应的离子方程式:___________ 。
(2)该反应中,氧化剂与还原剂的粒子个数之比为___________ 。
Ⅱ.高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为: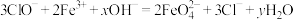 ,回答下列问题:
,回答下列问题:
(3)上述反应中的
___________ ,
___________ 。
(4)上述反应中氧化剂为___________ ;还原产物为___________ 。
(5)由上述反应可知,氧化性强弱:
___________  (填“>”或“<”,下同);还原性强弱:
(填“>”或“<”,下同);还原性强弱:
___________  。
。
(6)请用单线桥法表示该反应中电子的转移情况:___________ 。
Ⅰ.已知某容器中发生了一个化学反应,反应体系存在
 、
、 、
、 、
、 、
、 、
、 六种粒子。在反应过程中,溶液紫红色逐渐褪去。
六种粒子。在反应过程中,溶液紫红色逐渐褪去。(1)写出该反应的离子方程式:
(2)该反应中,氧化剂与还原剂的粒子个数之比为
Ⅱ.高铁酸钠
 是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为: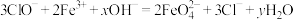 ,回答下列问题:
,回答下列问题:(3)上述反应中的


(4)上述反应中氧化剂为
(5)由上述反应可知,氧化性强弱:

 (填“>”或“<”,下同);还原性强弱:
(填“>”或“<”,下同);还原性强弱:
 。
。(6)请用单线桥法表示该反应中电子的转移情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】 因外观和食盐相似,又有咸味,容易使人误食中毒,已知
因外观和食盐相似,又有咸味,容易使人误食中毒,已知 能发生如下反应:
能发生如下反应: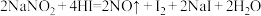 。
。
(1)上述反应中氧化剂是___________ ,每1mol该氧化剂参与反应,转移了___________ 个电子。
(2)根据上述反应,鉴别 和NaCl。可选用的物质有:①水、②淀粉碘化钾试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有
和NaCl。可选用的物质有:①水、②淀粉碘化钾试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有___________ (填序号)。
(3)某厂废液中,含有2%~5%的 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为不引起二次污染的
转化为不引起二次污染的 的是___________(填编号)。
的是___________(填编号)。
(4)请配平以下化学方程式: 。
。
并用单桥法标出电子转移的方向和数目___________ 。
(5)若反应过程中转移5mol ,则生成标准状况下
,则生成标准状况下 的体积为
的体积为___________ L。
 因外观和食盐相似,又有咸味,容易使人误食中毒,已知
因外观和食盐相似,又有咸味,容易使人误食中毒,已知 能发生如下反应:
能发生如下反应: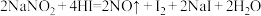 。
。(1)上述反应中氧化剂是
(2)根据上述反应,鉴别
 和NaCl。可选用的物质有:①水、②淀粉碘化钾试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有
和NaCl。可选用的物质有:①水、②淀粉碘化钾试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有(3)某厂废液中,含有2%~5%的
 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为不引起二次污染的
转化为不引起二次污染的 的是___________(填编号)。
的是___________(填编号)。| A.NaCl | B. | C. | D.浓 |
 。
。并用单桥法标出电子转移的方向和数目
(5)若反应过程中转移5mol
 ,则生成标准状况下
,则生成标准状况下 的体积为
的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硝酸是用途广泛的重要化工原料,自然界和化工生产中合成硝酸各物质转化关系如下图所示,请结合你所学的知识回答以下问题:
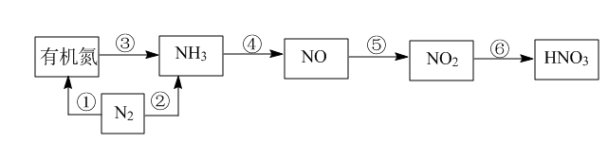
(1) 在自然界中能稳定存在的原因是
在自然界中能稳定存在的原因是___________ ;
(2)上图①~⑥各步转化中,属于氮的固定的是___________ (填序号);
(3)氨的催化氧化是工业合成硝酸的重要步骤,其中氧化剂与还原剂物质的量之比___________ ;
(4)为提高NO→ 的转化率,可采取的措施是
的转化率,可采取的措施是___________ ;
(5)工业制硝酸时含有NO、 等大气污染物。用尿素[
等大气污染物。用尿素[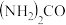 ]水溶液吸收氮氧化物是一种可行的方法。NO和
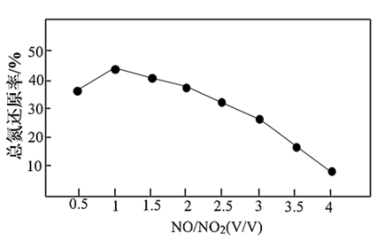
]水溶液吸收氮氧化物是一种可行的方法。NO和 不同配比混合气通入尿素溶液中,总氮还原率与配比关系如下图。
不同配比混合气通入尿素溶液中,总氮还原率与配比关系如下图。
①用尿素[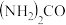 ]水溶液吸收体积比为1:1的NO和
]水溶液吸收体积比为1:1的NO和 混合气,可将N元素转变为对环境无害的气体。该反应的化学方程式
混合气,可将N元素转变为对环境无害的气体。该反应的化学方程式___________ ;
②随着NO和 配比的提高,总氮还原率降低的主要原因是
配比的提高,总氮还原率降低的主要原因是___________ 。

(1)
 在自然界中能稳定存在的原因是
在自然界中能稳定存在的原因是(2)上图①~⑥各步转化中,属于氮的固定的是
(3)氨的催化氧化是工业合成硝酸的重要步骤,其中氧化剂与还原剂物质的量之比
(4)为提高NO→
 的转化率,可采取的措施是
的转化率,可采取的措施是(5)工业制硝酸时含有NO、
 等大气污染物。用尿素[
等大气污染物。用尿素[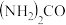 ]水溶液吸收氮氧化物是一种可行的方法。NO和
]水溶液吸收氮氧化物是一种可行的方法。NO和 不同配比混合气通入尿素溶液中,总氮还原率与配比关系如下图。
不同配比混合气通入尿素溶液中,总氮还原率与配比关系如下图。
①用尿素[
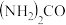 ]水溶液吸收体积比为1:1的NO和
]水溶液吸收体积比为1:1的NO和 混合气,可将N元素转变为对环境无害的气体。该反应的化学方程式
混合气,可将N元素转变为对环境无害的气体。该反应的化学方程式②随着NO和
 配比的提高,总氮还原率降低的主要原因是
配比的提高,总氮还原率降低的主要原因是
您最近一年使用:0次



