甲醇既是重要的化工原料,也是性能优良的能源和车用燃料。利用煤气过程中生成的CO和 可制备甲醇:
可制备甲醇:
 ,有关能量的变化如图甲所示。一定温度下,在容积为1L的恒容密闭容器中充入1 mol CO和
,有关能量的变化如图甲所示。一定温度下,在容积为1L的恒容密闭容器中充入1 mol CO和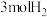 ,测得部分相关物质的浓度随时间的变化如图乙所示。
,测得部分相关物质的浓度随时间的变化如图乙所示。
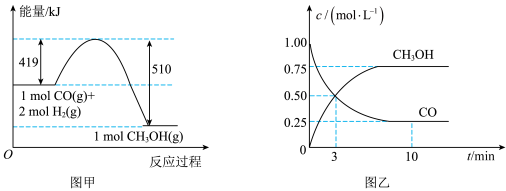
下列有关说法正确的是
 可制备甲醇:
可制备甲醇:
 ,有关能量的变化如图甲所示。一定温度下,在容积为1L的恒容密闭容器中充入1 mol CO和
,有关能量的变化如图甲所示。一定温度下,在容积为1L的恒容密闭容器中充入1 mol CO和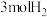 ,测得部分相关物质的浓度随时间的变化如图乙所示。
,测得部分相关物质的浓度随时间的变化如图乙所示。
下列有关说法正确的是
A.该反应的 | B.前3 min内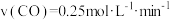 |
| C.氢气的平衡转化率为75% | D.该反应的平衡常数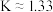 |
更新时间:2021-08-01 06:55:55
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g)△H=xkJ·mol-1
已知:①C(s)+O2(g)=CO2(g)△H=akJ·mol-1
②K2S(s)=S(s)+2K(s)△H=bkJ·mol-1
③2K(s)+N2(g)+3O2(g)=2KNO3(s)△H=ckJ·mol-1
下列说法不正确的是( )
S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g)△H=xkJ·mol-1
已知:①C(s)+O2(g)=CO2(g)△H=akJ·mol-1
②K2S(s)=S(s)+2K(s)△H=bkJ·mol-1
③2K(s)+N2(g)+3O2(g)=2KNO3(s)△H=ckJ·mol-1
下列说法不正确的是( )
| A.x<0 a>0 |
| B.b>0 c<0 |
| C.x=3a-b-c |
| D.1mol碳(s)在空气中不完全燃烧生成CO的焓变大于akJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知化学反应A2(g)+B2(g)=2AB(g)的能量变化如图所示,依据图象判断下列叙述正确的是( )
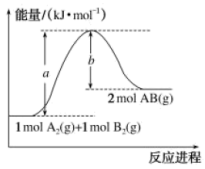

| A.反应A2(g)+B2(g)=2AB(g)的活化能是b |
| B.加入催化剂,(a-b)的差值减小 |
| C.2AB(g)=A2(g)+B2(g) △H<0 |
| D.若反应生成AB(l),吸收的热量大于(a-b)kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一 定条件下存在反应:C(s)+H2O(g) CO(g)+H2(g) △H>0,向甲、乙、丙三个恒容容器中加入一定量的初始物质,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示:
CO(g)+H2(g) △H>0,向甲、乙、丙三个恒容容器中加入一定量的初始物质,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示:
下列说法正确的是
 CO(g)+H2(g) △H>0,向甲、乙、丙三个恒容容器中加入一定量的初始物质,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示:
CO(g)+H2(g) △H>0,向甲、乙、丙三个恒容容器中加入一定量的初始物质,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示:| 容器 | 甲 | 乙 | 丙 |  |
| 容积/L | 1 | 1 | V | |
| 温度/℃ | T1 | T2 | T1 | |
| 起始量 | 2 molC(s)、2 mol H2O(g) | 2 mol CO(g)、2 mol H2(g) | 6 molC(s)、 4mol H2O(g) |
下列说法正确的是
| A.甲容器中,0~5 min内的平均反应速率v(CO)=0.1 mol/(L·min) |
| B.乙容器中,若平衡时n(C)=0.56 mol,则T2>T1 |
| C.温度为T1时,反应的平衡常数为K=9 |
| D.丙容器的容积V=0.8 L |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】用 固体与100mL稀盐酸反应制取
固体与100mL稀盐酸反应制取 ,反应过程中溶液体积变化忽略不计,实验过程中
,反应过程中溶液体积变化忽略不计,实验过程中 的体积变化如图所示(
的体积变化如图所示( 的体积已折算为标准状况下的体积)。下列分析正确的是
的体积已折算为标准状况下的体积)。下列分析正确的是

 固体与100mL稀盐酸反应制取
固体与100mL稀盐酸反应制取 ,反应过程中溶液体积变化忽略不计,实验过程中
,反应过程中溶液体积变化忽略不计,实验过程中 的体积变化如图所示(
的体积变化如图所示( 的体积已折算为标准状况下的体积)。下列分析正确的是
的体积已折算为标准状况下的体积)。下列分析正确的是
| A.此反应可用稀硫酸代替盐酸制取二氧化碳 |
| B.向溶液中加入氯化钠固体可降低该反应的化学反应速率 |
C.OE、EF、FG三段中,生成 的物质的量之比为2:6:7 的物质的量之比为2:6:7 |
D.0~3min内,该反应的平均反应速率约为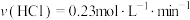 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】将一定物质的量的HI(g)置于2L的恒容密闭容器中,发生反应2HI(g)⇌H2(g)+I2(g)。在其他条件相同时,HI(g)的物质的量n随时间t的变化情况如表中数据所示,下列说法不正确的是
 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1(800℃) | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2(800℃) | 1.2 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 3(820℃) | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| A.在实验1中,反应在10~20min内v(HI)=6.5×10-3mol/(L·min) |
| B.根据实验1和实验2,可知反应恰好达到平衡状态的时间相同 |
| C.根据实验2和实验3,无法说明浓度对反应速率的影响趋势 |
| D.根据实验1和实验3,可得出反应吸热,温度越高,平衡越正向移动,HI的分解率越大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】T℃时,在2L恒容密闭容器中进行反应:X(g)+Y(g)→Z(g)(未配平)。反应过程中X、Y、Z的物质的量变化如图1所示;若保持其他条件不变温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。则下列结论错误的是
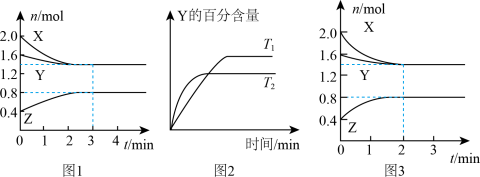

A.反应方程式为:3X(g)+Y(g) 2Z(g) 2Z(g) |
| B.0~3min,反应速率v(Z)=0.067mol∙L-1∙min-1 |
| C.其他条件不变,升高温度,化学平衡正向移动 |
| D.如图3所示的反应进程,改变的条件可能是增大压强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】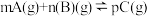 的速率和平衡的影响图象如下,下列判断正确的是
的速率和平衡的影响图象如下,下列判断正确的是

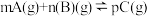 的速率和平衡的影响图象如下,下列判断正确的是
的速率和平衡的影响图象如下,下列判断正确的是
A.由图1可知, ,该反应正反应为吸热反应 ,该反应正反应为吸热反应 |
B.由图2可知,该反应 |
C.图3中,表示反应速率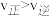 的是点3 的是点3 |
| D.图4中,a曲线一定是使用了催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g) CH3OH(g) ΔH。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是
CH3OH(g) ΔH。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是

 CH3OH(g) ΔH。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是
CH3OH(g) ΔH。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控温,进行实验,测得相关数据如下图1和图2。下列叙述不正确的是
| A.该反应的ΔH<0 |
| B.在500℃条件下达平衡时CO 的转化率为60% |
| C.平衡常数K1(3000C)<K2(5000C) |
| D.图2中达化学平衡的点为c、d、e |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】制备水煤气的反应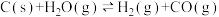
 ,下列说法正确的是
,下列说法正确的是
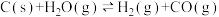
 ,下列说法正确的是
,下列说法正确的是A.该反应 |
| B.升高温度,反应速率增大 |
| C.恒温下,增大总压,H2O(g)的平衡转化率不变 |
| D.恒温恒压下,加入催化剂,平衡常数增大 |
您最近一年使用:0次

 和改性的
和改性的 基催化剂,可打通从合成气经草酸二甲酯常压催化加氢制备乙二醇的技术难关。下列说法正确的是
基催化剂,可打通从合成气经草酸二甲酯常压催化加氢制备乙二醇的技术难关。下列说法正确的是 2C(g),下图中曲线是不同温度下的平衡转化率曲线,图中a、b、c三点,则下列说法正确的是
2C(g),下图中曲线是不同温度下的平衡转化率曲线,图中a、b、c三点,则下列说法正确的是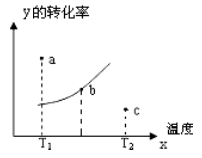
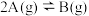
 ,反应起始时仅通入一定量的A(g),根据实验测得的数据,绘制的c-t图像如图。下列有关说法错误的是
,反应起始时仅通入一定量的A(g),根据实验测得的数据,绘制的c-t图像如图。下列有关说法错误的是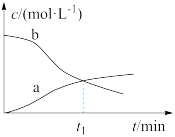
 ,
,
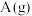 的总键能大于
的总键能大于
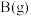 的总键能
的总键能 时表示
时表示 ,但反应未达到平衡状态
,但反应未达到平衡状态

