已知常温下:
① ,
, ,
, ,
, ;
;
②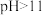 时,
时, 会转化为
会转化为 ;
;
③离子完全除去的标准:该离子浓度 。
。
某工业废水中含有 和
和 ,可采用沉淀法将其除去。
,可采用沉淀法将其除去。
(1)若加入 来沉淀
来沉淀 和
和 ,当溶液中
,当溶液中 和
和 共存时,
共存时,
___________ 。
(2)若加入 溶液来调节
溶液来调节 ,使
,使 和
和 完全沉淀,
完全沉淀, 应满足的范围为
应满足的范围为___________ 。
①
 ,
, ,
, ,
, ;
;②
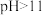 时,
时, 会转化为
会转化为 ;
;③离子完全除去的标准:该离子浓度
 。
。某工业废水中含有
 和
和 ,可采用沉淀法将其除去。
,可采用沉淀法将其除去。(1)若加入
 来沉淀
来沉淀 和
和 ,当溶液中
,当溶液中 和
和 共存时,
共存时,
(2)若加入
 溶液来调节
溶液来调节 ,使
,使 和
和 完全沉淀,
完全沉淀, 应满足的范围为
应满足的范围为
20-21高二·全国·单元测试 查看更多[2]
更新时间:2021-08-07 21:27:18
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】碱式硫酸铁[Fe(OH)SO4]是黄褐色固体,常用作媒染剂和净水剂。一种利用废铁屑(含少量Al、Al2O3、Fe2O3 等杂质)生产碱式硫酸铁的工艺流程如图所示:
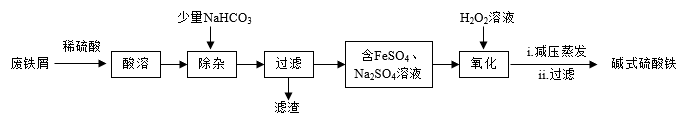
已知:①部分金属阳离子生成氢氧化物沉淀时溶液的pH如表:
②Fe(OH)2+发生电离:Fe(OH)2+ Fe3++OH-。
Fe3++OH-。
请回答下列问题:
(1)加入少量NaHCO3,调节pH的范围是___________ 。
(2)“氧化”过程中,发生反应的离子方程式为___________ ;该过程某同学选用稀硝酸代替H2O2溶液完成反应,你认为不足之处是___________ 。
(3)“氧化”过程中,若硫酸加入量过小,容易生成___________ (填化学式)沉淀;若硫酸加入量过大,不利于产品形成,试从平衡移动的角度分析原因是___________ 。
(4)将所得产品加蒸馏水溶解,为检验是否含有Fe2+,最好选用的试剂是___________ (填字母代号)。
A.氯水 B.KSCN溶液 C.K3[Fe(CN)6]溶液 D.H2O2溶液

已知:①部分金属阳离子生成氢氧化物沉淀时溶液的pH如表:
| 金属阳离子 | Fe2+ | Fe3+ | Al3+ |
| 开始沉淀 | 7.5 | 2.3 | 3.4 |
| 沉淀完全 | 9.7 | 3.2 | 4.4 |
②Fe(OH)2+发生电离:Fe(OH)2+
 Fe3++OH-。
Fe3++OH-。请回答下列问题:
(1)加入少量NaHCO3,调节pH的范围是
(2)“氧化”过程中,发生反应的离子方程式为
(3)“氧化”过程中,若硫酸加入量过小,容易生成
(4)将所得产品加蒸馏水溶解,为检验是否含有Fe2+,最好选用的试剂是
A.氯水 B.KSCN溶液 C.K3[Fe(CN)6]溶液 D.H2O2溶液
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】锑(Sb)常用作阻燃剂、电极材料、催化剂等物质的原材料。一种以辉锑矿(主要成分为Sb2S3,还含有Fe2O3、Al2O3、MgO、SiO2等)为原料提取锑的工艺如图:
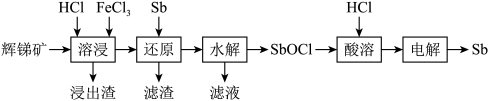
已知:溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
回答下列问题:
(1)“溶浸”时氧化产物是S,Sb2S3被氧化的化学方程式为____ 。
(2)“水解”时需控制溶液pH=2.5。
①Sb3+发生水解的离子方程式为____ 。
②下列能促进该水解反应的措施有____ (填字母)。
A.升高温度 B.增大c(H+) C.增大c(Cl-) D.加入Na2CO3粉末
③为避免水解产物中混入Fe(OH)3,Fe3+浓度应小于____ mol•L-1。
(3)“滤液”中含有的金属阳离子有____ 。向“滤液”中通入足量____ (填化学式)气体,再将滤液pH调至3.5,可析出Fe(OH)3沉淀。
(4)Sb可由SbCl 电解制得,阴极的电极反应式为
电解制得,阴极的电极反应式为____ 。

已知:溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
| 金属离子 | Fe3+ | Al3+ | Fe2+ | Mg2+ |
| 开始沉淀时(c=0.01mol•L-1)的pH | 2.2 | 3.7 | 7.5 | 9.6 |
| 完全沉淀时(c=1.0×10-5mol•L-1)的pH | 3.2 | 4.7 | 9.0 | 11.1 |
(1)“溶浸”时氧化产物是S,Sb2S3被氧化的化学方程式为
(2)“水解”时需控制溶液pH=2.5。
①Sb3+发生水解的离子方程式为
②下列能促进该水解反应的措施有
A.升高温度 B.增大c(H+) C.增大c(Cl-) D.加入Na2CO3粉末
③为避免水解产物中混入Fe(OH)3,Fe3+浓度应小于
(3)“滤液”中含有的金属阳离子有
(4)Sb可由SbCl
 电解制得,阴极的电极反应式为
电解制得,阴极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】钒(V)广泛应用于冶金、化工、航天等领域。一种以钒渣(主要成分是FeV2O4、Fe2SiO4、MnV2O4等)为原料制取金属钒的工艺流程如图所示:

已知:①VO 具有强氧化性,主要存在于pH<2的溶液中,pH>2时转化成酸式多钒酸盐。
具有强氧化性,主要存在于pH<2的溶液中,pH>2时转化成酸式多钒酸盐。
②溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
回答下列问题:
(1)FeV2O4中Fe为+2价,Fe2+的核外电子排布式为:______ ;基态钒原子价层电子排布图为_____ 。
(2)“焙烧I”中将MgO磨成粉末从炉顶投料,空气从炉底鼓入,目的是_____ ,FeV2O4转化为Mg2V2O7和Fe2O3的化学方程式为_____ 。
(3)“沉钒”可得到(NH4)4H2V10O28沉淀,“焙烧II”中发生反应的化学方程式为_____ 。
(4)“沉钒”中,下列说法正确的是_____ 。
(5)“沉钒”所得滤液中加入氨水调节溶液pH=x,过滤得到Mn(OH)2沉淀和溶液A,溶液A中Mg2+浓度为0.024g•L-1,为尽可能多地回收Mn2+,并避免Mn(OH)2中混入Mg(OH)2,应控制x=_____ 。
(6)此工艺流程中可循环利用的物质为______ 。
(7)一种钒的硫化物的晶胞结构(图a)及其俯视图(图b)如图所示:
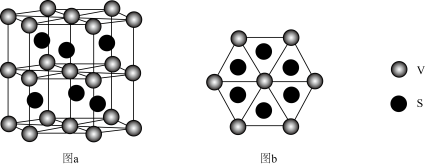
①该钒的硫化物晶胞中含_____ 个V原子。
②该钒的硫化物的晶体中,与每个S原子最近且等距的V原子的个数是_____ 。

已知:①VO
 具有强氧化性,主要存在于pH<2的溶液中,pH>2时转化成酸式多钒酸盐。
具有强氧化性,主要存在于pH<2的溶液中,pH>2时转化成酸式多钒酸盐。②溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
| 金属离子 | Fe3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀时(c=0.1mol•L-1)的pH | 1.9 | 7.0 | 8.1 | 8.9 |
| 沉淀完全时(c=1.0×10-5mol•L-1)的pH | 3.2 | 9.0 | 10.1 | 10.9 |
(1)FeV2O4中Fe为+2价,Fe2+的核外电子排布式为:
(2)“焙烧I”中将MgO磨成粉末从炉顶投料,空气从炉底鼓入,目的是
(3)“沉钒”可得到(NH4)4H2V10O28沉淀,“焙烧II”中发生反应的化学方程式为
(4)“沉钒”中,下列说法正确的是
| A.升温有利于加快“沉钒”速率,该过程应在高温下进行 |
| B.增大NH4Cl的浓度能降低(NH4)4H2V10O28的溶解度 |
| C.实际生产中,沉钒时间越长越好 |
| D.温度超过50℃,溶液中逸出的氨气增多 |
(6)此工艺流程中可循环利用的物质为
(7)一种钒的硫化物的晶胞结构(图a)及其俯视图(图b)如图所示:

①该钒的硫化物晶胞中含
②该钒的硫化物的晶体中,与每个S原子最近且等距的V原子的个数是
您最近一年使用:0次



