Ⅰ.完成下列填空
(1)已知在25℃、101kPa下,1g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7kJ的热量,试写出乙醇燃烧热的热化学方程式___________
(2)已知:C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5kJ/mol
2H2+O2(g)=2H2O(l) ΔH2=-517.6kJ/mol
2C2H2+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599.2kJ/mol
计算25℃时,由C(石墨,s)和H2(g)反应生成C2H2(g)的热化学方程式为___________ 。
Ⅱ.分别取50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。
(3)下图装置缺少一种玻璃仪器,该仪器的名称为___________ ;若用铜棒代替该仪器,会导致ΔH计算结果___________ (偏低、偏高或无影响),原因是___________ 。
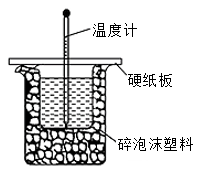
(4)某学生实验记录数据如下:(已知ρ溶液=1g/cm3,c溶液=4.18J/(g·℃)),依据该学生的实验数据计算,该实验测得的中和热为ΔH=___________ 。(保留小数点后1位)
Ⅲ.2SO2(g)+O2(g) 2SO3(g) △H反应过程的能量变化如图所示。已知:1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
2SO3(g) △H反应过程的能量变化如图所示。已知:1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
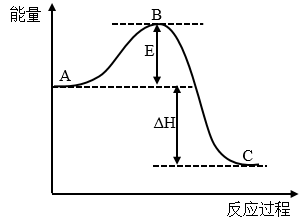
(5)图中A表示___________ 的能量(选用SO2、O2、SO3填空)。E的大小对该反应的反应热___________ (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点___________ (填“升高”还是“降低”),△H___________ (填“变大”、“变小”或“不变”)。
(6)题中反应的中△H=___________ kJ·mol-1。
(1)已知在25℃、101kPa下,1g乙醇在氧气中充分燃烧生成二氧化碳和液态水释放出29.7kJ的热量,试写出乙醇燃烧热的热化学方程式
(2)已知:C(石墨,s)+O2(g)=CO2(g) ΔH1=-393.5kJ/mol
2H2+O2(g)=2H2O(l) ΔH2=-517.6kJ/mol
2C2H2+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599.2kJ/mol
计算25℃时,由C(石墨,s)和H2(g)反应生成C2H2(g)的热化学方程式为
Ⅱ.分别取50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。
(3)下图装置缺少一种玻璃仪器,该仪器的名称为

(4)某学生实验记录数据如下:(已知ρ溶液=1g/cm3,c溶液=4.18J/(g·℃)),依据该学生的实验数据计算,该实验测得的中和热为ΔH=
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
Ⅲ.2SO2(g)+O2(g)
 2SO3(g) △H反应过程的能量变化如图所示。已知:1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
2SO3(g) △H反应过程的能量变化如图所示。已知:1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
(5)图中A表示
(6)题中反应的中△H=
更新时间:2021-10-09 21:35:34
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】氯气和含氯化合物在有机合成中具有重要作用。回答下列问题:
(1)烷烃与氯气光照条件下的反应属于自由基(标注“*”的物种)取代反应。
①已知: 、
、 键的键能分别为
键的键能分别为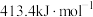 、
、 ,则
,则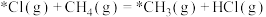 的
的
___________ 。
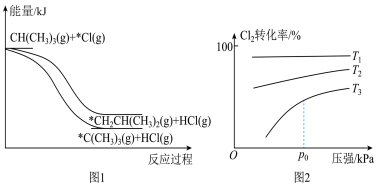
②异丁烷与氯气发生光照取代的一步反应的能量变化如图1所示。则异丁烷 中
中 键的键能比
键的键能比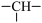 中
中 键的键能
键的键能___________ (填“大”“小”或“相等”),理由为___________ 。
(2)丙烯与氯气可发生的反应:
Ⅰ、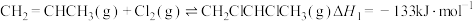
Ⅱ、
①将 和
和 的混合气体以一定流速通过填充有催化剂的反应器,出口气中含有
的混合气体以一定流速通过填充有催化剂的反应器,出口气中含有 、
、 、
、 、
、 、
、 。实验测得
。实验测得 的转化率与温度、压强的关系如图2所示。已知
的转化率与温度、压强的关系如图2所示。已知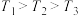 ,
, 转化率随温度升高而增大的原因为
转化率随温度升高而增大的原因为___________ ;温度为 时,随压强增大,
时,随压强增大, 的转化率基本保持不变的原因为
的转化率基本保持不变的原因为___________ 。
②一定温度下,向填充有催化剂的恒容密闭容器中以物质的量之比为1:1充入 和
和 ,实验测得反应前容器内气体压强为
,实验测得反应前容器内气体压强为 ,反应达到平衡时容器内气体压强为
,反应达到平衡时容器内气体压强为 、
、 的分压为
的分压为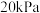 。则
。则 的平衡转化率为
的平衡转化率为___________ ;反应Ⅱ的平衡常数
___________ ( 是用分压表示的平衡常数)。
是用分压表示的平衡常数)。
③同时提高反应Ⅰ的速率和选择性的措施为___________ 。
(1)烷烃与氯气光照条件下的反应属于自由基(标注“*”的物种)取代反应。
①已知:
 、
、 键的键能分别为
键的键能分别为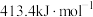 、
、 ,则
,则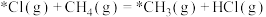 的
的
②异丁烷与氯气发生光照取代的一步反应的能量变化如图1所示。则异丁烷
 中
中 键的键能比
键的键能比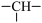 中
中 键的键能
键的键能
(2)丙烯与氯气可发生的反应:
Ⅰ、
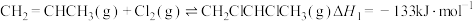
Ⅱ、

①将
 和
和 的混合气体以一定流速通过填充有催化剂的反应器,出口气中含有
的混合气体以一定流速通过填充有催化剂的反应器,出口气中含有 、
、 、
、 、
、 、
、 。实验测得
。实验测得 的转化率与温度、压强的关系如图2所示。已知
的转化率与温度、压强的关系如图2所示。已知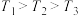 ,
, 转化率随温度升高而增大的原因为
转化率随温度升高而增大的原因为 时,随压强增大,
时,随压强增大, 的转化率基本保持不变的原因为
的转化率基本保持不变的原因为②一定温度下,向填充有催化剂的恒容密闭容器中以物质的量之比为1:1充入
 和
和 ,实验测得反应前容器内气体压强为
,实验测得反应前容器内气体压强为 ,反应达到平衡时容器内气体压强为
,反应达到平衡时容器内气体压强为 、
、 的分压为
的分压为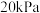 。则
。则 的平衡转化率为
的平衡转化率为
 是用分压表示的平衡常数)。
是用分压表示的平衡常数)。③同时提高反应Ⅰ的速率和选择性的措施为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】为减少 对环境造成的影响,可采用“
对环境造成的影响,可采用“ 催化加经制甲醇”方法将其资源化利用。该反应体系中涉及以下两个反应:
催化加经制甲醇”方法将其资源化利用。该反应体系中涉及以下两个反应:
I.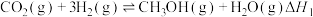
Ⅱ.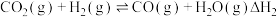
回答下列问题:
(1)反应Ⅰ、Ⅱ的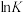 (
( 代表化学平衡常数)随
代表化学平衡常数)随 (温度的倒数)的变化如图所示。
(温度的倒数)的变化如图所示。
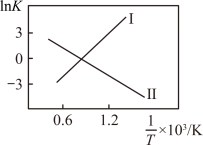

___________ 0(填“>”、“<”或“=”);升高温度,反应 的化学平衡常数
的化学平衡常数___________ (填“增大”、“减小”或“不变”)。
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________(填字母)。
(3)恒压下将 和
和 按体积比
按体积比 混合,在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内
混合,在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内 的选择性和产率随温度的变化如图。
的选择性和产率随温度的变化如图。
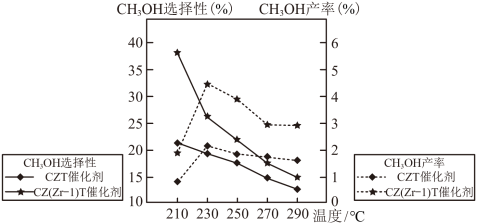
其中: 的选择性
的选择性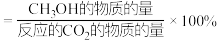
①在上述条件下合成甲醇的工业条件是___________ (填字母)。
A. B.
B. C.催化CZT D.催化剂
C.催化CZT D.催化剂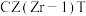
②在 以上,升高温度
以上,升高温度 的转化率增大,但甲醇的产率降低,原因是
的转化率增大,但甲醇的产率降低,原因是___________ 。
(4)恒温恒压密闭容器中,加入 和
和 ,只发生反应I和反应Ⅱ,初始压强为
,只发生反应I和反应Ⅱ,初始压强为 ,在
,在 发生反应,反应达平衡时,
发生反应,反应达平衡时, 的转化率为
的转化率为 ,容器体积减小
,容器体积减小 。则反应Ⅱ的平衡常数
。则反应Ⅱ的平衡常数
___________ (保留两位有效数字)。
 对环境造成的影响,可采用“
对环境造成的影响,可采用“ 催化加经制甲醇”方法将其资源化利用。该反应体系中涉及以下两个反应:
催化加经制甲醇”方法将其资源化利用。该反应体系中涉及以下两个反应:I.
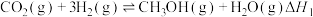
Ⅱ.
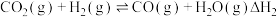
回答下列问题:
(1)反应Ⅰ、Ⅱ的
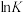 (
( 代表化学平衡常数)随
代表化学平衡常数)随 (温度的倒数)的变化如图所示。
(温度的倒数)的变化如图所示。

 的化学平衡常数
的化学平衡常数(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有___________(填字母)。
A.增大 的浓度,反应Ⅰ的平衡向正反应方向移动 的浓度,反应Ⅰ的平衡向正反应方向移动 |
| B.降低温度,反应Ⅰ和Ⅱ的正、逆反应速率都减小 |
| C.恒温恒容下充入氦气,反应Ⅰ的平衡向正反应方向移动 |
| D.增大压强,反应I和Ⅱ重新达到平衡的时间不同 |
(3)恒压下将
 和
和 按体积比
按体积比 混合,在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内
混合,在不同催化剂作用下发生反应Ⅰ和反应Ⅱ,在相同的时间段内 的选择性和产率随温度的变化如图。
的选择性和产率随温度的变化如图。
其中:
 的选择性
的选择性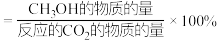
①在上述条件下合成甲醇的工业条件是
A.
 B.
B. C.催化CZT D.催化剂
C.催化CZT D.催化剂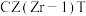
②在
 以上,升高温度
以上,升高温度 的转化率增大,但甲醇的产率降低,原因是
的转化率增大,但甲醇的产率降低,原因是(4)恒温恒压密闭容器中,加入
 和
和 ,只发生反应I和反应Ⅱ,初始压强为
,只发生反应I和反应Ⅱ,初始压强为 ,在
,在 发生反应,反应达平衡时,
发生反应,反应达平衡时, 的转化率为
的转化率为 ,容器体积减小
,容器体积减小 。则反应Ⅱ的平衡常数
。则反应Ⅱ的平衡常数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.某实验小组用 溶液和
溶液和 硫酸溶液进行中和热的测定。
硫酸溶液进行中和热的测定。
(1)写出该反应的热化学方程式(中和热为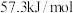 ):
):_______ ;
(2)取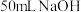 溶液和
溶液和 硫酸溶液进行实验,实验数据如下表。
硫酸溶液进行实验,实验数据如下表。
已知:反应前后,溶液的比热容均近似为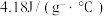 、溶液的密度均近似为
、溶液的密度均近似为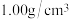 ,忽略溶液体积、质量变化。请计算中和热
,忽略溶液体积、质量变化。请计算中和热
_______ (保留三位有效数字)。
Ⅱ.已知①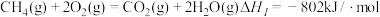 平衡常数
平衡常数
② 平衡常数
平衡常数
③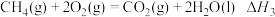 平衡常数
平衡常数
(3)比较
_______  (填“>”,“<”或“=”)
(填“>”,“<”或“=”)
(4)反应③的平衡常数表达式为
_______ ;
(5)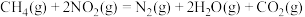 的平衡常数
的平衡常数
_______ (用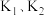 表示)
表示)
 溶液和
溶液和 硫酸溶液进行中和热的测定。
硫酸溶液进行中和热的测定。(1)写出该反应的热化学方程式(中和热为
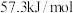 ):
):(2)取
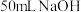 溶液和
溶液和 硫酸溶液进行实验,实验数据如下表。
硫酸溶液进行实验,实验数据如下表。| 温度实验次数 | 起始温度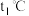 | 终止温度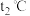 | ||
 |  | 平均值 | ||
| 1 | 26.4 | 26.2 | 26.3 | 29.8 |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 |
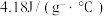 、溶液的密度均近似为
、溶液的密度均近似为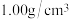 ,忽略溶液体积、质量变化。请计算中和热
,忽略溶液体积、质量变化。请计算中和热
Ⅱ.已知①
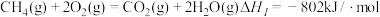 平衡常数
平衡常数
②
 平衡常数
平衡常数
③
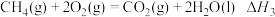 平衡常数
平衡常数
(3)比较

 (填“>”,“<”或“=”)
(填“>”,“<”或“=”)(4)反应③的平衡常数表达式为

(5)
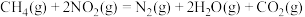 的平衡常数
的平衡常数
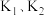 表示)
表示)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】Ⅰ、2SO2(g)+O2(g) 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
(1)E的大小对该反应的反应热_______ (填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点_______ (填“升高”还是“降低”)。
(2)完成SO2氧化为SO3的热化学方程式_______ 。
II、氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答:
(3)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=
2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=_______ 。平衡时H2的转化率为_______ %。
(4)平衡后,若提高H2的转化率,可以采取的措施有_______ (任写一项)。
(5)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示。请完成下列问题:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示。请完成下列问题:
①试比较K1、K2的大小,K1_______ K2(填“<、>、=”)
②400℃时,反应2NH3(g) N2(g)+3H2(g)的化学平衡常数为
N2(g)+3H2(g)的化学平衡常数为_______ 。当测得NH3、N2和H2物质的量分别为3mol、2mol和1mol时,则该反应的v(N2)正_______ v(N2)逆(填“<、>、=”)。
 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
已知1molSO2(g)氧化为1molSO3(g)的ΔH=-99kJ·mol-1。请回答下列问题:
(1)E的大小对该反应的反应热
(2)完成SO2氧化为SO3的热化学方程式
II、氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答:
(3)若在一容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2在一定条件下发生反应:N2(g)+3H2(g)
 2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=
2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则前5分钟的平均反应速率v(N2)=(4)平衡后,若提高H2的转化率,可以采取的措施有
(5)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g)
 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示。请完成下列问题:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示。请完成下列问题:| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1
②400℃时,反应2NH3(g)
 N2(g)+3H2(g)的化学平衡常数为
N2(g)+3H2(g)的化学平衡常数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
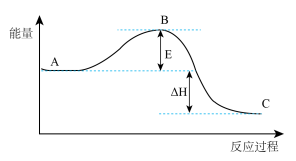
【推荐2】 已知:A为含金属离子的淡黄色固体化合物,E、X为空气中常见气体,A、B、C、D含有相同的金属离子,其转化关系如下图(部分产物已略去)。
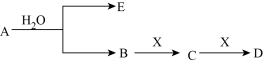
请回答下列问题:
(1)这种金属离子的离子结构示意图为____________ 。
(2) 请写出A的电子式______________________________________ 。常温常压下,15.6 g A与足量的水充分反应放出热量a kJ,写出该反应的热化学方程式为_________________________________________________________ 。
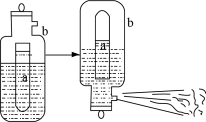
(3)D常用于一种泡沫灭火器,构造如图。内筒a是玻璃瓶,外筒b是钢瓶,平时泡沫灭火器内筒外筒盛有液态试剂,当遇火警时,将灭火器取下倒置,内外筒液体试剂立即混合产生大量CO2泡沫灭火。从液态试剂在灭火器中长久放置和快速灭火两个角度分析,则a中盛________ ,b中盛________ ,反应的化学方程式为_______________________
(4)将一定量的气体X通入2 L B的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。

请回答:b点溶液中所含溶质的化学式为___________ ,物质的量之比为____________ ,

请回答下列问题:
(1)这种金属离子的离子结构示意图为
(2) 请写出A的电子式

(3)D常用于一种泡沫灭火器,构造如图。内筒a是玻璃瓶,外筒b是钢瓶,平时泡沫灭火器内筒外筒盛有液态试剂,当遇火警时,将灭火器取下倒置,内外筒液体试剂立即混合产生大量CO2泡沫灭火。从液态试剂在灭火器中长久放置和快速灭火两个角度分析,则a中盛
(4)将一定量的气体X通入2 L B的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。

请回答:b点溶液中所含溶质的化学式为
您最近一年使用:0次
【推荐3】“一带一路”为中国化工企业开辟了新的国际市场,而能源、资源整合及环境治理是保驾护航的基础。
Ⅰ.在能源领域,科学家提出“绿色自由“”构想: 把含有大量CO2的空气吹入K2CO3溶液中,再把CO2从溶液中提取出来,并使之与H2反应生成可再生能源甲醇。其工艺流程如下图所示:

(1)在合成塔中,若有4400gCO2与足量H2完企反应,生成气态的H2O和气态甲醇,可放出5370kJ的热量,写出该反应的热化学方程式__________ 。
(2)一定条件下,向2L恒容密闭容器中充入1molCO2和3molH2,在不同催化剂作用下发生反应Ⅰ、反应Ⅱ与反应Ⅲ,相同时间内CO2的转化率随温度变化如下图所示:
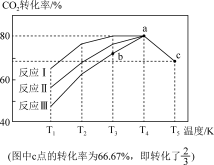
①催化剂效果最佳的反应是__________ (填“反应I”,“反应II”,“反应III”)。
②b点v (正)______ v (逆)(填 “>”, “<”, “=”)。
③c点时该反应的平衡常数K =_________ 。(写单位)
Ⅱ.环境治理中,安装汽车尾气催化转化器的反应是:2NO(g)+2CO(g)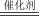 2CO2(g)+N2(g)ΔH<0
2CO2(g)+N2(g)ΔH<0
(3)温度升高K值_______ (填“增大”或“减小”)
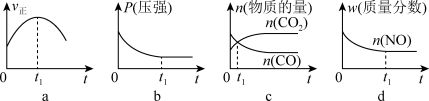
(4)若反应在恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是____________ 。
(5)下列所示装置可以在吸收SO2的同时,用阴极排出的溶液吸收NO2,(电极均为惰性电极)
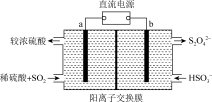
a极为______ 极(填“阴”、“阳”),b极的电极反应式为_________ ,结合电极反应式简述该装置能吸收SO2的原理:__________ 。
Ⅰ.在能源领域,科学家提出“绿色自由“”构想: 把含有大量CO2的空气吹入K2CO3溶液中,再把CO2从溶液中提取出来,并使之与H2反应生成可再生能源甲醇。其工艺流程如下图所示:

(1)在合成塔中,若有4400gCO2与足量H2完企反应,生成气态的H2O和气态甲醇,可放出5370kJ的热量,写出该反应的热化学方程式
(2)一定条件下,向2L恒容密闭容器中充入1molCO2和3molH2,在不同催化剂作用下发生反应Ⅰ、反应Ⅱ与反应Ⅲ,相同时间内CO2的转化率随温度变化如下图所示:

①催化剂效果最佳的反应是
②b点v (正)
③c点时该反应的平衡常数K =
Ⅱ.环境治理中,安装汽车尾气催化转化器的反应是:2NO(g)+2CO(g)
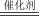 2CO2(g)+N2(g)ΔH<0
2CO2(g)+N2(g)ΔH<0(3)温度升高K值
(4)若反应在恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是

(5)下列所示装置可以在吸收SO2的同时,用阴极排出的溶液吸收NO2,(电极均为惰性电极)

a极为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】按要求填空:
(1)已知常温下拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则 与
与 反应生成
反应生成 的热化学方程式为:
的热化学方程式为:___________ 。
(2)已知反应①
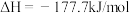
②

③
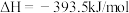
④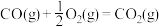
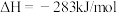
⑤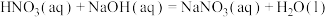

上述热化学方程式中,不正确的有___________ ;(填序号,以下同)表示燃烧热的热化学方程式是___________ ;表示中和热的热化学方程式是___________ 。
(3)下列六种溶液① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
加热蒸干后能得到原来物质的是(可以含有结晶水)___________ (填序号);写出②和③混合反应得离子方程式___________ ;写出②和⑤混合反应的离子方程式___________ ;等物质的量的①和②混合所得溶液中物料守恒关系式___________ 。
(1)已知常温下拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则
 与
与 反应生成
反应生成 的热化学方程式为:
的热化学方程式为:(2)已知反应①

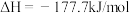
②


③

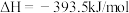
④
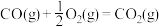
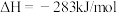
⑤
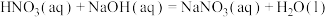

上述热化学方程式中,不正确的有
(3)下列六种溶液①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
加热蒸干后能得到原来物质的是(可以含有结晶水)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】在A~I的元素中选择符合题意的元素,按要求回答下列问题:
(1)只有负价而无正价的是______ (填元素名称);
(2)最高价氧化物的水化物酸性最强的是____ (填化学式);
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的化合物的结构式_____ ;
(4)在B、C、D、J、 E、F、G、H中,原子半径最大的是____ (填原子符号);
(5)画出上述元素中金属性最强的元素的原子结构示意图______ ;
(6)C单质与氢氧化钠溶液反应的离子方程式________________________ ;
(7)用电子式表示E单质的形成过程_______________________ ;
(8)写出冶炼B单质的化学方程式____________________ ;
(9)D的最简单氢化物的燃烧热为890.3 kJ/mol,写出D的最简单氢化物燃烧热的热化学方程式_____ ;
(10)写出NaHSO4熔融时电离方程式______________________ 。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | |||||
| 3 | B | C | J | F | H | I |
(2)最高价氧化物的水化物酸性最强的是
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的化合物的结构式
(4)在B、C、D、J、 E、F、G、H中,原子半径最大的是
(5)画出上述元素中金属性最强的元素的原子结构示意图
(6)C单质与氢氧化钠溶液反应的离子方程式
(7)用电子式表示E单质的形成过程
(8)写出冶炼B单质的化学方程式
(9)D的最简单氢化物的燃烧热为890.3 kJ/mol,写出D的最简单氢化物燃烧热的热化学方程式
(10)写出NaHSO4熔融时电离方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料,而氢气、二甲醚等都是很有发展前景的新能源。
(1)在25℃、101kPa时,1gCH4完全燃烧生成液态水时放出的热量是55.64 kJ,则表示甲烷燃烧热的热化学方程式是___________________________________________ 。
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)===3CO2(g)+4H2O(l)
ΔH=-2 220.0 kJ· mol-1,已知CO气体燃烧的热化学方程式为2CO(g)+O2(g)===2CO2(g) ΔH=-565.14 kJ·mol-1,试计算相同物质的量的C3H8和CO燃烧产生的热量的比值________ (保留小数点后一位)。
(3)氢气既能与氮气发生反应又能与氧气发生反应,但是反应的条件却不相同。
已知:2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ· mol-1
3H2(g)+N2(g) 2NH3(g) ΔH=-92.4 kJ· mol-1
2NH3(g) ΔH=-92.4 kJ· mol-1
计算断裂1 mol N≡N键需要消耗能量________ kJ。
(4)由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:
甲醇合成反应:①CO(g)+2H2(g)===CH3OH(g) ΔH1=-90.1 kJ· mol-1
②CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH2=-49.0 kJ· mol-1
水煤气变换反应:③CO(g)+H2O(g)===CO2(g)+H2(g) ΔH3=-41.1 kJ· mol
二甲醚合成反应:④2CH3OH(g)===CH3OCH3(g)+H2O(g) ΔH4=-24.5 kJ· mol-1
由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为_______________________ 。根据化学反应原理,分析增大压强对直接制备二甲醚反应的影响:_________________________________________________ 。
(1)在25℃、101kPa时,1gCH4完全燃烧生成液态水时放出的热量是55.64 kJ,则表示甲烷燃烧热的热化学方程式是
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)===3CO2(g)+4H2O(l)
ΔH=-2 220.0 kJ· mol-1,已知CO气体燃烧的热化学方程式为2CO(g)+O2(g)===2CO2(g) ΔH=-565.14 kJ·mol-1,试计算相同物质的量的C3H8和CO燃烧产生的热量的比值
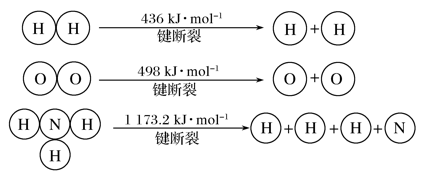
(3)氢气既能与氮气发生反应又能与氧气发生反应,但是反应的条件却不相同。
已知:2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ· mol-1
3H2(g)+N2(g)
 2NH3(g) ΔH=-92.4 kJ· mol-1
2NH3(g) ΔH=-92.4 kJ· mol-1
计算断裂1 mol N≡N键需要消耗能量
(4)由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:
甲醇合成反应:①CO(g)+2H2(g)===CH3OH(g) ΔH1=-90.1 kJ· mol-1
②CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH2=-49.0 kJ· mol-1
水煤气变换反应:③CO(g)+H2O(g)===CO2(g)+H2(g) ΔH3=-41.1 kJ· mol
二甲醚合成反应:④2CH3OH(g)===CH3OCH3(g)+H2O(g) ΔH4=-24.5 kJ· mol-1
由H2和CO直接制备二甲醚(另一产物为水蒸气)的热化学方程式为
您最近一年使用:0次
【推荐1】研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:
Fe2O3(s) + 3C(s)=2Fe(s) + 3CO(g) ΔH1=+489.0 kJ·mol-1,
C(s) +CO2(g)=2CO(g) ΔH2=+172.5kJ·mol-1
则CO(g)还原Fe2O3(s)的热化学方程式为____ 。
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式:_____ 。
(3)将CO2和H2充入1L的密闭容器中,在两种温度下发生反应:CO2(g) +3H2(g) CH3OH(g) +H2O(g)测得CH3OH的物质的量随时间的变化见下图。
CH3OH(g) +H2O(g)测得CH3OH的物质的量随时间的变化见下图。
①曲线I、Ⅱ对应的平衡常数大小关系为KⅠ___ KⅡ(填“>”或“=”或“<”)。
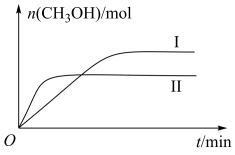
②一定温度下,往该容器中投入1 molCO2、3 mol H2,一段时间后达到平衡。若平衡后气体的压强为开始的0.8倍,则CO2的平衡转化率=____ 。
(1)CO可用于炼铁,已知:
Fe2O3(s) + 3C(s)=2Fe(s) + 3CO(g) ΔH1=+489.0 kJ·mol-1,
C(s) +CO2(g)=2CO(g) ΔH2=+172.5kJ·mol-1
则CO(g)还原Fe2O3(s)的热化学方程式为
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式:
(3)将CO2和H2充入1L的密闭容器中,在两种温度下发生反应:CO2(g) +3H2(g)
 CH3OH(g) +H2O(g)测得CH3OH的物质的量随时间的变化见下图。
CH3OH(g) +H2O(g)测得CH3OH的物质的量随时间的变化见下图。①曲线I、Ⅱ对应的平衡常数大小关系为KⅠ

②一定温度下,往该容器中投入1 molCO2、3 mol H2,一段时间后达到平衡。若平衡后气体的压强为开始的0.8倍,则CO2的平衡转化率=
您最近一年使用:0次
【推荐2】甲醇是一种很好的燃料,工业上可用多种原料通过不同的反应制得甲醇.
(1)已知在常温常压下:
CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=-442.8kJ∙mol﹣1
2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ∙mol﹣1
H2O(g)=H2O(l) △H=-44.0kJ∙mol﹣1
则2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H=
(2)已知C(s)+H2O(g)=CO(g)+H2(g) △H=akJ·mol-1
2C(s)+O2(g)=2CO(g) △H=-220kJ·mol-1
H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为____________________
(3)工业上正在研究利用来生产甲醇燃料的方法,该反应为:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0kJ∙mol﹣1
CH3OH(g)+H2O(g) △H=-49.0kJ∙mol﹣1
在某温度下,将6mol CO2和8mol H2充入容积为2L的密闭容器中,8分钟时达平衡状态,H2的转化率为75%.请回答:
①用CH3OH表示该反应在0~8min内的平均反应速率v(CH3OH)=_____ .
②此温度下该反应平衡常数K=_____ ;
(4)一氧化碳与氢气也可以合成甲醇:CO(g)+2H2(g) CH3OH(g) △H<0
CH3OH(g) △H<0
①若该反应在恒温恒容条件下进行,下列说法正确的是_____ ;
a.若混合气体的密度不再改变,说明反应已达化学平衡状态
b.反应达到平衡后,通入CH3OH(g)使压强增大,平衡向右移动
c.反应达到平衡后,通入氩气使压强增大,平衡向右移动
d.反应达到平衡后,升高温度,平衡逆向移动,平衡常数减小
e.若使用催化剂,会改变反应的途径,但反应热不变
②某温度下,在一个容积为2L的密闭容器中进行该反应,已知此温度下的平衡常数K=50L2∙mol﹣2,反应到某时刻测得各组分的物质的量如下:
请比较此时正、逆反应速率的大小:v正_____ v逆(填“>”、“<”或“=”).
(1)已知在常温常压下:
CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=-442.8kJ∙mol﹣1
2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ∙mol﹣1
H2O(g)=H2O(l) △H=-44.0kJ∙mol﹣1
则2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H=
(2)已知C(s)+H2O(g)=CO(g)+H2(g) △H=akJ·mol-1
2C(s)+O2(g)=2CO(g) △H=-220kJ·mol-1
H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为
(3)工业上正在研究利用来生产甲醇燃料的方法,该反应为:
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-49.0kJ∙mol﹣1
CH3OH(g)+H2O(g) △H=-49.0kJ∙mol﹣1在某温度下,将6mol CO2和8mol H2充入容积为2L的密闭容器中,8分钟时达平衡状态,H2的转化率为75%.请回答:
①用CH3OH表示该反应在0~8min内的平均反应速率v(CH3OH)=
②此温度下该反应平衡常数K=
(4)一氧化碳与氢气也可以合成甲醇:CO(g)+2H2(g)
 CH3OH(g) △H<0
CH3OH(g) △H<0①若该反应在恒温恒容条件下进行,下列说法正确的是
a.若混合气体的密度不再改变,说明反应已达化学平衡状态
b.反应达到平衡后,通入CH3OH(g)使压强增大,平衡向右移动
c.反应达到平衡后,通入氩气使压强增大,平衡向右移动
d.反应达到平衡后,升高温度,平衡逆向移动,平衡常数减小
e.若使用催化剂,会改变反应的途径,但反应热不变
②某温度下,在一个容积为2L的密闭容器中进行该反应,已知此温度下的平衡常数K=50L2∙mol﹣2,反应到某时刻测得各组分的物质的量如下:
| 物质 | CO | H2 | CH3OH |
| 物质的量/(mol) | 0.4 | 0.4 | 0.8 |
请比较此时正、逆反应速率的大小:v正
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】中科院大连化学物理研究所的一项最新成果实现了甲烷高效生产乙烯,如图所示,甲烷在催化作用下脱氢,在不同温度下分别形成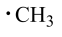 、
、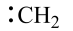 、
、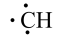 等自由基,在气相中经自由基:CH2偶联反应生成乙烯(该反应过程可逆)
等自由基,在气相中经自由基:CH2偶联反应生成乙烯(该反应过程可逆)
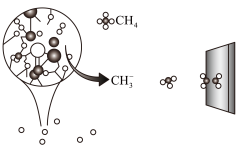
(1)已知相关物质的燃烧热如表所示,写出甲烷制备乙烯的热化学方程式__________ 。
(2)现代石油化工采用Ag作催化剂,可实现乙烯与氧气制备X(分子式为C2H4O,不含双键)该反应符合最理想的原子经济,则反应产物是__________ (填结构简式)
(3)在400℃时,向初始体积为1L的恒压密闭反应器中充入1molCH4,发生(1)中反应,测得平衡混合气体中C2H4的体积分数为25.0%。则:
①在该温度下,其平衡常数KC=__________ 。
②若向该反应器中通入高温水蒸气(不参加反应,高于400℃),则C2H4的产率__________ 。(填“增大”“减小”“不变”或“无法确定”),理由是__________ 。
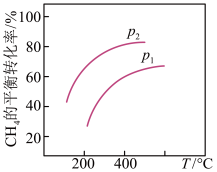
③若反应器的体积固定,不同压强下可得变化如图所示,则压强p1与p2的大小关系是__________ 。
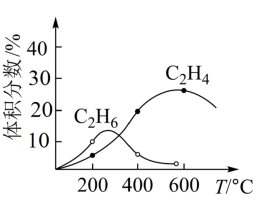
(4)实际制备C2H4时,通常存在副反应2CH4(g) C2H6(g)+H2(g)。反应器和CH4起始量不变,不同温度下C2H6和C2H4的体积分数与温度的关系曲线如图所示。在温度高于600℃时,有可能得到一种较多的双碳有机副产物的名称是
C2H6(g)+H2(g)。反应器和CH4起始量不变,不同温度下C2H6和C2H4的体积分数与温度的关系曲线如图所示。在温度高于600℃时,有可能得到一种较多的双碳有机副产物的名称是__________ 。
(5)C2H4、C2H6常常作为燃料电池的原料,请写出C2H4在NaOH溶液中做燃料电池的负极的电极反应方程式__________ 。
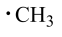 、
、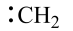 、
、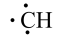 等自由基,在气相中经自由基:CH2偶联反应生成乙烯(该反应过程可逆)
等自由基,在气相中经自由基:CH2偶联反应生成乙烯(该反应过程可逆)
| 物质 | 燃烧热/(kJ·mol-1) |
| 氢气 | 285.8 |
| 甲烷 | 890.3 |
| 乙烯 | 1411.0 |
(1)已知相关物质的燃烧热如表所示,写出甲烷制备乙烯的热化学方程式
(2)现代石油化工采用Ag作催化剂,可实现乙烯与氧气制备X(分子式为C2H4O,不含双键)该反应符合最理想的原子经济,则反应产物是
(3)在400℃时,向初始体积为1L的恒压密闭反应器中充入1molCH4,发生(1)中反应,测得平衡混合气体中C2H4的体积分数为25.0%。则:
①在该温度下,其平衡常数KC=
②若向该反应器中通入高温水蒸气(不参加反应,高于400℃),则C2H4的产率
③若反应器的体积固定,不同压强下可得变化如图所示,则压强p1与p2的大小关系是

(4)实际制备C2H4时,通常存在副反应2CH4(g)
 C2H6(g)+H2(g)。反应器和CH4起始量不变,不同温度下C2H6和C2H4的体积分数与温度的关系曲线如图所示。在温度高于600℃时,有可能得到一种较多的双碳有机副产物的名称是
C2H6(g)+H2(g)。反应器和CH4起始量不变,不同温度下C2H6和C2H4的体积分数与温度的关系曲线如图所示。在温度高于600℃时,有可能得到一种较多的双碳有机副产物的名称是
(5)C2H4、C2H6常常作为燃料电池的原料,请写出C2H4在NaOH溶液中做燃料电池的负极的电极反应方程式
您最近一年使用:0次



