已知以下四个反应:
①4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②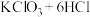 (浓)
(浓)
③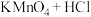 (浓)
(浓)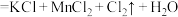 (未配平)
(未配平)
④
根据以上四个反应,回答下列有关问题:
(1)反应①中,氧化产物与还原产物的质量比为___________ 。(写最简整数比)
(2)反应②中氧化剂与还原剂的个数之比为___________ 。(写最简整数比)
(3)若要制得相同质量的氯气,①②反应中电子转移的数目之比为_______ 。(写最简整数比)
(4)请将反应③配平:
 (浓)=
(浓)=



________
(5)请用单线桥表示反应④的电子转移情况:
__________
(6)将 ,
, ,
, 按由强到弱的氧化性顺序排序
按由强到弱的氧化性顺序排序___________ 。(例A>B>C)
①4HCl(浓)+MnO2
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O②
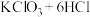 (浓)
(浓)
③
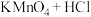 (浓)
(浓)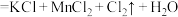 (未配平)
(未配平)④

根据以上四个反应,回答下列有关问题:
(1)反应①中,氧化产物与还原产物的质量比为
(2)反应②中氧化剂与还原剂的个数之比为
(3)若要制得相同质量的氯气,①②反应中电子转移的数目之比为
(4)请将反应③配平:

 (浓)=
(浓)=



(5)请用单线桥表示反应④的电子转移情况:

(6)将
 ,
, ,
, 按由强到弱的氧化性顺序排序
按由强到弱的氧化性顺序排序
更新时间:2021-10-26 11:55:17
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。下列反应可制得ClO2:NaClO3+ H2O2+ H2SO4→ClO2↑+Na2SO4+O2↑+H2O(未配平)
(1)反应中被氧化的元素是________ ,每生成2a个ClO2时有______ 个电子转移。
(2)写出配平后的方程式:___________ ,并用双线桥表示电子转移的方向和数目。
(3)高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂。其工业合成原理是下列物质间发生氧化还原反应:Fe(OH)3、NaCl、H2O 、NaOH 、NaClO、 Na2FeO4。写出并配平化学方程式:_____________________ 。
(4)SO2能使酸性酸性KMnO4溶液褪色,其反应原理是SO2在酸性条件下将 还原为Mn2+,自己转化为
还原为Mn2+,自己转化为 ,写出反应的离子方程式:
,写出反应的离子方程式:___________ 。
(1)反应中被氧化的元素是
(2)写出配平后的方程式:
(3)高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂。其工业合成原理是下列物质间发生氧化还原反应:Fe(OH)3、NaCl、H2O 、NaOH 、NaClO、 Na2FeO4。写出并配平化学方程式:
(4)SO2能使酸性酸性KMnO4溶液褪色,其反应原理是SO2在酸性条件下将
 还原为Mn2+,自己转化为
还原为Mn2+,自己转化为 ,写出反应的离子方程式:
,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是部分短周期元素的信息,用化学用语回答下列问题。
(1)元素A在元素周期表中的位置为________ 。B的某种核素中中子数比质子数多1,则表示该核素的原子符号为_________________ 。
(2)写出钙与M原子个数比为1:2的化合物的电子式______________ 其中含有的化学键类型为__________ (填离子键、极性键或非极性键)。
(3)M2-、D+、G2-离子半径大小顺序是___ > > (用离子符号回答)。
(4)某同学设计实验证明A、B、F的非金属性强弱关系。
①溶液a和b分别为__________ ,_____________ 。
②溶液c中的离子方程式为____________________ 。
(5)将0.5molD2M2投入100mL3mol/LECl3溶液中,转移电子的物质的量为________________ 。
| 元素 | D | M | G | E |
| 性质 结构 信息 | 单质制成的高压 灯,发出的黄光透 雾力强、射程远 | 氢化物常温下呈液 态,M的双原子阴 离子有18个电子 | 原子核外M 层比L层少2 个电子 | +3价阳离子的 核外电子排布 与氖原子相同 |
| 元素代号 | A | B | F |
| 原子半径/nm | 0.077 | 0.075 | 0.117 |
| 主要化合价 | +4、-4 | +5、-3 | +4、4 |
(1)元素A在元素周期表中的位置为
(2)写出钙与M原子个数比为1:2的化合物的电子式
(3)M2-、D+、G2-离子半径大小顺序是
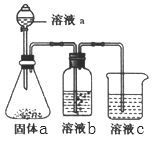
(4)某同学设计实验证明A、B、F的非金属性强弱关系。
①溶液a和b分别为
②溶液c中的离子方程式为
(5)将0.5molD2M2投入100mL3mol/LECl3溶液中,转移电子的物质的量为
您最近一年使用:0次
【推荐3】 是一种可溶性盐,它能被常见的强氧化剂氧化。回答下列问题:
是一种可溶性盐,它能被常见的强氧化剂氧化。回答下列问题:
(1)金属加工后的废液中含有2%~5%的 ,它是一种环境污染物。人们用
,它是一种环境污染物。人们用 溶液来处理此废液,使亚硝酸钠转化为无毒物质。该反应分两步进行:
溶液来处理此废液,使亚硝酸钠转化为无毒物质。该反应分两步进行:
第一步: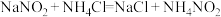
第二步: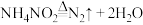
下列对上述反应的叙述中正确的是_______(填字母)。
①两步均为氧化还原反应 ②第二步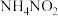 仅发生氧化反应 ③第二步
仅发生氧化反应 ③第二步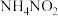 发生了分解反应 ④第二步中
发生了分解反应 ④第二步中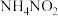 既被氧化又被还原 ⑤第一步为复分解反应
既被氧化又被还原 ⑤第一步为复分解反应
(2)实验室中,亚硝酸钠可用来处理过量的叠氮化钠,有关反应的化学方程式如下:
a.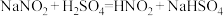
b.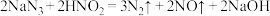
用单线桥法标出b反应中电子转移情况:_______ 。
(3) 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。
①该反应中,被氧化的元素是_______ (填元素符号),氧化剂是_______ (填离子符号)。
②将以上物质分别填入下面对应的横线上,并配平该反应:_______ 。
_______+_______+_______=_______+_______+_______ 。
。
 是一种可溶性盐,它能被常见的强氧化剂氧化。回答下列问题:
是一种可溶性盐,它能被常见的强氧化剂氧化。回答下列问题:(1)金属加工后的废液中含有2%~5%的
 ,它是一种环境污染物。人们用
,它是一种环境污染物。人们用 溶液来处理此废液,使亚硝酸钠转化为无毒物质。该反应分两步进行:
溶液来处理此废液,使亚硝酸钠转化为无毒物质。该反应分两步进行:第一步:
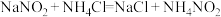
第二步:
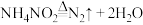
下列对上述反应的叙述中正确的是_______(填字母)。
①两步均为氧化还原反应 ②第二步
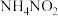 仅发生氧化反应 ③第二步
仅发生氧化反应 ③第二步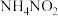 发生了分解反应 ④第二步中
发生了分解反应 ④第二步中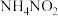 既被氧化又被还原 ⑤第一步为复分解反应
既被氧化又被还原 ⑤第一步为复分解反应| A.①③ | B.①④ | C.②③④ | D.③④⑤ |
a.
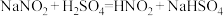
b.
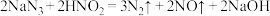
用单线桥法标出b反应中电子转移情况:
(3)
 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。①该反应中,被氧化的元素是
②将以上物质分别填入下面对应的横线上,并配平该反应:
_______+_______+_______=_______+_______+_______
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】配平下面的化学方程式:
___ MnO2+___ HCl(浓)= ___ MnCl2+___ Cl2↑+___ H2O
每当有1molCl2生成,转移电子的物质的量为_______ mol。
每当有1molCl2生成,转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4C1、FeC13、N2、Fe2O3、Fe和X。
(1)根据题意,可判断出X是______ (写化学式)。
(2)写出并配平该反应的化学方程式:______ ;
(3)当转移的电子总数为a个时,氮气物质的量变化了bmol,阿伏加德罗数常数为(用含a、b的代数式表示)______ 。
(4)反应中被氧化产生了11.2L(标准状况)的气体时,被还原的物质的质量为______ 。
(1)根据题意,可判断出X是
(2)写出并配平该反应的化学方程式:
(3)当转移的电子总数为a个时,氮气物质的量变化了bmol,阿伏加德罗数常数为(用含a、b的代数式表示)
(4)反应中被氧化产生了11.2L(标准状况)的气体时,被还原的物质的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】配平下列氧化-还原反应
(1)_______KNO2=_______K2O+_______NO+_______O2;_______ 。
(2)_______P+_______KOH+_______H2O=_______PH3+_______KH2PO2;_______ 。
(3)_______P+_______CuSO4+_______H2O=_______Cu+_______H3PO4+_______H2SO4;_______ 。
(4)_______P+_______CuSO4+_______H2O=_______Cu3P+_______H3PO4+_______H2SO4;_______ 。
(5)_______HClO3+_______P4+_______H2O=_______HCl+_______H3PO4;_______ 。
(6)_______Fe(OH)3+_______NaOH+_______Cl2=_______Na2FeO4+_______NaCl+_______H2O;_______ 。
(7)_______KI+_______H2SO4=_______I2+_______H2S+_______KHSO4+_______H2O;_______ 。
(8)_______PbO2+_______H2SO4=_______PbSO4+_______O2+_______H2O;_______ 。
(9)_______AsH3+_______AgNO3+_______H2O=_______As2O3+_______Ag+_______HNO3;_______ 。
(10)_______NH4ClO4=_______N2↑+_______HCl↑+_______O2↑+_______H2O;_______ 。
(11)_______S+_______KOH=_______K2S+_______K2SO3+_______H2O;_______ 。
(12)_______NO2+_______NaOH=_______NaNO2+_______NaNO3+_______H2O;_______ 。
(1)_______KNO2=_______K2O+_______NO+_______O2;
(2)_______P+_______KOH+_______H2O=_______PH3+_______KH2PO2;
(3)_______P+_______CuSO4+_______H2O=_______Cu+_______H3PO4+_______H2SO4;
(4)_______P+_______CuSO4+_______H2O=_______Cu3P+_______H3PO4+_______H2SO4;
(5)_______HClO3+_______P4+_______H2O=_______HCl+_______H3PO4;
(6)_______Fe(OH)3+_______NaOH+_______Cl2=_______Na2FeO4+_______NaCl+_______H2O;
(7)_______KI+_______H2SO4=_______I2+_______H2S+_______KHSO4+_______H2O;
(8)_______PbO2+_______H2SO4=_______PbSO4+_______O2+_______H2O;
(9)_______AsH3+_______AgNO3+_______H2O=_______As2O3+_______Ag+_______HNO3;
(10)_______NH4ClO4=_______N2↑+_______HCl↑+_______O2↑+_______H2O;
(11)_______S+_______KOH=_______K2S+_______K2SO3+_______H2O;
(12)_______NO2+_______NaOH=_______NaNO2+_______NaNO3+_______H2O;
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】ClO2是一种消毒、杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O
试回答下列问题。
(1)该反应中还原剂的化学式是___ ;
(2)试比较KClO3和CO2的氧化性强弱___ ;
(3)消毒时,ClO2还可以将水中的Mn2+等转化成难溶物MnO2,ClO2被还原成Cl-,写出该反应的离子方程式_________ 。
(4)当转移0.2 mol电子时,生成的ClO2在标准状况下的体积为______ 。
(5)某反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O,写出在碱性条件下,制取FeO42-离子反应方程式_________
试回答下列问题。
(1)该反应中还原剂的化学式是
(2)试比较KClO3和CO2的氧化性强弱
(3)消毒时,ClO2还可以将水中的Mn2+等转化成难溶物MnO2,ClO2被还原成Cl-,写出该反应的离子方程式
(4)当转移0.2 mol电子时,生成的ClO2在标准状况下的体积为
(5)某反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O,写出在碱性条件下,制取FeO42-离子反应方程式
您最近一年使用:0次
【推荐2】实验室用KMnO4和浓HCl来快速制取少量Cl2;产物除了Cl2,还有KCl、MnCl2和H2O。方程式为:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O。
(1)请用双线桥表明上述方程式中电子转移的方向和数目_____ ;
(2)该反应中的浓HCl体现了_____ ;
A.氧化性 B.还原性 C.既有氧化性又有还原性 D.酸性
(3)该反应中的氧化剂是______ ,氧化产物是_______ 。
(4)若要制备标准状况下3.36L的Cl2,则参加反应的KMnO4固体质量为________ g。
(1)请用双线桥表明上述方程式中电子转移的方向和数目
(2)该反应中的浓HCl体现了
A.氧化性 B.还原性 C.既有氧化性又有还原性 D.酸性
(3)该反应中的氧化剂是
(4)若要制备标准状况下3.36L的Cl2,则参加反应的KMnO4固体质量为
您最近一年使用:0次
【推荐1】工业制备硫酸分三步完成:
①FeS2+O2 Fe2O3+SO2(未配平,FeS2是二硫化亚铁)
Fe2O3+SO2(未配平,FeS2是二硫化亚铁)
②2SO2+O2 2SO3
2SO3
③SO3+H2O=H2SO4
(1)配平反应①:__ 。
(2)三步反应中,属于氧化还原反应的是__ (填序号)。
(3)反应①中,氧化产物是__ 。
(4)反应①中,有32gO2参加反应时,被氧化的铁元素的质量是__ g。
①FeS2+O2
 Fe2O3+SO2(未配平,FeS2是二硫化亚铁)
Fe2O3+SO2(未配平,FeS2是二硫化亚铁)②2SO2+O2
 2SO3
2SO3③SO3+H2O=H2SO4
(1)配平反应①:
(2)三步反应中,属于氧化还原反应的是
(3)反应①中,氧化产物是
(4)反应①中,有32gO2参加反应时,被氧化的铁元素的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】油画中使用的无机颜料雄黄(As2S3)在不同空气湿度和光照条件下会发生褪色,主要发生以下两种化学反应:

(1)紫外光照射下,被氧化的元素是___________ (填元素符号),每生成 ,转移电子的物质的量为
,转移电子的物质的量为___________ mol。
(2)自然光照射下发生反应的化学方程式:___________ 。
(3)氧化等量 时,紫外光与自然光照射下消耗
时,紫外光与自然光照射下消耗 的物质的量之比为
的物质的量之比为___________ 。
(4) 和
和 按物质的量之比为2:1混合后加热,向溶液中通入
按物质的量之比为2:1混合后加热,向溶液中通入 即可获得
即可获得 和
和 ,该反应的离子方程式:
,该反应的离子方程式:___________ 。上述过程一般在碱性环境下进行,若在酸性条件下由于生成副产物___________ 导致产品会发黄。
(5)芯片制造工业中利用 与
与 反应,将As氧化为+5价,该反应的氧化剂与还原剂物质的量之比为
反应,将As氧化为+5价,该反应的氧化剂与还原剂物质的量之比为___________ 。

(1)紫外光照射下,被氧化的元素是
 ,转移电子的物质的量为
,转移电子的物质的量为(2)自然光照射下发生反应的化学方程式:
(3)氧化等量
 时,紫外光与自然光照射下消耗
时,紫外光与自然光照射下消耗 的物质的量之比为
的物质的量之比为(4)
 和
和 按物质的量之比为2:1混合后加热,向溶液中通入
按物质的量之比为2:1混合后加热,向溶液中通入 即可获得
即可获得 和
和 ,该反应的离子方程式:
,该反应的离子方程式:(5)芯片制造工业中利用
 与
与 反应,将As氧化为+5价,该反应的氧化剂与还原剂物质的量之比为
反应,将As氧化为+5价,该反应的氧化剂与还原剂物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学研究中应当学会实验与探究、归纳与演绎、分析与综合等方法的运用。回答下列问题:
I.现有下列10种物质:
①冰水混合物 ②有色玻璃 ③ ④
④ ⑤熔融
⑤熔融 ⑥
⑥ 溶液 ⑦
溶液 ⑦ ⑧硫酸溶液 ⑨
⑧硫酸溶液 ⑨ ⑩固体
⑩固体 。
。
(1)属于分散系的是___________ ,属于强电解质且能导电的是___________ ,属于非电解质的是___________ 。
(2)向⑥溶液中滴加用⑩物质配制的溶液,至 恰好完全沉淀时的离子方程式:
恰好完全沉淀时的离子方程式:___________ 。
Ⅱ.完成下列问题
(3) 溶液能用作
溶液能用作 中毒的解毒剂反应可生成P的最高价含氧酸和铜;该反应的化学方程式是
中毒的解毒剂反应可生成P的最高价含氧酸和铜;该反应的化学方程式是___________ 。
(4)汽车剧烈碰撞时,安全气囊中发生反应: 。该反应中氧化产物与还原产物的质量比为
。该反应中氧化产物与还原产物的质量比为___________ ;若氧化产物比还原产物多 ,则反应生成的
,则反应生成的 在标准状况下的体积为
在标准状况下的体积为___________ L。
I.现有下列10种物质:
①冰水混合物 ②有色玻璃 ③
 ④
④ ⑤熔融
⑤熔融 ⑥
⑥ 溶液 ⑦
溶液 ⑦ ⑧硫酸溶液 ⑨
⑧硫酸溶液 ⑨ ⑩固体
⑩固体 。
。(1)属于分散系的是
(2)向⑥溶液中滴加用⑩物质配制的溶液,至
 恰好完全沉淀时的离子方程式:
恰好完全沉淀时的离子方程式:Ⅱ.完成下列问题
(3)
 溶液能用作
溶液能用作 中毒的解毒剂反应可生成P的最高价含氧酸和铜;该反应的化学方程式是
中毒的解毒剂反应可生成P的最高价含氧酸和铜;该反应的化学方程式是(4)汽车剧烈碰撞时,安全气囊中发生反应:
 。该反应中氧化产物与还原产物的质量比为
。该反应中氧化产物与还原产物的质量比为 ,则反应生成的
,则反应生成的 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次




