氯乙酸( )是重要的有机化工原料,实验室中先用
)是重要的有机化工原料,实验室中先用 和浓盐酸制备干燥、纯净的
和浓盐酸制备干燥、纯净的 ,然后将
,然后将 通入冰醋酸中生成氯乙酸。回答下列问题:
通入冰醋酸中生成氯乙酸。回答下列问题:
(1)基态Mn原子的价层电子排布图为___________ ,I 1(Mn) ___________ I 1(K) (填“大于”或“小于”)。
(2)氯乙酸的组成元素电负性由大到小的顺序为___________ ;其分子中碳原子的杂化方式为___________
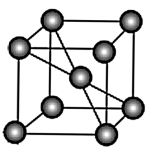
(3) 中两种金属元素单质的晶体结构堆积方式相同,晶胞结构如下图所示。
中两种金属元素单质的晶体结构堆积方式相同,晶胞结构如下图所示。 为阿伏加德罗常数的值。锰的摩尔质量为
为阿伏加德罗常数的值。锰的摩尔质量为 ,晶胞的密度为
,晶胞的密度为 ,则锰的晶胞参数为
,则锰的晶胞参数为___________  (用含
(用含 、
、 、
、 的式子表示)。
的式子表示)。
 )是重要的有机化工原料,实验室中先用
)是重要的有机化工原料,实验室中先用 和浓盐酸制备干燥、纯净的
和浓盐酸制备干燥、纯净的 ,然后将
,然后将 通入冰醋酸中生成氯乙酸。回答下列问题:
通入冰醋酸中生成氯乙酸。回答下列问题:(1)基态Mn原子的价层电子排布图为
(2)氯乙酸的组成元素电负性由大到小的顺序为
(3)
 中两种金属元素单质的晶体结构堆积方式相同,晶胞结构如下图所示。
中两种金属元素单质的晶体结构堆积方式相同,晶胞结构如下图所示。 为阿伏加德罗常数的值。锰的摩尔质量为
为阿伏加德罗常数的值。锰的摩尔质量为 ,晶胞的密度为
,晶胞的密度为 ,则锰的晶胞参数为
,则锰的晶胞参数为 (用含
(用含 、
、 、
、 的式子表示)。
的式子表示)。
更新时间:2021-10-22 11:29:38
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】镁铝尖晶石作为一种有前途的绿色环保型无机功能材料,向其中参入Cr、Mn、Ti等过渡元素,可使镁铝尖晶石发光材料实现发光颜色的转变和发光效率的提高,适应其在发光二极管、显示器及固态照明等领域的应用。
(1)钛元素属于元素周期表_______ 区,基态钛原子核外有_______ 种运动状态不同的电子。下列Al原子的核外电子排布式中,能量最低的是_______ (填字母)。
a.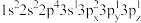 b.
b.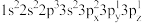
c.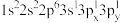 d.
d.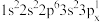
(2)镁铝尖晶石由Mg、Al、O元素组成,按第一电离能由大到小的排列顺序为_______ 。
(3)一种烷基铝配合物的结构如图,该物质中碳的杂化类型为_______ ,氮与其成键的3原子共同构成的空间构型为_______ ,氮与铝形成的是_______ 键(填编号,双选)
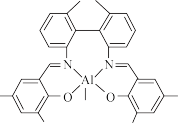
a.配位键 b.金属键 d.σ键 d.π键
(4)氯化铬(CrCl3)熔点为83℃,氯化镍(NiCl2)的熔点为1001℃,氯化铬的熔点远低于氯化镍的熔点,原因是_______ 。
(5)某种镁铝尖晶石的立方晶胞结构如图所示,晶胞中含有A型和B型两种结构单元。

与O2-最邻近的Al3+离子数为_______ ,若晶胞边长为apm,阿伏加德罗常数为NA,则该尖晶石的密度为_______ g/cm3(用含a、NA的代数式表示)。
(1)钛元素属于元素周期表
a.
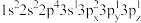 b.
b.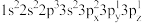
c.
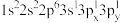 d.
d.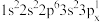
(2)镁铝尖晶石由Mg、Al、O元素组成,按第一电离能由大到小的排列顺序为
(3)一种烷基铝配合物的结构如图,该物质中碳的杂化类型为

a.配位键 b.金属键 d.σ键 d.π键
(4)氯化铬(CrCl3)熔点为83℃,氯化镍(NiCl2)的熔点为1001℃,氯化铬的熔点远低于氯化镍的熔点,原因是
(5)某种镁铝尖晶石的立方晶胞结构如图所示,晶胞中含有A型和B型两种结构单元。

与O2-最邻近的Al3+离子数为
您最近一年使用:0次
【推荐2】人类文明的发展历程,也是化学物质的认识和发现的历程。
(1)铜原子在基态时价电子(外围电子)排布式为_______ 。已知高温下Cu2O比CuO更稳定,试从核外电子排布的角度解释:_______ 。
(2)铜与类卤素(SCN)2反应生成Cu(SCN)2,类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H-S-C≡N)的沸点低于异硫氰酸(H-N=C=S)的沸点,其原因是_______ 。每个硫氰酸(H-S-C≡N)分子中都包含_______ 个σ键,_______ 个π键。
(3)BF3与一定量的水可形成如图所示晶体R晶体R中各种微粒间的作用力涉及_______ (填字母代号),
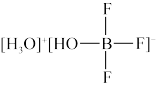
a.离子键 b.共价键 c.配位键 d.金属键 e.范德华力
(4)C、N、O元素原子的第一电离能由大到小的顺序为_______ ;已知第三电离能数据: ,
,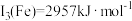 ,锰的第三电离能大于铁的第三电离能,其主要原因是
,锰的第三电离能大于铁的第三电离能,其主要原因是_______ 。
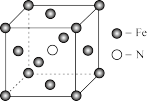
(5)铁和氨在640℃可发生置换反应,产物之一的立方晶胞结构如图所示,写出该反应的化学方程式:_______ 。
(1)铜原子在基态时价电子(外围电子)排布式为
(2)铜与类卤素(SCN)2反应生成Cu(SCN)2,类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H-S-C≡N)的沸点低于异硫氰酸(H-N=C=S)的沸点,其原因是
(3)BF3与一定量的水可形成如图所示晶体R晶体R中各种微粒间的作用力涉及

a.离子键 b.共价键 c.配位键 d.金属键 e.范德华力
(4)C、N、O元素原子的第一电离能由大到小的顺序为
 ,
,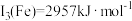 ,锰的第三电离能大于铁的第三电离能,其主要原因是
,锰的第三电离能大于铁的第三电离能,其主要原因是(5)铁和氨在640℃可发生置换反应,产物之一的立方晶胞结构如图所示,写出该反应的化学方程式:

您最近一年使用:0次
【推荐3】短周期的7种元素A、B、C、D、E、F、G的原子序数依次增大,其中A原子中的电子只有1种运动状态,且与B同主族,C的基态原子2p能级上只有1个电子,F与A可形成两种常温下的液态化合物;F与G同主族。根据上述描述,请回答下列问题:
(1)上述7种元素中电负性最小的元素与A元素形成的化合物的电子式为______ (用具体元素符号表示电子式),基态原子的一电离能最大的元素是_____ (填元素符号)。
(2)1molD3A6链状分子中含有的σ键数为________ 。
(3)已知A2F2的分子结构如图所示:
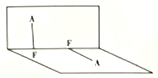
①用电离方程式表示呈弱酸性的原因:______________ 。
②A2F2的沸点比A2F高的原因:_______________ 。
(1)上述7种元素中电负性最小的元素与A元素形成的化合物的电子式为
(2)1molD3A6链状分子中含有的σ键数为
(3)已知A2F2的分子结构如图所示:

①用电离方程式表示呈弱酸性的原因:
②A2F2的沸点比A2F高的原因:
您最近一年使用:0次
【推荐1】前四周期原子序数依次增大的元素a、b、c、d中,a和b的价电子层中未成对电子均只有1个。并且a—和b+的电子数相差8;c和d与b位于同一周期,c和d的价电子层中的未成对电子数分别为4和2,且原子序数相差2。回答下列问题:
(1)a元素在元素周期表中的位置是___________ ,属于___________ 区。
(2)基态b原子中。电子占据最高能层的符号是___________ , 基态b+占据的最高能级共有___________ 个原子轨道。
(3)d元素基态原子的简化电子排布式为___________ 。
(4)a、b、c、d四种元素中,电负性最大的为___________ (填元素符号)。
(5)a、b、d三种元素的第一电离能由大到小的顺序为___________ (填元素符号)。
(6)Mn和c两种元素的部分电离能数据如表所示:
比较两元素的I2、 I3可知,气态Mn2+再失去一个电子比气态c2+再失去一个电子更难,原因是___________ 。
(1)a元素在元素周期表中的位置是
(2)基态b原子中。电子占据最高能层的符号是
(3)d元素基态原子的简化电子排布式为
(4)a、b、c、d四种元素中,电负性最大的为
(5)a、b、d三种元素的第一电离能由大到小的顺序为
(6)Mn和c两种元素的部分电离能数据如表所示:
| 元素 | 电离能/(kJ·mol-1) | ||
| I1 | I2 | I3 | |
| c元素 | 759 | 1561 | 2957 |
| Mn元素 | 717 | 1509 | 3248 |
比较两元素的I2、 I3可知,气态Mn2+再失去一个电子比气态c2+再失去一个电子更难,原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】碳和硅是同主族元素,但是 和
和 的性质和应用却有着很大差异。
的性质和应用却有着很大差异。
(1)原子结构与元素性质分析
①基态碳原子占据的最高能级的原子轨道的形状是___________ (填名称)。
②基态 的价层电子轨道表示式是:
的价层电子轨道表示式是:___________
③元素C、Si、O的电负性由大到小的关系是___________
(2)微粒间相互作用与物质性质
① 和
和 中同时存在
中同时存在 键和
键和 键的是
键的是___________ (填化学式)。
② 分子的空间结构是
分子的空间结构是___________ ,碳原子的杂化轨道类型为___________ ﹔
③ 晶体结构如下图所示,硅原子的杂化轨道类型为
晶体结构如下图所示,硅原子的杂化轨道类型为___________ 。

(3)不同聚集状态的物质与性质
①Si与C同主族,但 与
与 的熔沸点等物理性质差距很大,请从晶体结构角度解释其原因
的熔沸点等物理性质差距很大,请从晶体结构角度解释其原因___________ 。
②干冰晶体结构如上图所示,下列关于 与
与 叙述正确的是
叙述正确的是___________ 。
a.固体 一定是晶体
一定是晶体
b.干冰晶体中,每个 周围紧邻12个
周围紧邻12个
c. 晶胞中,含有Si原子8个和O原子16个
晶胞中,含有Si原子8个和O原子16个
③某种含硅化合物晶胞结构如下图所示,这种含硅化合物的化学式为___________ 。
④已知该化合物的晶胞边长为acm,阿伏伽德罗常数的值为 ,则其晶体的密度为
,则其晶体的密度为___________  。
。

 和
和 的性质和应用却有着很大差异。
的性质和应用却有着很大差异。(1)原子结构与元素性质分析
①基态碳原子占据的最高能级的原子轨道的形状是
②基态
 的价层电子轨道表示式是:
的价层电子轨道表示式是:③元素C、Si、O的电负性由大到小的关系是
(2)微粒间相互作用与物质性质
①
 和
和 中同时存在
中同时存在 键和
键和 键的是
键的是②
 分子的空间结构是
分子的空间结构是③
 晶体结构如下图所示,硅原子的杂化轨道类型为
晶体结构如下图所示,硅原子的杂化轨道类型为
(3)不同聚集状态的物质与性质
①Si与C同主族,但
 与
与 的熔沸点等物理性质差距很大,请从晶体结构角度解释其原因
的熔沸点等物理性质差距很大,请从晶体结构角度解释其原因②干冰晶体结构如上图所示,下列关于
 与
与 叙述正确的是
叙述正确的是a.固体
 一定是晶体
一定是晶体b.干冰晶体中,每个
 周围紧邻12个
周围紧邻12个
c.
 晶胞中,含有Si原子8个和O原子16个
晶胞中,含有Si原子8个和O原子16个③某种含硅化合物晶胞结构如下图所示,这种含硅化合物的化学式为
④已知该化合物的晶胞边长为acm,阿伏伽德罗常数的值为
 ,则其晶体的密度为
,则其晶体的密度为 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】表中列出了第三周期的几种元素的部分性质:
请按要求回答下列问题:
(1)写出基态 原子的价层电子轨道表示式:
原子的价层电子轨道表示式:___________ 。
(2)表中元素原子半径最大的是(写元素符号)___________ 。预测 值的区间
值的区间___________ 。
(3) 、
、 、
、 三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)
三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)___________ 。
(4)d、e最高价氧化物对应水化物相互反应的离子方程式为___________ 。
(5)上表中五种元素的第一电离能由大到小的顺序是(写元素符号)___________ 。
(6)某化学兴趣小组为探究元素性质的递变规律,设计了以下系列实验。
①甲同学为探究同主族元素金属性的递变规律,取绿豆粒大小的钠、钾分别放入到盛有 水的烧杯(滴有几滴酚酞溶液)中,通过观察现象得出的结论是
水的烧杯(滴有几滴酚酞溶液)中,通过观察现象得出的结论是___________ 。
②乙同学利用现有药品: 溶液、
溶液、 固体、浓盐酸、
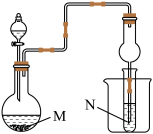
固体、浓盐酸、 ,设计如图装置探究第三周期部分元素非金属性的递变规律。
,设计如图装置探究第三周期部分元素非金属性的递变规律。 中所装药品为
中所装药品为___________ ,装置 中的实验现象为有淡黄色沉淀生成,离子方程式为
中的实验现象为有淡黄色沉淀生成,离子方程式为___________ ;所得结论为___________ 。
| 元素编号 |  |  |  |  |  |
| 电负性 | 3.0 | 2.5 |  | 1.5 | 0.9 |
| 主要化合价 | -1,+7 | -2,+6 | -3,+5 | +3 | +1 |
(1)写出基态
 原子的价层电子轨道表示式:
原子的价层电子轨道表示式:(2)表中元素原子半径最大的是(写元素符号)
 值的区间
值的区间(3)
 、
、 、
、 三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)
三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)(4)d、e最高价氧化物对应水化物相互反应的离子方程式为
(5)上表中五种元素的第一电离能由大到小的顺序是(写元素符号)
(6)某化学兴趣小组为探究元素性质的递变规律,设计了以下系列实验。
①甲同学为探究同主族元素金属性的递变规律,取绿豆粒大小的钠、钾分别放入到盛有
 水的烧杯(滴有几滴酚酞溶液)中,通过观察现象得出的结论是
水的烧杯(滴有几滴酚酞溶液)中,通过观察现象得出的结论是②乙同学利用现有药品:
 溶液、
溶液、 固体、浓盐酸、
固体、浓盐酸、 ,设计如图装置探究第三周期部分元素非金属性的递变规律。
,设计如图装置探究第三周期部分元素非金属性的递变规律。 中所装药品为
中所装药品为 中的实验现象为有淡黄色沉淀生成,离子方程式为
中的实验现象为有淡黄色沉淀生成,离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的EMIM+由H、C、N三种元素组成,结构如下图所示。回答下列问题:

(1)碳原子价层电子的轨道表达式为______ ,基态碳原子中,核外电子占据的最高能级的电子云轮廓图为______ 形。
(2)根据价层电子对互斥理论,NH3、 、
、 中,中心原子价层电子对数不同于其他两种粒子的是
中,中心原子价层电子对数不同于其他两种粒子的是_______ 。NH3比PH3的沸点高,原因是____________ 。
(3)氮元素的第一电离能比同周期相邻元素都大的原因是____________ 。
(4)EMIM+中,碳原子的杂化轨道类型为________ 。分子中的大π键可用符号 表示,其中n代表参与形成的大π键原子数,m代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中n代表参与形成的大π键原子数,m代表参与形成的大π键电子数(如苯分子中的大π键可表示为 ),则EMIM+中的大π键应表示为
),则EMIM+中的大π键应表示为________ 。
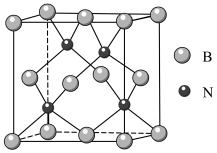
(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如下图所示。立方氮化硼属于______ 晶体,其中硼原子的配位数为_____ 。已知:立方氮化硼密度为d g/cm3,B原子半径为x pm,N原子半径为y pm,阿伏加 德罗常数的值为NA,则该晶胞中原子的空间利用率为_______ (列出化简后的计算式)。

(1)碳原子价层电子的轨道表达式为
(2)根据价层电子对互斥理论,NH3、
 、
、 中,中心原子价层电子对数不同于其他两种粒子的是
中,中心原子价层电子对数不同于其他两种粒子的是(3)氮元素的第一电离能比同周期相邻元素都大的原因是
(4)EMIM+中,碳原子的杂化轨道类型为
 表示,其中n代表参与形成的大π键原子数,m代表参与形成的大π键电子数(如苯分子中的大π键可表示为
表示,其中n代表参与形成的大π键原子数,m代表参与形成的大π键电子数(如苯分子中的大π键可表示为 ),则EMIM+中的大π键应表示为
),则EMIM+中的大π键应表示为(5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如下图所示。立方氮化硼属于

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】Ⅰ.钒( )泛应用于催化及钢铁工业,有“化学面包”“金属维生素”之称。
)泛应用于催化及钢铁工业,有“化学面包”“金属维生素”之称。
(1)基态钒原子的价电子排布式为___________ ;与钒同周期的所有元素的基态原子中,未成对电子数最多的是___________ (填元素符号)。
Ⅱ. 为两性氧化物。
为两性氧化物。 溶解在稀硫酸中时,生成强氧化性的
溶解在稀硫酸中时,生成强氧化性的 ;
; 溶解在NaOH溶液中时,可得到
溶解在NaOH溶液中时,可得到 ,其空间构型与
,其空间构型与 相同。
相同。
(2)写出稀硫酸溶解 的化学方程式:
的化学方程式:___________ 。
(3) 中心原子价层孤电子对数目为___________。
中心原子价层孤电子对数目为___________。
(4)在碱性环境中,溶液中 与
与 可以相互转化。
可以相互转化。
① 转化为
转化为 的离子方程式为:
的离子方程式为:___________ 。
②室温下,当 时,1.0 mol⋅L-1
时,1.0 mol⋅L-1 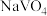 溶液中
溶液中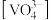 为0.10 mol⋅L-1。可知上述转化反应的平衡常数数值为
为0.10 mol⋅L-1。可知上述转化反应的平衡常数数值为___________ 。
Ⅲ.用活化后的 作催化剂,在有氧条件下氨气将NO还原成
作催化剂,在有氧条件下氨气将NO还原成 的一种反应历程如图所示。
的一种反应历程如图所示。
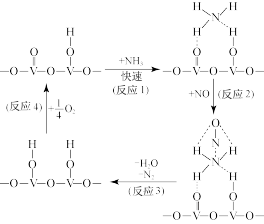
(5)上述历程中,钒元素被氧化的过程是反应___________ (填序号);写出总反应的化学方程式:___________ 。
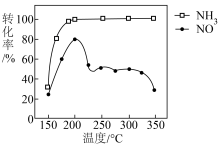
(6)按上述图中 、NO和
、NO和 的比例进行催化脱硝反应。反应一定的时间,
的比例进行催化脱硝反应。反应一定的时间, 和NO的转化率与温度的关系如图所示。超过200℃后,NO转化率急剧下降,而
和NO的转化率与温度的关系如图所示。超过200℃后,NO转化率急剧下降,而 仍维持较高,原因可能是:
仍维持较高,原因可能是:___________ 。
 )泛应用于催化及钢铁工业,有“化学面包”“金属维生素”之称。
)泛应用于催化及钢铁工业,有“化学面包”“金属维生素”之称。(1)基态钒原子的价电子排布式为
Ⅱ.
 为两性氧化物。
为两性氧化物。 溶解在稀硫酸中时,生成强氧化性的
溶解在稀硫酸中时,生成强氧化性的 ;
; 溶解在NaOH溶液中时,可得到
溶解在NaOH溶液中时,可得到 ,其空间构型与
,其空间构型与 相同。
相同。(2)写出稀硫酸溶解
 的化学方程式:
的化学方程式:(3)
 中心原子价层孤电子对数目为___________。
中心原子价层孤电子对数目为___________。| A.0 | B.1 | C.2 | D.3 |
(4)在碱性环境中,溶液中
 与
与 可以相互转化。
可以相互转化。①
 转化为
转化为 的离子方程式为:
的离子方程式为:②室温下,当
 时,1.0 mol⋅L-1
时,1.0 mol⋅L-1 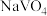 溶液中
溶液中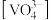 为0.10 mol⋅L-1。可知上述转化反应的平衡常数数值为
为0.10 mol⋅L-1。可知上述转化反应的平衡常数数值为Ⅲ.用活化后的
 作催化剂,在有氧条件下氨气将NO还原成
作催化剂,在有氧条件下氨气将NO还原成 的一种反应历程如图所示。
的一种反应历程如图所示。
(5)上述历程中,钒元素被氧化的过程是反应
(6)按上述图中
 、NO和
、NO和 的比例进行催化脱硝反应。反应一定的时间,
的比例进行催化脱硝反应。反应一定的时间, 和NO的转化率与温度的关系如图所示。超过200℃后,NO转化率急剧下降,而
和NO的转化率与温度的关系如图所示。超过200℃后,NO转化率急剧下降,而 仍维持较高,原因可能是:
仍维持较高,原因可能是:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】电石(CaC2)是一种用于生产乙炔的浅色固体。它是由氧化钙与焦炭反应形成的:CaO+3C CaC2+CO。德国化学家维勒发现,电石与水反应释放出乙炔气体(C2H2)和氢氧化钙,也含有H2S、PH3等杂质气体。
CaC2+CO。德国化学家维勒发现,电石与水反应释放出乙炔气体(C2H2)和氢氧化钙,也含有H2S、PH3等杂质气体。
回答下列问题:
(1)上述六种元素中,电负性最大的是___________ (填写元素名称),原子半径最大者在基态时核外电子占据的轨道数目为___________ 个。
(2)H2S、PH3分子中心原子的价层电子对数目___________ (填“相同”或“不同”)。根据等电子原理,画出C 离子的电子式
离子的电子式___________ ,乙炔分子中C原子的杂化方式为___________ 。
(3)已知键能数据如下表:
请解释CO比N2容易发生反应:___________ 。
(4)如图为电石的四方晶胞(长方体),钙离子位于___________ ,它填入C 离子围成的八面体空隙。计算一个晶胞内含有化学式的数量为
离子围成的八面体空隙。计算一个晶胞内含有化学式的数量为___________ 。
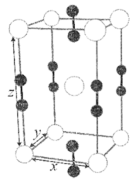
(5)已知电石密度为2.13 g·cm-3,阿伏加德罗常数为6.02×1023 mol-1,x、y值均为a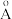 (1
(1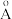 =10-10m),则z=
=10-10m),则z=___________ nm(用含a的式子表示,且数字保留整数)。已知a<4.0,则距离钙最近的C 中心有
中心有___________ 个。
 CaC2+CO。德国化学家维勒发现,电石与水反应释放出乙炔气体(C2H2)和氢氧化钙,也含有H2S、PH3等杂质气体。
CaC2+CO。德国化学家维勒发现,电石与水反应释放出乙炔气体(C2H2)和氢氧化钙,也含有H2S、PH3等杂质气体。回答下列问题:
(1)上述六种元素中,电负性最大的是
(2)H2S、PH3分子中心原子的价层电子对数目
 离子的电子式
离子的电子式(3)已知键能数据如下表:
| 化学键 | N-N | N= N | N=N |
| 键能/kJ.mol-1 | 247 | 418 | 942 |
| 化学键 | C-O | C=O | C=O |
| 键能/kJ. mol-1 | 351 | 745 | 1072 |
(4)如图为电石的四方晶胞(长方体),钙离子位于
 离子围成的八面体空隙。计算一个晶胞内含有化学式的数量为
离子围成的八面体空隙。计算一个晶胞内含有化学式的数量为
(5)已知电石密度为2.13 g·cm-3,阿伏加德罗常数为6.02×1023 mol-1,x、y值均为a
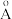 (1
(1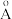 =10-10m),则z=
=10-10m),则z= 中心有
中心有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】A、M、B、C、D、E、F、N、G、H是前4周期常见元素,原子序数依次增大。A原子是周期表中半径最小的原子;B的基态原子最外层有3个未成对电子;C原子的2p轨道上有1个电子的自旋方向与其它电子相反;D的价层电子排布式为ns1,E和C形成的化合物是引起酸雨的主要大气污染物;G的+3价离子的3d轨道为半充满状态,H元素的原子M层全充满且只有一个单电子。
(1)D、C、E分别形成的简单离子的半径由大到小顺序为_______ (填离子符号)
(2)F同周期元素中,第一电离能最大的是_______ (写元素符号)。
(3)H与F形成的一种化合物的立方晶胞如图所示。
①该化合物的化学式为_______ ,H位于F围成的_______ 空隙中。

②若该化合物密度为4.4 g·cm-3,则最近的F和H之间的距离为_______ pm。(阿伏加德罗常数NA)
(4)G(MC)5常温下是一种浅黄色液体,熔点-20℃,不溶于水、易溶于苯。
①1 mol G(MC)5中所含σ键的数目为_______ NA。
②G(MC)5分子的结构可能为下图中的_______ (填“甲”或“乙”)。

(5)由M、B、G、N元素形成的一种蓝色晶体,其晶体结构如图丙所示(图中N+未画出)。该蓝色晶体的化学式为_______ 。

(1)D、C、E分别形成的简单离子的半径由大到小顺序为
(2)F同周期元素中,第一电离能最大的是
(3)H与F形成的一种化合物的立方晶胞如图所示。
①该化合物的化学式为

②若该化合物密度为4.4 g·cm-3,则最近的F和H之间的距离为
(4)G(MC)5常温下是一种浅黄色液体,熔点-20℃,不溶于水、易溶于苯。
①1 mol G(MC)5中所含σ键的数目为
②G(MC)5分子的结构可能为下图中的

(5)由M、B、G、N元素形成的一种蓝色晶体,其晶体结构如图丙所示(图中N+未画出)。该蓝色晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】 、
、 在电化学和催化领域均有重要地位.回答下列问题:
在电化学和催化领域均有重要地位.回答下列问题:
(1)基态 原子核外占据最高能层电子的电子云轮廓图的形状为
原子核外占据最高能层电子的电子云轮廓图的形状为_______ ; 、
、 两种基态原子的价层电子数目之比为
两种基态原子的价层电子数目之比为_______ ; 、
、 、
、 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为_______ 。
(2)碳有多种同素异形体,其中等质量的石墨与金刚石中共价键的数目之比为_______ 。
(3) 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为_______ ,原因为_______ 。
(4) 的酸性弱于
的酸性弱于 的原因为
的原因为_______ ; 中
中 的杂化方式为
的杂化方式为_______ 。
(5) 的晶胞结构如图所示。
的晶胞结构如图所示。

① 晶体中,C周围距离最近且相等的
晶体中,C周围距离最近且相等的 的数目为
的数目为_______ 。
②若阿伏加德罗常数的值为 ,则
,则 晶体密度
晶体密度
_______  。
。
 、
、 在电化学和催化领域均有重要地位.回答下列问题:
在电化学和催化领域均有重要地位.回答下列问题:(1)基态
 原子核外占据最高能层电子的电子云轮廓图的形状为
原子核外占据最高能层电子的电子云轮廓图的形状为 、
、 两种基态原子的价层电子数目之比为
两种基态原子的价层电子数目之比为 、
、 、
、 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为(2)碳有多种同素异形体,其中等质量的石墨与金刚石中共价键的数目之比为
(3)
 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为(4)
 的酸性弱于
的酸性弱于 的原因为
的原因为 中
中 的杂化方式为
的杂化方式为(5)
 的晶胞结构如图所示。
的晶胞结构如图所示。
①
 晶体中,C周围距离最近且相等的
晶体中,C周围距离最近且相等的 的数目为
的数目为②若阿伏加德罗常数的值为
 ,则
,则 晶体密度
晶体密度
 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】金属及其化合物在科学研究和工业生产中具有重要的用途。
(1)三氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:

①此配合物中,铁离子价电子排布图为_______________ ;
②此配离子中碳原子的杂化轨道类型为_________________ ;
③此配离子中含有的化学键为_______________ 。
A 离子键 B 金属键 C 极性键 D 非极性键 E 配位键 F 氢键 G σ键 H π键
(2)NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验K+的存在。NO2-离子的VSEPR模型名称为_____ ,K3[Co(NO2)6]是黄色沉淀,该物质中四种元素的电负性由大到小的顺序是_________ 。
(3)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2,其中适合作录音带磁粉原料的是_____ 。
(4)锰的一种配合物的化学式为Mn(BH4)2(THF)3,写出两种与BH4-互为等电子体的微粒____ (请写一个分子和一个离子)。
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶体的结构如图所示,a的配位数为_____ ,已知晶胞密度为ρ g/cm3,则晶包的棱长为_____ nm(NA表示阿伏伽德罗常数)。

(1)三氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:

①此配合物中,铁离子价电子排布图为
②此配离子中碳原子的杂化轨道类型为
③此配离子中含有的化学键为
A 离子键 B 金属键 C 极性键 D 非极性键 E 配位键 F 氢键 G σ键 H π键
(2)NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验K+的存在。NO2-离子的VSEPR模型名称为
(3)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2,其中适合作录音带磁粉原料的是
(4)锰的一种配合物的化学式为Mn(BH4)2(THF)3,写出两种与BH4-互为等电子体的微粒
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶体的结构如图所示,a的配位数为

您最近一年使用:0次



