在1100℃,一定容积的密闭容器中发生反应: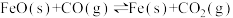
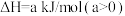 ,该温度下
,该温度下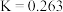 ,下列有关该反应的说法正确的是
,下列有关该反应的说法正确的是
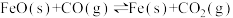
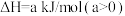 ,该温度下
,该温度下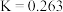 ,下列有关该反应的说法正确的是
,下列有关该反应的说法正确的是| A.若生成1 mol Fe,则吸收的热量小于a kJ |
| B.相同温度,若容器内FeO、CO、Fe、CO2四种物质物质的量分别为5.0 mol、1.2 mol、1.5 mol、1.0 mol,则此时上述反应的平衡向正反应方向移动 |
| C.若升高温度,则正反应速率加快,逆反应速率加快,化学平衡逆向移动 |
D.达到化学平衡状态时,若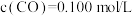 ,则 ,则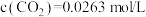 |
更新时间:2021-11-08 21:09:19
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:

下列说法正确的是

下列说法正确的是
| A.使用催化剂,反应的ΔH变小 | B.在该过程中,CO断键形成C和O |
| C.CO和O生成了具有极性共价键的CO2 | D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关反应热叙述正确的是
| A.化学反应的反应热与反应过程有密切的关系 |
| B.CO(g)燃烧热△H=-283.0kJ/mol,则 2CO2(g)=2CO(g)+O2(g)反应的△H=+566.0kJ/mol |
| C.若反应断键吸收能量大于成键放出的能量,则该反应的反应热△H<0 |
| D.1mol 甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列反应条件的改变对 反应速率的影响正确的是
反应速率的影响正确的是
 反应速率的影响正确的是
反应速率的影响正确的是A.增大 的浓度能加快反应速率 的浓度能加快反应速率 | B.减小HCl的浓度能加快反应速率 |
| C.升高温度能减慢反应速率 | D.及时将生成的Si移出可加快反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列图示与对应叙述相符的是
A.如图:常温下,0.1 mol ·L-1盐酸稀释时pH随加入水的体积变化 |
B.如图:铅蓄电池放电时,正极附近溶液的pH随时间的变化 |
C.如图:不同压强下,可逆反应A(g)+B(g) C(g)+D(s)中A的浓度随时间的变化 C(g)+D(s)中A的浓度随时间的变化 |
D.如图:镁条放入足量2 mol ·L-1盐酸中,生成氢气速率随时间的变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知:Na2S2O3+H2SO4=S↓+SO2↑+H2O+Na2SO4,通过析出硫的快慢可以说明反应速率的大小,请判断下列几种情况下,最先看到硫析出的是
选项 | 温度 | Na2S2O3溶液的体积和物质的量浓度 | H2SO4的体积和物质的量浓度 |
A | 20℃ | 15mL0.1mol·L-1 | 15mL0.1mol·L-1 |
B | 20℃ | 10mL0.2mol·L-1 | 10mL0.2mol·L-1 |
C | 50℃ | 50mL0.1mol·L-1 | 50mL0.1mol·L-1 |
D | 50℃ | 5mL0.5mol·L-1 | 5mL0.5mol·L-1 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关说法正确的是
| A.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
| B.等物质的量浓度的CH3COOH溶液和HCl溶液中,水的电离程度相同 |
| C.0.1 mol/LNa2CO3溶液:c(OH-)=c(H2CO3)+c(HCO3-)+c(H+) |
D.对于反应2SO2+O2  2SO3,使用催化剂能加快反应速率和提高SO2平衡转化率 2SO3,使用催化剂能加快反应速率和提高SO2平衡转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列事实不能用勒夏特列原理(化学平衡移动原理)解释的是
| A.合成氨时,选定温度为400~500℃,而不是常温 |
| B.人体血液的pH稳定在7.4±0.05范围内 |
| C.氯气在水中的溶解度大于在饱和食盐水中的溶解度 |
| D.生活中,可用热的纯碱溶液除油污 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】顺—1,2—二甲基环丙烷和反—1,2—二甲基环丙烷可发生如下转化:

该反应的速率方程可表示为:v(正)=k(正)·c(顺)和v(逆)=k(逆)·c(反),k(正)和k(逆)分别称作正、逆反应速率常数,它们受温度和催化剂影响。下列有关说法正确的是( )

该反应的速率方程可表示为:v(正)=k(正)·c(顺)和v(逆)=k(逆)·c(反),k(正)和k(逆)分别称作正、逆反应速率常数,它们受温度和催化剂影响。下列有关说法正确的是( )
A.某温度时,该反应的平衡常数可表示为K= |
| B.正、逆反应速率常数改变,平衡常数也一定会随之改变 |
| C.若升高温度,平衡逆向移动,则说明正反应的活化能高于逆反应的活化能 |
| D.催化剂可以改变反应速率但不影响平衡,说明催化剂同等程度改变k(正)和k(逆) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】甲烷和水蒸气催化制氢是未来解决能源危机的理想方法之一,其主要反应为:
i.
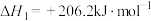
ii.
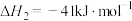
一定温度下,往刚性密闭容器中充入甲烧和水蒸气,发生催化反应。下列说法正确的是
i.

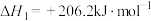
ii.

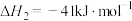
一定温度下,往刚性密闭容器中充入甲烧和水蒸气,发生催化反应。下列说法正确的是
| A.反应i在任意条件下都可以自发 |
| B.降低温度,反应ii的正化学反应速率升高、逆化学反应速率降低 |
C.选择合适的催化剂能提高 的平衡转化率 的平衡转化率 |
D.达到平衡状态后,升高温度,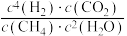 的值变大 的值变大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】部分弱电解质的电离常数如下表:
下列说法错误的是
| 弱电解质 | HCOOH | HCN | H2CO3 |
| 电离常数(25℃) |  | 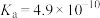 |   |
A.根据电离常数,可判断酸性 |
B.等体积、等浓度的 和 和 溶液中离子总数:前者大于后者 溶液中离子总数:前者大于后者 |
C.向NaCN溶液中通入少量CO2,离子方程式为: |
D. 时,反应 时,反应 的化学平衡常数为 的化学平衡常数为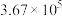 |
您最近一年使用:0次

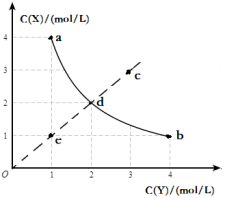
 3H2F2(g) ΔH1=+a kJ·mol-1,②H2F2(g)
3H2F2(g) ΔH1=+a kJ·mol-1,②H2F2(g)  。按照不同配比充入X、Y,达到平衡时容器中X、Y浓度变化如图中曲线(实线)所示。下列判断错误的是
。按照不同配比充入X、Y,达到平衡时容器中X、Y浓度变化如图中曲线(实线)所示。下列判断错误的是