难溶电解质在水中达到沉淀溶解平衡时,下列说法中错误的是
| A.沉淀的速率和溶解的速率相等 |
| B.难溶电解质在水中形成饱和溶液 |
| C.再加入难溶电解质,溶液中各离子的浓度不变 |
| D.难溶电解质溶解形成的阴、阳离子的浓度相等 |
21-22高二上·河南洛阳·期中 查看更多[8]
更新时间:2021-11-13 20:30:05
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是五种银盐的溶度积常数(25℃):
下列说法错误的是
| 化学式 | AgCl |  |  | AgBr | AgI |
| 溶度积 |  |  | 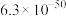 |  | 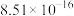 |
A.因AgI溶于水存在沉淀溶解平衡,其电离方程式为 |
| B.AgCl沉淀中加入NaBr溶液,不会生成AgBr沉淀 |
C.在 的混合溶液中,逐滴滴加硝酸银溶液,依次产生AgI、AgBr、AgCl沉淀 的混合溶液中,逐滴滴加硝酸银溶液,依次产生AgI、AgBr、AgCl沉淀 |
D.五种物质在常温下溶解度最大的是 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.升高温度,某沉淀溶解平衡逆向移动,说明它的溶解度是减小的,Ksp也变小 |
| B.Ksp既与难溶电解质的性质和温度有关,也与沉淀的量和溶液中离子浓度有关 |
| C.常温下,向BaCO3饱和溶液中加入Na2CO3固体,BaCO3的Ksp减小 |
| D.向Ca(OH)2悬浊液中加入少量NaOH固体,Ca(OH)2固体质量不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,Ksp(ZnS)=l.6×10-24,Ksp(FeS)=6.4×10-18,其中FeS为黑色晶体,ZnS是一种白色颜料的组成成分。下列说法正确的是
| A.向物质的量浓度相等的FeSO4和ZnSO4混合液中滴加Na2S溶液,先产生黑色沉淀 |
| B.常温下,反应FeS(s)+Zn2+(aq)⇌ZnS(s)+Fe2+(aq)的平衡常数K=4.0×l06 |
| C.在ZnS的饱和溶液中,加入FeSO4溶液,一定不会产生FeS沉淀 |
| D.向FeS悬浊液中通入少许HCl,c(Fe2+)与Ksp(FeS)均增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验操作、现象和结论都正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将HI溶液加入Fe(NO3)3溶液中,充分反应后再加入CCl4混合振荡,静置 | 溶液分层, 下层液体显紫红色 | 氧化性:Fe3+>I2 |
| B | 过量的铁粉和氯气反应,将反应后的固体溶于盐酸后,滴加KSCN溶液 | 溶液不显红色 | 过量铁与氯气反应的产物为FeCl2 |
| C | 室温下,用pH试纸分别测定浓度均为0.1mol/L的Na2SO3溶液和CH3COONa溶液的pH | pH:Na2SO3>CH3COONa | H2SO3酸性弱于CH3COOH |
| D | 向2支装有等物质的量的AgCl、AgI的试管中分别滴加足量等体积等浓度的氨水 | AgCl溶解而AgI不溶解 | 相同温度下,Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】已知锌及其化合物的性质与铝及其化合物相似。如图横坐标为溶液的pH,纵坐标为Zn2+或[Zn(OH)4]2-的物质的量浓度的对数。下列说法中错误的是( )
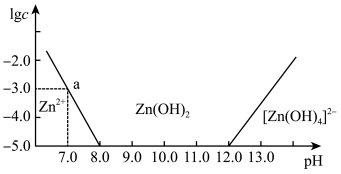

| A.在该温度下,Zn(OH)2的溶度积(Ksp)为1×10-17 |
| B.往1.0 L 1.0 mol·L-1 ZnCl2溶液中加入NaOH固体至pH=6,没有Zn(OH)2沉淀生成 |
| C.往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式为Zn2++4OH-=[Zn(OH)4]2- |
| D.某废液中含Zn2+,为提取Zn2+可以控制溶液中pH的范围为8.0~12.0 |
您最近一年使用:0次




