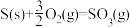已知:
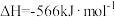


根据以上热化学方程式,判断下列说法正确的是

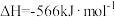


根据以上热化学方程式,判断下列说法正确的是
| A.1molCO完全燃烧,放出热量为283J |
B. 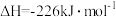 |
C.CO与 反应放出509kJ热量时,电子转移数一定是 反应放出509kJ热量时,电子转移数一定是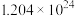 |
| D.CO的燃烧热为-283kJ |
21-22高二上·浙江·期中 查看更多[3]
天津市两校联考2021-2022学年高二上学期第二次质量检测化学试题(已下线)第六单元 化学反应与能量(A卷 新题基础练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)浙江省“七彩阳光”新高考研究联盟2021-2022学年高二上学期期中联考化学试题
更新时间:2021-11-18 16:55:42
|
相似题推荐
单选题
|
较易
(0.85)
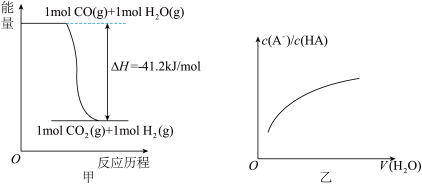
【推荐1】关于下列各图的叙述不正确的是
化学方程式 | 平衡常数K |
F2 + H2 = 2HF | 6.5×1095 |
Cl2 + H2 = 2HCl | 2.6×1033 |
Br2 + H2 = 2HBr | 1.9×1019 |
I2 + H2 = 2HI | 8.7×102 |

| A.已知CO的燃烧热283kJ·mol-1,O2(g) +2 H2(g) = 2H2O(g) ΔH = -483.6 kJ·mol-1,则图甲表示CO和H2O(g)生成CO2和H2的能量变化 |
| B.某温度下,pH =11的NH3∙H2O和pH =1的盐酸等体积混合后(不考虑混合后溶液体积的变化)恰好完全反应,反应后的溶液中NH4+、NH3∙H2O与NH3三种微粒的平衡浓度之和为0.05mol∙L-1 |
| C.在常温下,X2(g) 和 H2反应生成HX的平衡常数如表乙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐渐降低,且X2与H2反应的剧烈程度逐渐减弱 |
D.图丙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,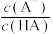 的变化情况 的变化情况 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
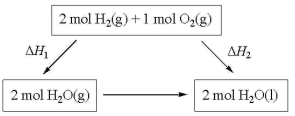
【推荐2】化学反应N2(g)+3H2(g)===2NH3(l)的能量变化如图所示,则该反应的ΔH等于 ( )
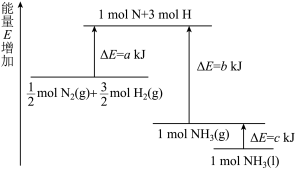

| A.2(a-b-c) kJ·mol-1 | B.-2(b-a) kJ·mol-1 |
| C.- (b+c-a) kJ·mol-1 | D.(a+b) kJ·mol -1 -1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】已知反应N2(g)+3H2(g)⇌2NH3(g)ΔH=﹣92.2kJ·mol﹣1。当反应器中按n(N2):n(H2)=1:3投料后,在不同温度下,反应达到平衡时,得到混合物中NH3的物质的量分数随压强的变化曲线a、b、c如图所示。下列说法正确的是
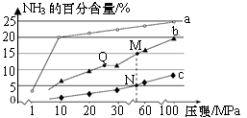

| A.若反应器中充入1molN2和3molH2,则反应达平衡时将释放92.2kJ热量 |
| B.从Q到M,平衡向左移动 |
| C.M、N、Q达到平衡所需时间关系为tQ>tM>tN |
| D.图中M、N、Q点平衡常数K的大小关系为K(N)>K(M)=K(Q) |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法正确的是
| A.热化学方程式中化学计量数不能为分数 |
| B.燃烧热是指101KPa时,1mol纯物质完全燃烧放出的热量 |
| C.化学反应的反应热只与反应体系的始态和终态有关,与反应途径无关 |
| D.所有碰撞都是有效碰撞 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】对于燃烧热,下列叙述正确的是
| A.在25 ℃、101 kPa时,纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫作该物质的燃烧热 |
| B.反应热有正、负之分,燃烧热ΔH全部是正值 |
| C.在25 ℃、101 kPa时,1 mol纯物质完全燃烧生成稳定的氧化物时所放出的热量即为该物质的燃烧热 |
| D.化学方程式前的化学计量数扩大,燃烧热亦扩大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】在下列各说法中,正确的是
| A.热化学方程式中的化学计量数可以是分数 | B. 表示放热反应, 表示放热反应, 表示吸热反应 表示吸热反应 |
C. 的大小与热化学方程式中的计量数无关 的大小与热化学方程式中的计量数无关 | D.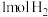 与 与 反应放出的热就是 反应放出的热就是 的燃烧热 的燃烧热 |
您最近一年使用:0次


 的过程中,
的过程中,
 和1mol
和1mol 的总能量大于2mol
的总能量大于2mol 的总能量
的总能量 ,只与反应体系的始态和终态有关,与反应途径无关
,只与反应体系的始态和终态有关,与反应途径无关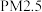 浓度为主要目标。合理使用燃料可减少污染,符合“绿色化学”理念,下列说法正确的是
浓度为主要目标。合理使用燃料可减少污染,符合“绿色化学”理念,下列说法正确的是 ,硫燃烧热的热化学方程式:
,硫燃烧热的热化学方程式: