A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如图的反应关系:
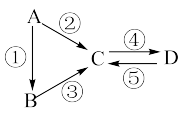
(1)若A为一种常见金属,反应②、⑤均用到同一种黄绿色气体单质,反应④用到A,写出A与水高温下反应的化学方程式___________ 。
(2)若A是一种非金属单质,B常用于制作高档光学器材、光导纤维,C、D为钠盐,其中C可用作粘合剂,反应⑤用到B,条件为高温,则反应⑤的化学方程式为___________ 。
(3)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出该反应的化学方程式:___________ 。
(4)若D物质具有两性,反应②、③均要用强碱溶液,反应④需通入过量的一种引起温室效应的气体。反应④离子方程式___________ 。

(1)若A为一种常见金属,反应②、⑤均用到同一种黄绿色气体单质,反应④用到A,写出A与水高温下反应的化学方程式
(2)若A是一种非金属单质,B常用于制作高档光学器材、光导纤维,C、D为钠盐,其中C可用作粘合剂,反应⑤用到B,条件为高温,则反应⑤的化学方程式为
(3)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出该反应的化学方程式:
(4)若D物质具有两性,反应②、③均要用强碱溶液,反应④需通入过量的一种引起温室效应的气体。反应④离子方程式
更新时间:2021-11-22 21:09:24
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如图中的每一方格表示有关的一种反应物或生成物,其中A和C为无色气体。
填写下列空白:

(1)物质M可以是___ ;C是___ ;F是___ (填化学式)。
(2)反应①的化学方程式是___ 。
(3)反应②的离子方程式是___ 。
填写下列空白:

(1)物质M可以是
(2)反应①的化学方程式是
(3)反应②的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A是灰黑色、有金属光泽的固体单质。根据如图所示的物质之间的转化关系,回答下列有关问题。
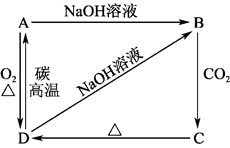
(1)写出A、B、C、D的化学式:A________ ,B________ ,C________ ,D________ 。
(2)写出D→A的化学方程式:__________________________________________ 。
(3)写出下列反应的离子方程式。
B→C:____________________________________ ;
D→B:____________________________________ 。

(1)写出A、B、C、D的化学式:A
(2)写出D→A的化学方程式:
(3)写出下列反应的离子方程式。
B→C:
D→B:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示:

(1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):
A________ 、 B________ 、 D________ 、E________ 。
(2)写出下列反应的化学方程式(请注明反应条件):
A+H2O:____________________ ;
A → D:____________________ 。

(1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):
A
(2)写出下列反应的化学方程式(请注明反应条件):
A+H2O:
A → D:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】某同学在学习元素化合物知识的过程中,发现含有相同元素的物质间在一定条件下存在
转化规律,绘制出如下转化关系图,图中A、B、C、D是由短周期元素组成的物质。

请回答:
(1)若A为单质,其焰色反应为黄色,C为淡黄色固体。则组成A的元素在周期表中的位置是__ ,C的电子式为__ 。
(2)若A为能使湿润红色石蕊试纸变蓝的气体,C为红棕色气体。
①A→B反应的化学方程式是__ 。过量的A的水溶液与AlCl3溶液反应离子方程式为__ 。
②A与C反应生成E和水,E是空气中含量最多的气体。当生成19.6gE时,转移电子的物质的量为__ mol。
(3)若B为能使品红溶液褪色的无色刺激性的气体,B→C反应的化学方程式是__ ,B与KMnO4溶液反应离子方程式为__ 。
转化规律,绘制出如下转化关系图,图中A、B、C、D是由短周期元素组成的物质。

请回答:
(1)若A为单质,其焰色反应为黄色,C为淡黄色固体。则组成A的元素在周期表中的位置是
(2)若A为能使湿润红色石蕊试纸变蓝的气体,C为红棕色气体。
①A→B反应的化学方程式是
②A与C反应生成E和水,E是空气中含量最多的气体。当生成19.6gE时,转移电子的物质的量为
(3)若B为能使品红溶液褪色的无色刺激性的气体,B→C反应的化学方程式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】(1)臭氧可用于烟气脱硝。O3氧化NO结合水洗,可产生HNO3和O2,该反应的化学方程式为_________________________ 。
(2)如图是用NH3脱除烟气中NO的原理。

①该脱硝原理中,NO最终转化为__________ (填化学式)和H2O。
②当消耗2mLNH3和0.5molO2时,除去的NO在标准状况下的体积为________ L。
(3)用碱液脱硝是目前研究的课题之一。
①将NO、NO2通入石灰乳中可制备重要的工业原料Ca(NO3)2。该工艺需控制NO和NO2物质的量之比接近1:1。若n(NO2):n(NO)>1:1,则会导致_____________ ;若n(NO2):n(NO)<1:1,则会导致_____________ 。
②将氢氧化钠溶液脱硝得到的NaNO2、NaNO3的混合液和NaOH溶液分别加到如图所示的电解槽中进行电解。写出A室NO2-发生的电极反应式:______________ 。

(2)如图是用NH3脱除烟气中NO的原理。

①该脱硝原理中,NO最终转化为
②当消耗2mLNH3和0.5molO2时,除去的NO在标准状况下的体积为
(3)用碱液脱硝是目前研究的课题之一。
①将NO、NO2通入石灰乳中可制备重要的工业原料Ca(NO3)2。该工艺需控制NO和NO2物质的量之比接近1:1。若n(NO2):n(NO)>1:1,则会导致
②将氢氧化钠溶液脱硝得到的NaNO2、NaNO3的混合液和NaOH溶液分别加到如图所示的电解槽中进行电解。写出A室NO2-发生的电极反应式:

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。

(1)A物质的化学式为___________ ,A与足量NaOH溶液加热条件下反应的离子方程式为___________ 。
(2)当X为强碱时,写出过量B与Cl2反应的化学方程式___________ ,该反应中氧化产物与还原产物的物质的量之比为___________ 。
(3)当X为强碱时,写出铜与F的稀溶液反应的离子方程式___________ 。
(4)当X为强酸时,B与D发生反应的化学方程式为___________ 。

(1)A物质的化学式为
(2)当X为强碱时,写出过量B与Cl2反应的化学方程式
(3)当X为强碱时,写出铜与F的稀溶液反应的离子方程式
(4)当X为强酸时,B与D发生反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】磷矿石的主要成分是Ca5F(PO4)3,含少量MgO、Fe2O3等杂质。工业上以磷矿石为原料制备H3PO4的常用流程如图:
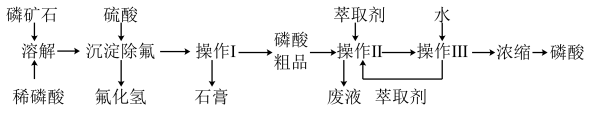
已知:Ca5F(PO4)3+7H3PO4→5Ca(H2PO4)2+HF
(1)采用这种方法在实验室溶解磷矿石___ (填“能”或“不能”)用玻璃仪器,原因是___ 。
(2)操作Ⅰ的名称是___ ,所得磷酸粗品中除含H+外,还含有的阳离子是__ 。
(3)在实验室中实现操作Ⅱ和Ⅲ所需要的玻璃仪器有___ ,推测该萃取剂一定具有的性质是__ 。
a.该萃取剂与水互不相溶
b.相同条件下,该萃取剂的密度比水小
c.磷酸在该萃取剂中的溶解度很小
d.某些磷酸二氢盐在该萃取剂中的溶解度很小
(4)采用该流程除制取磷酸外,还有__ 等副产品产生,请说出其中一种副产品的用___ 。
(5)与直接用硫酸溶解磷矿石的工艺相比,该工艺的优点是___ 。
(6)测定磷酸产品的浓度可采用滴定法。准确量取10.00mL磷酸产品(密度为1.526g/cm3)溶于水配成1L溶液;取溶解后的溶液20.00mL,以甲基橙作指示剂,用0.103mol/L标准NaOH溶液滴定至终点(生成NaH2PO4),消耗NaOH溶液21.35mL。该磷酸产品的质量分数为___ 。

已知:Ca5F(PO4)3+7H3PO4→5Ca(H2PO4)2+HF
(1)采用这种方法在实验室溶解磷矿石
(2)操作Ⅰ的名称是
(3)在实验室中实现操作Ⅱ和Ⅲ所需要的玻璃仪器有
a.该萃取剂与水互不相溶
b.相同条件下,该萃取剂的密度比水小
c.磷酸在该萃取剂中的溶解度很小
d.某些磷酸二氢盐在该萃取剂中的溶解度很小
(4)采用该流程除制取磷酸外,还有
(5)与直接用硫酸溶解磷矿石的工艺相比,该工艺的优点是
(6)测定磷酸产品的浓度可采用滴定法。准确量取10.00mL磷酸产品(密度为1.526g/cm3)溶于水配成1L溶液;取溶解后的溶液20.00mL,以甲基橙作指示剂,用0.103mol/L标准NaOH溶液滴定至终点(生成NaH2PO4),消耗NaOH溶液21.35mL。该磷酸产品的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W为四种短周期元素。X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价的代数和为6;Z在地壳中的含量仅次于氧;Y、Z、W同周期,W的最低负化合价为-2。回答下列问题:
(1)Y-的结构示意图为____________ 。
(2)写出含有10个中子的X原子的原子符号_____________ 。
(3)Z的最高价氧化物与Z同主族的单质A能发生置换反应,这个反应在工业上是获得Z的一步重要反应。写出该步反应的化学方程式,并用单线桥法标出电子转移的方向与数目________________ 。
(4)向WX2溶液中加入足量的NaOH溶液,反应的离子方程式为___________ 。
(5)Y的气态氢化物与氨气在空气中相遇有白烟生成,该反应的化学方程式为_____________ 。
(6)ZX2与NaOH溶液反应的化学方程式为_____________________ 。
(1)Y-的结构示意图为
(2)写出含有10个中子的X原子的原子符号
(3)Z的最高价氧化物与Z同主族的单质A能发生置换反应,这个反应在工业上是获得Z的一步重要反应。写出该步反应的化学方程式,并用单线桥法标出电子转移的方向与数目
(4)向WX2溶液中加入足量的NaOH溶液,反应的离子方程式为
(5)Y的气态氢化物与氨气在空气中相遇有白烟生成,该反应的化学方程式为
(6)ZX2与NaOH溶液反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】氟碳铈矿(主要成分为 )是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的工艺流程如图所示。回答下列问题:
)是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的工艺流程如图所示。回答下列问题:

(1) 中F的化合价为
中F的化合价为_______ 。操作Ⅰ的名称为_______ 。
(2)氧化焙烧操作不能使用陶瓷容器。原因是_______ (用化学方程式解释)。
(3)焙烧后的产物之一为 ,则酸浸时主要反应的离子方程式为
,则酸浸时主要反应的离子方程式为_______ 。
(4)酸浸时不能用浓盐酸,原因是_______ (结合化学方程式解释)。
(5)为了提高酸浸率,可以适当提高反应温度,但温度偏高浸出率反而会减小,其原因是_______ 。
(6)有机物 能将
能将 从水溶液中提取出来,该过程可表示为
从水溶液中提取出来,该过程可表示为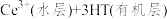
 。试解释向
。试解释向 中加入稀硫酸的作用及其原理:
中加入稀硫酸的作用及其原理:_______ 。
(7)写出向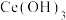 悬浊液中通入氧气得到产品
悬浊液中通入氧气得到产品 的化学方程式:
的化学方程式: _______ 。
 )是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的工艺流程如图所示。回答下列问题:
)是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的工艺流程如图所示。回答下列问题:
(1)
 中F的化合价为
中F的化合价为(2)氧化焙烧操作不能使用陶瓷容器。原因是
(3)焙烧后的产物之一为
 ,则酸浸时主要反应的离子方程式为
,则酸浸时主要反应的离子方程式为(4)酸浸时不能用浓盐酸,原因是
(5)为了提高酸浸率,可以适当提高反应温度,但温度偏高浸出率反而会减小,其原因是
(6)有机物
 能将
能将 从水溶液中提取出来,该过程可表示为
从水溶液中提取出来,该过程可表示为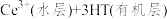
 。试解释向
。试解释向 中加入稀硫酸的作用及其原理:
中加入稀硫酸的作用及其原理:(7)写出向
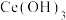 悬浊液中通入氧气得到产品
悬浊液中通入氧气得到产品 的化学方程式:
的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业上可由铝土矿(主要成分是Al2O3和Fe2O3)和焦炭制备,流程如下:
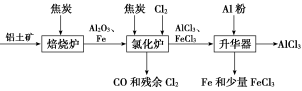
已知:AlCl3、FeCl3分别在183 ℃、315 ℃时升华
(1)Cl2的电子式________ 。
(2)氯化炉中Al2O3、Cl2和焦炭在高温下发生反应的化学方程式为______________ ;炉气中残余的少量Cl2,可用NaOH溶液吸收,其离子方程式为_____________________________________ 。
(3)700 ℃时,升华器中物质经充分反应后需降温实现FeCl3和AlCl3的分离。请选择合适的温度范围________ 。
a.低于183 ℃ b.介于183 ℃和315 ℃之间
c.高于315 ℃
(4)样品(含少量FeCl3)中AlCl3含量可通过下列操作测得(部分物质略去)。
m克样品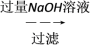 NaAlO2溶液
NaAlO2溶液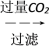 Al(OH)3
Al(OH)3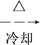 n克Al2O3
n克Al2O3
计算该样品中AlCl3的质量分数________ (结果用m、n表示,不必化简)。

已知:AlCl3、FeCl3分别在183 ℃、315 ℃时升华
(1)Cl2的电子式
(2)氯化炉中Al2O3、Cl2和焦炭在高温下发生反应的化学方程式为
(3)700 ℃时,升华器中物质经充分反应后需降温实现FeCl3和AlCl3的分离。请选择合适的温度范围
a.低于183 ℃ b.介于183 ℃和315 ℃之间
c.高于315 ℃
(4)样品(含少量FeCl3)中AlCl3含量可通过下列操作测得(部分物质略去)。
m克样品
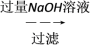 NaAlO2溶液
NaAlO2溶液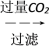 Al(OH)3
Al(OH)3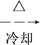 n克Al2O3
n克Al2O3计算该样品中AlCl3的质量分数
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】工业上用铝土矿(主要成分为A12O3,还有少量的Fe2O3,SiO2等杂质)提取氧化铝作冶炼铝的原料,提取的操作过程如图:

(1)I和II步骤中分离溶液和沉淀的操作是:______ 。
(2)沉淀M中除含有泥沙外,一定还含有______ ,固体N是_____ 。
(3)滤液X中,含铝元素的溶质的化学式为______ ,它属于______ (填“酸”、“碱”或“盐”)类物质。
(4)请写出步骤Ⅱ的离子方程式______ 。
(5)实验室里制取A1(OH)3,在AlCl3溶液中最好加入______ 。

(1)I和II步骤中分离溶液和沉淀的操作是:
(2)沉淀M中除含有泥沙外,一定还含有
(3)滤液X中,含铝元素的溶质的化学式为
(4)请写出步骤Ⅱ的离子方程式
(5)实验室里制取A1(OH)3,在AlCl3溶液中最好加入
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其他为化合物。试推断:
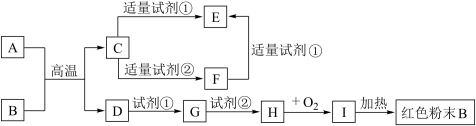
(1)写出物质的化学式:A:______________ B:_____________
C:_____________ Ⅰ:________________
(2)向F中逐滴滴加试剂①的现象为________________
(3)写出下列反应的方程式:
C→E的离子方程式________________
C→F的离子方程式________________
G→H的离子方程式________________

(1)写出物质的化学式:A:
C:
(2)向F中逐滴滴加试剂①的现象为
(3)写出下列反应的方程式:
C→E的离子方程式
C→F的离子方程式
G→H的离子方程式
您最近一年使用:0次



