(1)臭氧可用于烟气脱硝。O3氧化NO结合水洗,可产生HNO3和O2,该反应的化学方程式为_________________________ 。
(2)如图是用NH3脱除烟气中NO的原理。

①该脱硝原理中,NO最终转化为__________ (填化学式)和H2O。
②当消耗2mLNH3和0.5molO2时,除去的NO在标准状况下的体积为________ L。
(3)用碱液脱硝是目前研究的课题之一。
①将NO、NO2通入石灰乳中可制备重要的工业原料Ca(NO3)2。该工艺需控制NO和NO2物质的量之比接近1:1。若n(NO2):n(NO)>1:1,则会导致_____________ ;若n(NO2):n(NO)<1:1,则会导致_____________ 。
②将氢氧化钠溶液脱硝得到的NaNO2、NaNO3的混合液和NaOH溶液分别加到如图所示的电解槽中进行电解。写出A室NO2-发生的电极反应式:______________ 。

(2)如图是用NH3脱除烟气中NO的原理。

①该脱硝原理中,NO最终转化为
②当消耗2mLNH3和0.5molO2时,除去的NO在标准状况下的体积为
(3)用碱液脱硝是目前研究的课题之一。
①将NO、NO2通入石灰乳中可制备重要的工业原料Ca(NO3)2。该工艺需控制NO和NO2物质的量之比接近1:1。若n(NO2):n(NO)>1:1,则会导致
②将氢氧化钠溶液脱硝得到的NaNO2、NaNO3的混合液和NaOH溶液分别加到如图所示的电解槽中进行电解。写出A室NO2-发生的电极反应式:

更新时间:2020-01-26 09:14:06
|
相似题推荐
【推荐1】CO2还原为甲醇(CH3OH)是人工合成淀粉的第一步。CO2催化加氢主要反应为:CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) ΔH=-49.4 kJ·mol−1。
(1)H2O分子用电子式表示为_______ 。该反应中每生成0.5 mol甲醇,转移电子的物质的量是_______ mol。
(2)一定条件下,该反应过程中的能量变化情况如图所示,图中E2-E1 =_______ kJ·mol−1。
 CH3OH(g) + H2O(g),测得不同时间(t)各物质的物质的量如下表:
CH3OH(g) + H2O(g),测得不同时间(t)各物质的物质的量如下表:
①0 ~ t1 min内,用H2浓度变化表示该反应的化学反应速率为_______ mol·L−1·min−1。
②下列有关上述反应的说法正确的是_______ (填序号)
A.CH3OH中的化学键是共价键
B.消耗3 mol H2(g)的同时生成1 mol H2O(g),此时该反应达到化学平衡
C.0 ~ t1 min内反应放出的热小于t1~ t2 min内放出的热
(4)甲醇(CH3OH)燃料电池的电极采用膜电极,该电极由催化剂层和质子交换膜构成,其中质子交换膜能传导H+,同时作为隔膜防止两极的物质相互反应。该电池的工作原理如图:
_______ 。(填“电极a”或“电极b”)
②工作时,电极b的电极反应式是_______ 。
(1)H2O分子用电子式表示为
(2)一定条件下,该反应过程中的能量变化情况如图所示,图中E2-E1 =

 CH3OH(g) + H2O(g),测得不同时间(t)各物质的物质的量如下表:
CH3OH(g) + H2O(g),测得不同时间(t)各物质的物质的量如下表:| t / min | n(CO2) / mol | n(H2) / mol | n(CH3OH) / mol | n(H2O) / mol |
| 0 | 2.00 | 6.00 | 0 | 0 |
| t1 | 1.65 | a | 0.35 | 0.35 |
| t2 | b | 3.60 | 0.80 | 0.80 |
| t3 | b | 3.60 | 0.80 | 0.80 |
②下列有关上述反应的说法正确的是
A.CH3OH中的化学键是共价键
B.消耗3 mol H2(g)的同时生成1 mol H2O(g),此时该反应达到化学平衡
C.0 ~ t1 min内反应放出的热小于t1~ t2 min内放出的热
(4)甲醇(CH3OH)燃料电池的电极采用膜电极,该电极由催化剂层和质子交换膜构成,其中质子交换膜能传导H+,同时作为隔膜防止两极的物质相互反应。该电池的工作原理如图:

②工作时,电极b的电极反应式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:

已知:
①2KOH + Cl2 = KCl + KClO + H2O(条件:温度较低)
②6KOH + 3Cl2 = 5KCl + KClO3 + 3H2O(条件:温度较高)
③2Fe(NO3)3 + 3KClO + 10KOH = 2K2FeO4 + 6KNO3 + 3KCl + 5H2O
回答下列问题:
(1)该生产工艺应在______________ (填“温度较高”或“温度较低”)情况下进行,从绿色化学的角度考虑通入氯气速率应________ (填“较快”或“较慢”);
(2)写出工业上制取Cl2的化学方程式_____________________________________ ;
(3)K2 FeO4可作为新型多功能水处理剂的原因是______________________ ;
(4)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度为____________ (保留整数);
(5)在“反应液I”中加KOH固体的目的是__________ :
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为 KClO
(6)从“反应液II”中分离出K2FeO4后,会有副产品_____________ (写化学式)。
(7)该工艺每得到1.98 kg K2FeO4,理论上消耗Cl2的物质的量为___________ mol。

已知:
①2KOH + Cl2 = KCl + KClO + H2O(条件:温度较低)
②6KOH + 3Cl2 = 5KCl + KClO3 + 3H2O(条件:温度较高)
③2Fe(NO3)3 + 3KClO + 10KOH = 2K2FeO4 + 6KNO3 + 3KCl + 5H2O
回答下列问题:
(1)该生产工艺应在
(2)写出工业上制取Cl2的化学方程式
(3)K2 FeO4可作为新型多功能水处理剂的原因是
(4)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度为
(5)在“反应液I”中加KOH固体的目的是
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为 KClO
(6)从“反应液II”中分离出K2FeO4后,会有副产品
(7)该工艺每得到1.98 kg K2FeO4,理论上消耗Cl2的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】硫化锌(ZnS)是一种半导体材料,某小组在实验室制备硫化锌: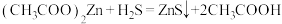 。回答下列问题:
。回答下列问题:
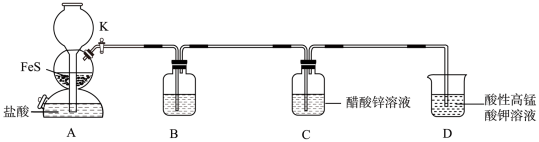
(1)装置A中发生反应的化学方程式为__________________ 。
(2)装置B中盛装的试剂可能是____________ (填标号)。
a.NaOH溶液 b.饱和NaHS溶液 c.新制氯水
(3)装置A能控制反应的发生和停止,装置C中完全反应后,停止装置A中反应的操作是____________ 。
(4)当装置D中0.01mol 完全反应时,转移0.08mol电子,则该反应中氧化产物与还原产物的物质的量之比为
完全反应时,转移0.08mol电子,则该反应中氧化产物与还原产物的物质的量之比为____________ 。
(5)实验完毕后,从装置C中得到较纯净的ZnS的操作是____________ (填标号)、洗涤、干燥。
(6)测定ZnS产品纯度。
准确称取mg产品(杂质不含Zn元素)溶于足量盐酸,加热至不产生气泡,稀释成250mL溶液,准确量取25.00mL稀释后的溶液于锥形瓶中,调节pH在1.5~3,用二苯胺作指示剂,用 的亚铁氰化钾{
的亚铁氰化钾{ }标准溶液滴定至终点,消耗标准溶液VmL。
}标准溶液滴定至终点,消耗标准溶液VmL。
已知:滴定反应为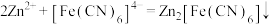 。
。
①加热的目的是____________ 。
②该产品中ZnS的质量分数为____________ (用含m、c、V的代数式表示)%。
③如果其他操作均正确,滴定前俯视读数,滴定终点时仰视读数,那么测得结果____________ (填“偏高”、“偏低”或“无影响”)。
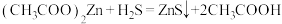 。回答下列问题:
。回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)装置B中盛装的试剂可能是
a.NaOH溶液 b.饱和NaHS溶液 c.新制氯水
(3)装置A能控制反应的发生和停止,装置C中完全反应后,停止装置A中反应的操作是
(4)当装置D中0.01mol
 完全反应时,转移0.08mol电子,则该反应中氧化产物与还原产物的物质的量之比为
完全反应时,转移0.08mol电子,则该反应中氧化产物与还原产物的物质的量之比为(5)实验完毕后,从装置C中得到较纯净的ZnS的操作是

(6)测定ZnS产品纯度。
准确称取mg产品(杂质不含Zn元素)溶于足量盐酸,加热至不产生气泡,稀释成250mL溶液,准确量取25.00mL稀释后的溶液于锥形瓶中,调节pH在1.5~3,用二苯胺作指示剂,用
 的亚铁氰化钾{
的亚铁氰化钾{ }标准溶液滴定至终点,消耗标准溶液VmL。
}标准溶液滴定至终点,消耗标准溶液VmL。已知:滴定反应为
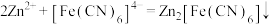 。
。①加热的目的是
②该产品中ZnS的质量分数为
③如果其他操作均正确,滴定前俯视读数,滴定终点时仰视读数,那么测得结果
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】依据如图中氮元素及其化合物的转化关系,回答问题:
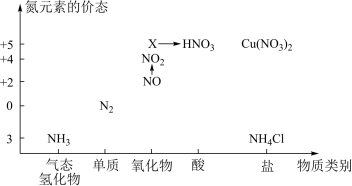
(1)图中,X的化学式为_______ 。
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:_______ 。
②下列试剂不能用于干燥NH3的是_______ (填字母)。
A.浓硫酸 B.碱石灰 C.氯化钙固体
③氨气是重要的化工原料,可以合成多种物质,写出催化氧化的化学方程式:_______ 。
(3)回答下列关于NO、NO2的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,发生的反应为:2NO+2CO N2+2CO2该反应中,被氧化的物质是
N2+2CO2该反应中,被氧化的物质是_______ (填化学式),若反应中生成1molN2,则转移电子_______ mol。
②NO→NO2的颜色变化是_______ 。
(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:
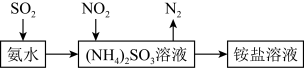
NO2被吸收过程的离子方程式是_______ 。

(1)图中,X的化学式为
(2)回答下列关于NH3的问题:
①实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为:
②下列试剂不能用于干燥NH3的是
A.浓硫酸 B.碱石灰 C.氯化钙固体
③氨气是重要的化工原料,可以合成多种物质,写出催化氧化的化学方程式:
(3)回答下列关于NO、NO2的问题:
①汽车排气管上装有催化转化器可减少尾气对环境的污染,发生的反应为:2NO+2CO
 N2+2CO2该反应中,被氧化的物质是
N2+2CO2该反应中,被氧化的物质是②NO→NO2的颜色变化是
(4)工业生产中利用氨水吸收SO2和NO2,原理如图所示:

NO2被吸收过程的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx的反应进行了探究。回答下列问题:
(1)氨气的制备

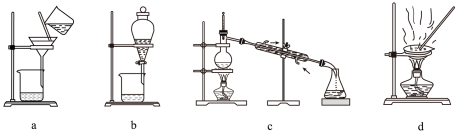
①氨气的发生装置可以选择上图中的_______ (填字母),反应的化学方程式为________ 。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序:发生装置→_________ (按气流方向,用小写字母表示)。
(2)二氧化氮的制备
二氧化氮可以用铜和浓硝酸制备,反应的化学方程式为_________ 。
(3)氨气与二氧化氮的反应
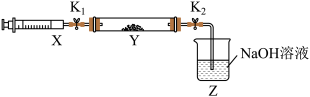
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按下图装置进行实验。
(1)氨气的制备

①氨气的发生装置可以选择上图中的
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序:发生装置→
(2)二氧化氮的制备
二氧化氮可以用铜和浓硝酸制备,反应的化学方程式为
(3)氨气与二氧化氮的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按下图装置进行实验。

| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,推动注射器活塞,使X中的氨气缓慢通入Y管中完全反应 | ①Y管中 | ②反应的化学方程式为 |
| 将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝集 |
| 打开K2 | ③ | ④NaOH溶液的作用是 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】二氧化氮是主要的大气污染物之一,工业上在一定条件下用NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略):

回答下列问题:
(1)用装置A制备NH3,其中发生反应的化学方程式为___________ ;装置B内的试剂是___________ 。
(2)装置D中发生反应的化学方程式是___________ 。
(3)用装置M材的方法收集氮气,是因为氮气的密度比空气___________ (填“大”或“小”)。
(4)NH3和NO2在M中充分反应,产生两种对环境友好的物质,该反应的化学方程式为___________ ,,M中可观察到的现象是___________ 。

回答下列问题:
(1)用装置A制备NH3,其中发生反应的化学方程式为
(2)装置D中发生反应的化学方程式是
(3)用装置M材的方法收集氮气,是因为氮气的密度比空气
(4)NH3和NO2在M中充分反应,产生两种对环境友好的物质,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验小组制备 ,并探究其性质。
,并探究其性质。
I.制备

(1)仪器a的名称是___________ ;气体b的化学式为___________ 。用漏斗代替导管的目的是___________ (答2条)。
(2)为检验B中制得 ,甲进行以下实验:
,甲进行以下实验:
乙认为上述3组实验无法证明B中一定含 ,还需补充实验,理由是
,还需补充实验,理由是___________ 。
II.探究 的性质
的性质
资料:i. 在溶液中呈棕色。
在溶液中呈棕色。
ii. 在溶液中不稳定,易分解产生
在溶液中不稳定,易分解产生 和
和 气体。
气体。
(3)溶液迅速变为棕色的原因是___________ 。已知棕色溶液变浅是由于生成了 ,反应的离子方程式是
,反应的离子方程式是___________ 。
(4)最终棕褐色溶液的成分是 ,测得装置中混合溶液体积为
,测得装置中混合溶液体积为 ,设计如下实验测定其组成。
,设计如下实验测定其组成。
资料:充分反应后, 全部转化为
全部转化为 。
。

加掩蔽剂 的原理和目的是(掩蔽
的原理和目的是(掩蔽 的颜色除外)
的颜色除外)___________ 。由上述数据可知 中
中
___________ (用含 、
、 的代数式表示)。
的代数式表示)。
 ,并探究其性质。
,并探究其性质。I.制备


(1)仪器a的名称是
(2)为检验B中制得
 ,甲进行以下实验:
,甲进行以下实验:| 序号 | 试管 | 操作 | 现象 |
| ① | 2mLB中溶液 | 加   溶液,滴加几滴淀粉溶液 溶液,滴加几滴淀粉溶液 | 不变蓝 |
| ② | 2mLB中溶液 | 滴加几滴 溶液至 溶液至 ,加 ,加   溶液,滴加几滴淀粉溶液 溶液,滴加几滴淀粉溶液 | 变蓝 |
| ③ | 2mL | 滴加几滴 溶液至 溶液至 ,加 ,加   溶液,滴加几滴淀粉溶液 溶液,滴加几滴淀粉溶液 | 不变蓝 |
 ,还需补充实验,理由是
,还需补充实验,理由是II.探究
 的性质
的性质| 装置 | 操作 | 现象 |
 | 取   溶液于试剂瓶中,加入几滴 溶液于试剂瓶中,加入几滴 溶液酸化,再加入 溶液酸化,再加入   溶液,迅速塞上橡胶塞,缓缓通入足量 溶液,迅速塞上橡胶塞,缓缓通入足量 | i.溶液迅速变为棕色 ii.溶液逐渐变浅,有无色气泡产 生,溶液上方为浅红棕色 ⅲ。最终形成棕褐色溶液 |
 在溶液中呈棕色。
在溶液中呈棕色。ii.
 在溶液中不稳定,易分解产生
在溶液中不稳定,易分解产生 和
和 气体。
气体。(3)溶液迅速变为棕色的原因是
 ,反应的离子方程式是
,反应的离子方程式是(4)最终棕褐色溶液的成分是
 ,测得装置中混合溶液体积为
,测得装置中混合溶液体积为 ,设计如下实验测定其组成。
,设计如下实验测定其组成。资料:充分反应后,
 全部转化为
全部转化为 。
。
加掩蔽剂
 的原理和目的是(掩蔽
的原理和目的是(掩蔽 的颜色除外)
的颜色除外) 中
中
 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氨气在工农业生产中有着重要应用,请回答下列问题:
I.实验室用消石灰和氯化铵固体制备NH3,并验证其还原性。
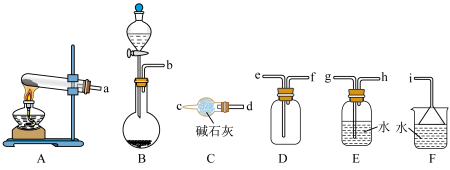
(1)仪器C的名称为_______ ;用消石灰和氯化铵固体共热制取氨气的发生装置为_______ (填“A”或“B”),写出该反应的化学方程式:_______ 。
(2)欲收集一瓶干燥的NH3,选择如图的装置,其连接顺序为:发生装置→_______ (按气流方向,用小写字母表示)。
(3)将制得的氨气通入灼热的氧化铜粉末中,一段时间后,黑色粉末逐渐变红,并产生无毒的气体,写出该反应的化学方程式:_______ 。
Ⅱ.如图为工业制备硝酸的工艺流程,请回答相关问题:

(4)Pt-Rh合金网上发生的化学反应方程式为_______ 。
(5)硝酸工业尾气中的NO、NO2进入大气后,会形成光化学烟雾、破坏臭氧层等。可用氢氧化钠溶液对含氮氧化物的废气进行处理,反应的化学方程式如下:NO+NO2+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO2+NaNO3+H2O,将一定量NO和NO2的混合气体通入300mL5mol•L-1NaOH溶液中,恰好被完全吸收,则标准状况下NO最多为_______ L。
I.实验室用消石灰和氯化铵固体制备NH3,并验证其还原性。

(1)仪器C的名称为
(2)欲收集一瓶干燥的NH3,选择如图的装置,其连接顺序为:发生装置→
(3)将制得的氨气通入灼热的氧化铜粉末中,一段时间后,黑色粉末逐渐变红,并产生无毒的气体,写出该反应的化学方程式:
Ⅱ.如图为工业制备硝酸的工艺流程,请回答相关问题:

(4)Pt-Rh合金网上发生的化学反应方程式为
(5)硝酸工业尾气中的NO、NO2进入大气后,会形成光化学烟雾、破坏臭氧层等。可用氢氧化钠溶液对含氮氧化物的废气进行处理,反应的化学方程式如下:NO+NO2+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO2+NaNO3+H2O,将一定量NO和NO2的混合气体通入300mL5mol•L-1NaOH溶液中,恰好被完全吸收,则标准状况下NO最多为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】铜和硝酸的反应实验是体现硝酸重要性质的实验,某教师设计了如图装置进行铜和稀硝酸的反应实验,步骤如下:
步骤ⅰ.将弹簧状细铜丝放入注射器 底部并固定,注射器
底部并固定,注射器 吸入少量蒸馏水后将活塞推至最低处;注射器
吸入少量蒸馏水后将活塞推至最低处;注射器 吸取
吸取 溶液(过量),注射器
溶液(过量),注射器 于烧杯中吸取
于烧杯中吸取 稀硝酸,注射器
稀硝酸,注射器 吸取
吸取 (过量)。
(过量)。
步骤ⅱ.按图连接好装置,打开止水夹 、
、 ,关闭
,关闭 、
、 ,将注射器
,将注射器 中的稀硝酸注入
中的稀硝酸注入 中。
中。
步骤ⅲ.关闭止水夹 ,打开止水夹
,打开止水夹 ,抽动注射器
,抽动注射器 的活塞,将注射器
的活塞,将注射器 中生成的
中生成的 气体全部抽入
气体全部抽入 中。
中。
步骤ⅳ.关闭止水夹 ,打开止水夹
,打开止水夹 ,将注射器
,将注射器 中气体全部抽入
中气体全部抽入 中。
中。 、
、 的容积为
的容积为 ,注射器
,注射器 、
、 的容积为
的容积为 ;②止水夹
;②止水夹 、
、 、
、 、
、 连在四通管上;③该实验中,铜与稀硝酸反应生成的气体只有
连在四通管上;③该实验中,铜与稀硝酸反应生成的气体只有 。
。
请回答下列问题:
(1)步骤ⅰ中注射器 吸入少量蒸馏水后将活塞推至最低处的目的是
吸入少量蒸馏水后将活塞推至最低处的目的是______ ;步骤ⅱ注射器 中的稀硝酸注入
中的稀硝酸注入 中时发生反应的化学方程式为
中时发生反应的化学方程式为______ ,观察到的现象为______ ,该反应中稀硝酸体现了______ (填化学性质)。
(2)步骤ⅲ将注射器 中生成的气体全部抽入
中生成的气体全部抽入 中,注射器
中,注射器 中能观察到的现象为
中能观察到的现象为______ ;该过程中, 发生了
发生了______ (填“氧化”或“还原”)反应。
(3)步骤ⅳ将注射器 中气体全部抽入
中气体全部抽入 中,
中, 和
和 的混合气体与
的混合气体与 溶液反应生成的盐只有
溶液反应生成的盐只有 ,该反应的离子方程式为
,该反应的离子方程式为______ ,该反应中氧化剂和氧化产物的物质的量之比为______ 。
(4)若反应过程中有 铜丝参与反应,要使注射器
铜丝参与反应,要使注射器 中产生的
中产生的 最终在注射器
最终在注射器 中全部转化为
中全部转化为 ,需要消耗
,需要消耗______ 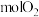 。
。
步骤ⅰ.将弹簧状细铜丝放入注射器
 底部并固定,注射器
底部并固定,注射器 吸入少量蒸馏水后将活塞推至最低处;注射器
吸入少量蒸馏水后将活塞推至最低处;注射器 吸取
吸取 溶液(过量),注射器
溶液(过量),注射器 于烧杯中吸取
于烧杯中吸取 稀硝酸,注射器
稀硝酸,注射器 吸取
吸取 (过量)。
(过量)。步骤ⅱ.按图连接好装置,打开止水夹
 、
、 ,关闭
,关闭 、
、 ,将注射器
,将注射器 中的稀硝酸注入
中的稀硝酸注入 中。
中。步骤ⅲ.关闭止水夹
 ,打开止水夹
,打开止水夹 ,抽动注射器
,抽动注射器 的活塞,将注射器
的活塞,将注射器 中生成的
中生成的 气体全部抽入
气体全部抽入 中。
中。步骤ⅳ.关闭止水夹
 ,打开止水夹
,打开止水夹 ,将注射器
,将注射器 中气体全部抽入
中气体全部抽入 中。
中。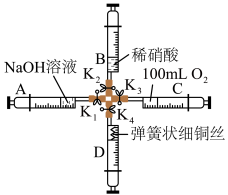
 、
、 的容积为
的容积为 ,注射器
,注射器 、
、 的容积为
的容积为 ;②止水夹
;②止水夹 、
、 、
、 、
、 连在四通管上;③该实验中,铜与稀硝酸反应生成的气体只有
连在四通管上;③该实验中,铜与稀硝酸反应生成的气体只有 。
。请回答下列问题:
(1)步骤ⅰ中注射器
 吸入少量蒸馏水后将活塞推至最低处的目的是
吸入少量蒸馏水后将活塞推至最低处的目的是 中的稀硝酸注入
中的稀硝酸注入 中时发生反应的化学方程式为
中时发生反应的化学方程式为(2)步骤ⅲ将注射器
 中生成的气体全部抽入
中生成的气体全部抽入 中,注射器
中,注射器 中能观察到的现象为
中能观察到的现象为 发生了
发生了(3)步骤ⅳ将注射器
 中气体全部抽入
中气体全部抽入 中,
中, 和
和 的混合气体与
的混合气体与 溶液反应生成的盐只有
溶液反应生成的盐只有 ,该反应的离子方程式为
,该反应的离子方程式为(4)若反应过程中有
 铜丝参与反应,要使注射器
铜丝参与反应,要使注射器 中产生的
中产生的 最终在注射器
最终在注射器 中全部转化为
中全部转化为 ,需要消耗
,需要消耗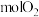 。
。
您最近一年使用:0次
【推荐1】Ⅰ.环氧乙烷常用于医学消毒,工业上常用乙烯氧化法生产,其反应原理为:CH2=CH2(g)+ O2(g)
O2(g)
 (g);ΔH=-120kJ/mol;
(g);ΔH=-120kJ/mol;
(2)化工生产设计时,常用串联多个反应器的工艺方法进行合成,并在两个相同的反应器中间加产物吸收装置和热交换降温装置,设计这种工艺的目的
Ⅱ.反应过程中常伴随副反应
 ;ΔH=-1350kJ/mol,在恒容密闭容器中充入
;ΔH=-1350kJ/mol,在恒容密闭容器中充入 乙烯和含
乙烯和含 的净化空气,在
的净化空气,在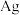 (耐热)催化下发生上述两个反应,反应相同时间后测得乙烯的转化率
(耐热)催化下发生上述两个反应,反应相同时间后测得乙烯的转化率 及
及 的分压随温度变化如图所示:
的分压随温度变化如图所示:
 点:v正
点:v正(4)200℃时测得环氧乙烷的选择性为
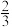 (某产物的选择性
(某产物的选择性 ),计算该温度下主反应的平衡常数(用物质分压表示
),计算该温度下主反应的平衡常数(用物质分压表示
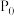 的式子表示)。
的式子表示)。Ⅲ.我国化学工作者最新发明用电解法制乙烯,原理如图所示。

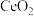 多孔单晶,其在氧化过程可以促进晶格氧向活性氧的转变。
多孔单晶,其在氧化过程可以促进晶格氧向活性氧的转变。(5)①阳极的电极反应式为
②如图为
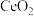 的晶胞(●、○分别表示
的晶胞(●、○分别表示 或
或 ),该晶胞中
),该晶胞中 的配位数为
的配位数为 ,则该
,则该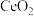 晶体的密度为
晶体的密度为 (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 的摩尔质量用
的摩尔质量用 表示,
表示, )。
)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】清洁能源的综合利用可有效降低碳排放,是实现“碳中和、碳达峰"的重要途径。
(1)以环己烷为原料通过芳构化反应生产苯,同时可获取氢气。图甲是该反应过程中几种物质间的能量关系。
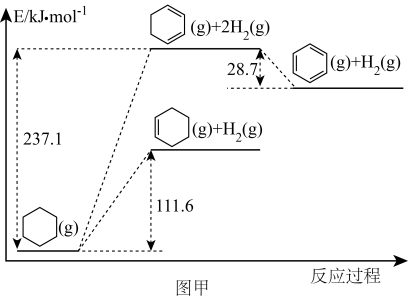
芳构化反应: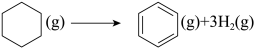 ΔH=
ΔH=_______ kJ/mol。
(2)H2和CO2合成乙醇反应为: 2CO2(g)+6H2(g)⇌C2H5OH(g)+3H2O(g)。 将等物质的量的CO2和H2充入一刚性容器中,测得平衡时乙醇的体积分数随温度和压强的关系如图乙。
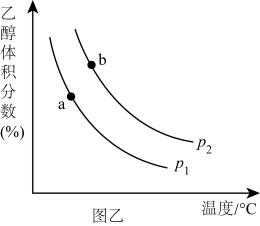
①压强P1_______ P2(填*>”“=”或“<", 下同),a、b两点的平衡常数Ka_______ Kb。
②已知Arrhenius经验公式为RInk=- +C(Ea为活化能,k为速率常数, R和C为常数),为探究m、n两种催化剂的储化效能,进行了实验探究,依据实验数获得图丙曲线。
+C(Ea为活化能,k为速率常数, R和C为常数),为探究m、n两种催化剂的储化效能,进行了实验探究,依据实验数获得图丙曲线。
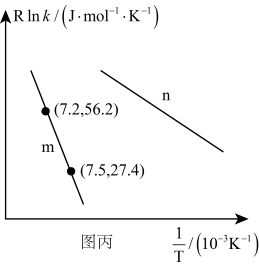
在m催化剂作用下,该反应的活化能Ea=_______ J/mol。 从图中信息获知催化效能较高的催化剂是_______ (“m"或“n"), 判断理由是_______ 。
(3)电催化还原CO2受到广泛的研究,一种原理如图所示:
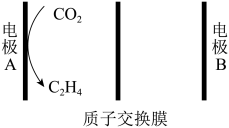
写出A电极发生的电极方程式:_______ 。若用铅蓄电池提供电能,则电极B连接铅蓄电池的_______ 极(填化学式)。
(1)以环己烷为原料通过芳构化反应生产苯,同时可获取氢气。图甲是该反应过程中几种物质间的能量关系。

芳构化反应:
 ΔH=
ΔH=(2)H2和CO2合成乙醇反应为: 2CO2(g)+6H2(g)⇌C2H5OH(g)+3H2O(g)。 将等物质的量的CO2和H2充入一刚性容器中,测得平衡时乙醇的体积分数随温度和压强的关系如图乙。

①压强P1
②已知Arrhenius经验公式为RInk=-
 +C(Ea为活化能,k为速率常数, R和C为常数),为探究m、n两种催化剂的储化效能,进行了实验探究,依据实验数获得图丙曲线。
+C(Ea为活化能,k为速率常数, R和C为常数),为探究m、n两种催化剂的储化效能,进行了实验探究,依据实验数获得图丙曲线。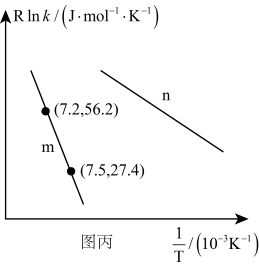
在m催化剂作用下,该反应的活化能Ea=
(3)电催化还原CO2受到广泛的研究,一种原理如图所示:

写出A电极发生的电极方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】党的二十大报告中强调“实现碳达峰碳中和是一场广泛而深刻的经济社会系统性变革”。
 的转化和利用是实现碳中和的有效途径。回答下列问题:
的转化和利用是实现碳中和的有效途径。回答下列问题:
Ⅰ.利用 合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
①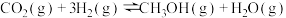
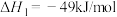
②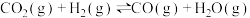
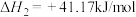
③

(1)反应③中活化能
__________ (填“>”或“<”)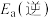 。
。
(2)在催化剂作用下,按 的比例向某密闭容器中通入一定量的原料气,只发生①②两个反应。维持压强为3.2MPa,测得不同温度下,反应经过相同时间时
的比例向某密闭容器中通入一定量的原料气,只发生①②两个反应。维持压强为3.2MPa,测得不同温度下,反应经过相同时间时 的转化率、甲醇的选择性如图所示:
的转化率、甲醇的选择性如图所示: 。
。
①从图中曲线的变化趋势分析a点之后温度升高,甲醇选择性降低的原因__________ ,在实际工业生产中压强不能过高也不能过低的原因是____________ 。
② 时,若反应在催化剂的活性范围内,反应从开始到达到a点所用时间为10min,则
时,若反应在催化剂的活性范围内,反应从开始到达到a点所用时间为10min,则 的分压=
的分压=__________ MPa,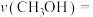
__________ MPa/min,反应②的
__________ ( 指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数×p总,最终结果用分数表示)。
指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数×p总,最终结果用分数表示)。
Ⅱ.近年来,有研究人员用 通过电催化生成多种燃料,实现
通过电催化生成多种燃料,实现 的回收利用,其工作原理如图所示:
的回收利用,其工作原理如图所示: ,则该电极反应式为
,则该电极反应式为____________________ 。

 的转化和利用是实现碳中和的有效途径。回答下列问题:
的转化和利用是实现碳中和的有效途径。回答下列问题:Ⅰ.利用
 合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:①
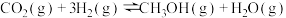
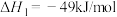
②
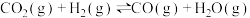
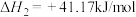
③


(1)反应③中活化能

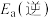 。
。(2)在催化剂作用下,按
 的比例向某密闭容器中通入一定量的原料气,只发生①②两个反应。维持压强为3.2MPa,测得不同温度下,反应经过相同时间时
的比例向某密闭容器中通入一定量的原料气,只发生①②两个反应。维持压强为3.2MPa,测得不同温度下,反应经过相同时间时 的转化率、甲醇的选择性如图所示:
的转化率、甲醇的选择性如图所示:
 。
。①从图中曲线的变化趋势分析a点之后温度升高,甲醇选择性降低的原因
②
 时,若反应在催化剂的活性范围内,反应从开始到达到a点所用时间为10min,则
时,若反应在催化剂的活性范围内,反应从开始到达到a点所用时间为10min,则 的分压=
的分压=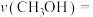

 指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数×p总,最终结果用分数表示)。
指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数×p总,最终结果用分数表示)。Ⅱ.近年来,有研究人员用
 通过电催化生成多种燃料,实现
通过电催化生成多种燃料,实现 的回收利用,其工作原理如图所示:
的回收利用,其工作原理如图所示: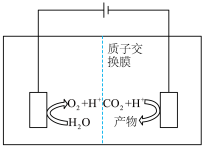
 ,则该电极反应式为
,则该电极反应式为
您最近一年使用:0次



