沉淀溶解平衡对于定量分离沉淀时如何选择洗涤剂具有指导作用。例如,现制得0.1g BaSO4沉淀,常温下如果用100 mL蒸馏水洗涤该沉淀以除掉杂质,将损失2.4×10-4 g BaSO4;如果改用100 mL0.01 mol/L硫酸洗涤该沉淀,仅损失2.6×10-7 g BaSO4,与用等体积的蒸馏水洗涤相比,BaSO4损失少得多。请解释原因____________________ 。
更新时间:2021-12-02 08:43:00
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】Ⅰ.请用相关术语回答下列问题:
(1)已知NaHA水溶液呈碱性。
①用离子方程式及文字表示NaHA水溶液呈碱性的原因__________________ 。
②在NaHA水溶液中各离子浓度的大小关系是______________ 。
(2)25℃时,向浓度均为0.1mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________ 沉淀(填化学式),生成该沉淀的离子方程式为__________________ 。已知25℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。
Ⅱ.已知二元酸H2A在水中存在以下电离:H2A=H++HA-,HA- H++A2-。试回答下列问题:
H++A2-。试回答下列问题:
(3)NaHA溶液呈________ (填“酸”、“碱”或“中”)性,理由是___________________ 。
(4)某温度下,向10mL、0.1mol/L NaHA溶液中加入0.1mol/L KOH溶液VmL至中性,此时溶液中以下关系一定正确的是_________ (填写字母)。
(1)已知NaHA水溶液呈碱性。
①用离子方程式及文字表示NaHA水溶液呈碱性的原因
②在NaHA水溶液中各离子浓度的大小关系是
(2)25℃时,向浓度均为0.1mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成
Ⅱ.已知二元酸H2A在水中存在以下电离:H2A=H++HA-,HA-
 H++A2-。试回答下列问题:
H++A2-。试回答下列问题:(3)NaHA溶液呈
(4)某温度下,向10mL、0.1mol/L NaHA溶液中加入0.1mol/L KOH溶液VmL至中性,此时溶液中以下关系一定正确的是
| A.溶液pH=7 | B.水的离子积Kw=[c2(OH-)] |
| C.V=10 | D.c(K+)<c(Na+) |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】弱电解质的电离平衡、盐类的水解平衡和难溶物的沉淀溶解平衡均属于化学平衡。
I.已知 在水中存在以下平衡:
在水中存在以下平衡: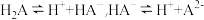 。
。
(1)常温下, 溶液的
溶液的
______ (填字母序号),原因是______ (填离子方程式)。
A.大于7 B.小于7 C.等于7 D.无法确定
(2)常温下,若向 的
的 溶液中逐滴滴加
溶液中逐滴滴加
 溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是
溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是______ (填字母序号)。
A.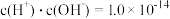 B.
B.
C.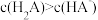 D.
D.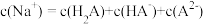
(3)常温下, 的饱和溶液中存在以下平衡:
的饱和溶液中存在以下平衡: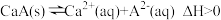 ,若要使该溶液中
,若要使该溶液中 浓度增大,可采取的措施有
浓度增大,可采取的措施有______ (填字母序号)。
A.升高温度 B.降低温度 C.加入少量蒸馏水 D.加入 固体
固体
Ⅱ.化学沉淀法是除去酸性废水中 的主要方法。根据其原理不同可以分为氢氧化物沉淀法、硫化物沉淀法等。水样中各形态铅的百分含量X与溶液
的主要方法。根据其原理不同可以分为氢氧化物沉淀法、硫化物沉淀法等。水样中各形态铅的百分含量X与溶液 变化的关系如图所示。向含
变化的关系如图所示。向含 的溶液中逐滴滴加
的溶液中逐滴滴加 溶液,溶液变浑浊,继续滴加
溶液,溶液变浑浊,继续滴加 溶液又变澄清。
溶液又变澄清。
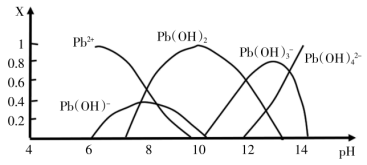
(4)若采用氢氧化物沉淀法除溶液中的 ,应将溶液的
,应将溶液的 调至约为
调至约为______ ; 时,溶液中发生的主要离子方程式为
时,溶液中发生的主要离子方程式为______ 。
(5)向酸性含铅废水中加 可将
可将 转化为
转化为 沉淀除去。若某工厂处理过的废水中
沉淀除去。若某工厂处理过的废水中 浓度为
浓度为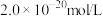 ,则
,则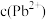 为
为______ 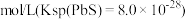 。
。
I.已知
 在水中存在以下平衡:
在水中存在以下平衡: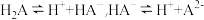 。
。(1)常温下,
 溶液的
溶液的
A.大于7 B.小于7 C.等于7 D.无法确定
(2)常温下,若向
 的
的 溶液中逐滴滴加
溶液中逐滴滴加
 溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是
溶液至溶液呈中性。此时该混合溶液中的下列关系一定正确的是A.
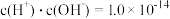 B.
B.
C.
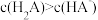 D.
D.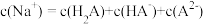
(3)常温下,
 的饱和溶液中存在以下平衡:
的饱和溶液中存在以下平衡: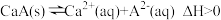 ,若要使该溶液中
,若要使该溶液中 浓度增大,可采取的措施有
浓度增大,可采取的措施有A.升高温度 B.降低温度 C.加入少量蒸馏水 D.加入
 固体
固体Ⅱ.化学沉淀法是除去酸性废水中
 的主要方法。根据其原理不同可以分为氢氧化物沉淀法、硫化物沉淀法等。水样中各形态铅的百分含量X与溶液
的主要方法。根据其原理不同可以分为氢氧化物沉淀法、硫化物沉淀法等。水样中各形态铅的百分含量X与溶液 变化的关系如图所示。向含
变化的关系如图所示。向含 的溶液中逐滴滴加
的溶液中逐滴滴加 溶液,溶液变浑浊,继续滴加
溶液,溶液变浑浊,继续滴加 溶液又变澄清。
溶液又变澄清。
(4)若采用氢氧化物沉淀法除溶液中的
 ,应将溶液的
,应将溶液的 调至约为
调至约为 时,溶液中发生的主要离子方程式为
时,溶液中发生的主要离子方程式为(5)向酸性含铅废水中加
 可将
可将 转化为
转化为 沉淀除去。若某工厂处理过的废水中
沉淀除去。若某工厂处理过的废水中 浓度为
浓度为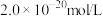 ,则
,则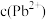 为
为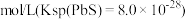 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】现有25℃时,0.1 mol/L的氨水。请回答下列问题:
(1)若向0.1 mol·L-1氨水中加入少量硫酸铵固体,此时溶液中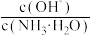
____ (填“增大”“减小”或“不变”)。
(2)若向0.1mol·L-1氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=a mol·L-1,则
c(SO42-)=_____________ 。
(3)若向0.1 mol·L-1氨水中加入pH=1的硫酸,且氨水与硫酸的体积比1:1,则所得溶液中各离子物质的量浓度由大到小的顺序是______________ 。
(4)将足量的AgCl固体分别放入: ①5mL水,②10mL 0.2mol·L-1MgCl2溶液,③20mL 0.5 mol·L-1 NaCI溶液,④40mL 0.1mol·L-1盐酸中溶解至溶液饱和,各溶液中Ag+的物质的量浓度分别为a、b、c、d,它们由大到小的排列顺序是______________ 。
(1)若向0.1 mol·L-1氨水中加入少量硫酸铵固体,此时溶液中
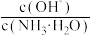
(2)若向0.1mol·L-1氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=a mol·L-1,则
c(SO42-)=
(3)若向0.1 mol·L-1氨水中加入pH=1的硫酸,且氨水与硫酸的体积比1:1,则所得溶液中各离子物质的量浓度由大到小的顺序是
(4)将足量的AgCl固体分别放入: ①5mL水,②10mL 0.2mol·L-1MgCl2溶液,③20mL 0.5 mol·L-1 NaCI溶液,④40mL 0.1mol·L-1盐酸中溶解至溶液饱和,各溶液中Ag+的物质的量浓度分别为a、b、c、d,它们由大到小的排列顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】 与溶解度
与溶解度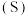 都可用来表示物质的溶解能力,
都可用来表示物质的溶解能力, 小的物质的溶解度是否一定也小
小的物质的溶解度是否一定也小_______ 。
 与溶解度
与溶解度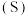 都可用来表示物质的溶解能力,
都可用来表示物质的溶解能力, 小的物质的溶解度是否一定也小
小的物质的溶解度是否一定也小
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】用沉淀法除杂能否将杂质离子全部通过沉淀除去________ ?
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】写出下列反应的离子方程式。
(1)向Na2S2O3溶液中加入稀硫酸_____________________________________________________________
(2)在Mg(OH)2悬浊液中加入FeCl3溶液,沉淀变为红褐色____________________________________
(3)Mg(OH)2沉淀溶于NH4Cl溶液中______________________________________________________
(1)向Na2S2O3溶液中加入稀硫酸
(2)在Mg(OH)2悬浊液中加入FeCl3溶液,沉淀变为红褐色
(3)Mg(OH)2沉淀溶于NH4Cl溶液中
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】沉淀的转化
(1)【实验探究】沉淀的转化实验
实验结论:_______ 。
(2)沉淀转化的实质就是_______ 的移动,一般而言,溶解能力相对较强的物质容易转化为溶解能力较弱的物质。
(3)两种沉淀的溶解度差别越大,沉淀转化越_______ 。
(4)沉淀转化的应用实例
①锅炉形成的水垢中常含有CaSO4,除去方法是CaSO4(s)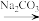 CaCO3(s)
CaCO3(s)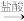 Ca2+(aq)。化学方程为:
Ca2+(aq)。化学方程为:_______ ,_______ 。
②在分析化学中常用饱和Na2CO3溶液,将难溶强酸盐BaSO4转化为难溶弱酸盐BaCO3,然后用强酸溶解,使阳离子进入溶液。BaSO4转化为BaCO3反应的离子方程式为:_______ 。
③除去CuSO4溶液中的Fe3+,向溶液中加入_______ 或_______ ,调节pH至_______ ,Fe3+会全部转化为Fe(OH)3沉淀除去。
(1)【实验探究】沉淀的转化实验
| 实验现象 | 离子方程式 | |
| 实验1 | ||
| 实验2 | ||
| 实验3 |
(2)沉淀转化的实质就是
(3)两种沉淀的溶解度差别越大,沉淀转化越
(4)沉淀转化的应用实例
①锅炉形成的水垢中常含有CaSO4,除去方法是CaSO4(s)
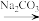 CaCO3(s)
CaCO3(s)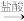 Ca2+(aq)。化学方程为:
Ca2+(aq)。化学方程为:②在分析化学中常用饱和Na2CO3溶液,将难溶强酸盐BaSO4转化为难溶弱酸盐BaCO3,然后用强酸溶解,使阳离子进入溶液。BaSO4转化为BaCO3反应的离子方程式为:
③除去CuSO4溶液中的Fe3+,向溶液中加入
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知常温下,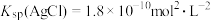 ,
,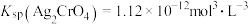 。向含有
。向含有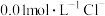 和
和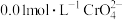 的混合溶液中逐滴加入
的混合溶液中逐滴加入 溶液(忽略溶液体积变化),判断先析出的物质是
溶液(忽略溶液体积变化),判断先析出的物质是________ (写化学式)。
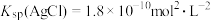 ,
,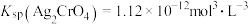 。向含有
。向含有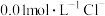 和
和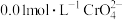 的混合溶液中逐滴加入
的混合溶液中逐滴加入 溶液(忽略溶液体积变化),判断先析出的物质是
溶液(忽略溶液体积变化),判断先析出的物质是
您最近一年使用:0次



