请解释钾与钠产生焰色及焰色不同的原因___________ 。
更新时间:2021-12-03 09:07:47
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】下表为元素周期表的短周期部分,请参照元素①~⑧在表中的位置,用化学用语回答下列题:
(1)半径最小的元素是______________ ,金属性最强的元素是____________ ;(填元素符号)
(2)⑤和⑧两元素可形成化合物,灼烧该化合物时火焰颜色为___________ 色;
(3)元素⑧在周期表中的位置是__________________________ ;
(4)①和③两元素形成的化合物的电子式为__________________ ;
(5)①分别与②、③、④形成的化合物中,最稳定是(填写化学式)______________________ ;
(6)④、⑤、⑥三种元素形成的简单离子中,离子半径最大的是(填离子符号)__________________ ;
(7)②、③的最高价含氧酸的酸性强弱比较(用化学式表示)_____________________________ 。
① | |||||||
② | ③ | ④ | |||||
⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)半径最小的元素是
(2)⑤和⑧两元素可形成化合物,灼烧该化合物时火焰颜色为
(3)元素⑧在周期表中的位置是
(4)①和③两元素形成的化合物的电子式为
(5)①分别与②、③、④形成的化合物中,最稳定是(填写化学式)
(6)④、⑤、⑥三种元素形成的简单离子中,离子半径最大的是(填离子符号)
(7)②、③的最高价含氧酸的酸性强弱比较(用化学式表示)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)为了证明某NaCl样品中含有钠元素,可以采用的实验方法是利用__________ 反应,操作方法是使用带有铂丝的玻璃棒蘸取待测样品放到酒精灯上灼烧,观察火焰呈_________ 色。若再需检验某样品中是否含钾元素,则要先将该铂丝用________ 洗净后反复灼烧至无色再蘸取待测样品,此时观察火焰颜色需要透过_________________ 。
(2)合金具有很多优良性能,例如,合金的硬度一般_________ 组分金属,而熔点_______ 组分金属。铜的合金主要有__________ 、___________ 、白铜等。铁的合金之一----钢可分为__________ 和________ 两大类。
(2)合金具有很多优良性能,例如,合金的硬度一般
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】完成下列问题:
(1)现有下列十种物质:①铜; ②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥氢氧化钾⑦氢氧化铁胶体;⑧盐酸;⑨乙醇;⑩硫酸铁。
上述十种物质中,属于混合物的是___________ (填序号),②的电离方程式为___________ 。
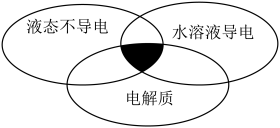
(2)下列物质属于如图所示化学概念交叉部分(阴影部分)的是___________ 。
A. B.
B. C.
C. (乙醇) D.
(乙醇) D. E.
E.
(3)观察⑥氢氧化钾的焰色试验的火焰颜色的操作及现象是___________ 。
(4)高铁酸钠 是一种新型绿色消毒剂
是一种新型绿色消毒剂
①其中一种制备 的离子方程式可表示为:
的离子方程式可表示为: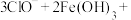 ___________
___________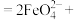 ___________+___________
___________+___________ ,请补全以上反应,并用双线桥法表示电子转移的方向和数目
,请补全以上反应,并用双线桥法表示电子转移的方向和数目___________ 。
②已知: 在处理饮用水的过程中铁元素会被转化为
在处理饮用水的过程中铁元素会被转化为 ,进而
,进而 在水中产生
在水中产生 胶体,
胶体, 胶体为
胶体为___________ 色,写出区分胶体与溶液的实验方法名称:___________ 。检验含 的溶液中是否含有
的溶液中是否含有 的试剂是
的试剂是___________ (化学式),反应的离子方程式为___________ 。
(1)现有下列十种物质:①铜; ②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥氢氧化钾⑦氢氧化铁胶体;⑧盐酸;⑨乙醇;⑩硫酸铁。
上述十种物质中,属于混合物的是
(2)下列物质属于如图所示化学概念交叉部分(阴影部分)的是

A.
 B.
B. C.
C. (乙醇) D.
(乙醇) D. E.
E.
(3)观察⑥氢氧化钾的焰色试验的火焰颜色的操作及现象是
(4)高铁酸钠
 是一种新型绿色消毒剂
是一种新型绿色消毒剂①其中一种制备
 的离子方程式可表示为:
的离子方程式可表示为: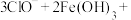 ___________
___________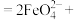 ___________+___________
___________+___________ ,请补全以上反应,并用双线桥法表示电子转移的方向和数目
,请补全以上反应,并用双线桥法表示电子转移的方向和数目②已知:
 在处理饮用水的过程中铁元素会被转化为
在处理饮用水的过程中铁元素会被转化为 ,进而
,进而 在水中产生
在水中产生 胶体,
胶体, 胶体为
胶体为 的溶液中是否含有
的溶液中是否含有 的试剂是
的试剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】许多金属及其化合物在生活、化工、医药、材料等各个领域有着广泛的应用。
(1)钛美誉为“未来钢铁”“战略金属”。基态钛原子中电子占据最高能级的符号为____ 。
(2)镓在周期表中的位置____ 。
(3)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因是____ 。
(4)下列Li原子电子排布图表示的状态中,能量最高的为____ (填字母)。
A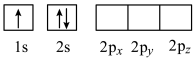 . B.
. B. 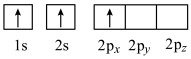 C.
C.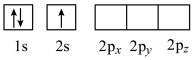
(5)Li+与H-具有相同的电子层结构,r(Li+)小于r(H-),原因是____ 。
(1)钛美誉为“未来钢铁”“战略金属”。基态钛原子中电子占据最高能级的符号为
(2)镓在周期表中的位置
(3)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因是
(4)下列Li原子电子排布图表示的状态中,能量最高的为
A
 . B.
. B.  C.
C.
(5)Li+与H-具有相同的电子层结构,r(Li+)小于r(H-),原因是
您最近一年使用:0次
【推荐2】按要求填空。
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是_______(填标号)。
(2)基态Fe原子中,电子占据的最高能层的符号为_______ ,该能层具有的原子轨道数为_______ 。
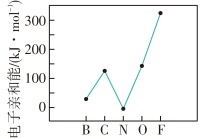
(3)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能( )。第二周期部分元素的
)。第二周期部分元素的 变化趋势如图所示,其中除氮元素外,其他元素的
变化趋势如图所示,其中除氮元素外,其他元素的 自左而右依次增大。而氮元素的
自左而右依次增大。而氮元素的 呈现异常的原因是
呈现异常的原因是_______ 。
(4) 是离子化合物,下图是Born−Haber循环。
是离子化合物,下图是Born−Haber循环。
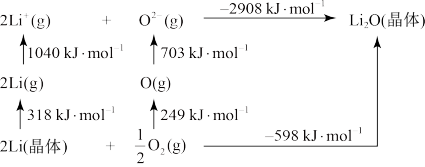
可知,Li原子的第一电离能为_______  ,O=O键键能为
,O=O键键能为_______  。
。
(5)下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据:
下列说法正确的是_______(填字母)。
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是_______(填标号)。
A. | B. | C.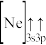 | D. |
(3)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(
 )。第二周期部分元素的
)。第二周期部分元素的 变化趋势如图所示,其中除氮元素外,其他元素的
变化趋势如图所示,其中除氮元素外,其他元素的 自左而右依次增大。而氮元素的
自左而右依次增大。而氮元素的 呈现异常的原因是
呈现异常的原因是
(4)
 是离子化合物,下图是Born−Haber循环。
是离子化合物,下图是Born−Haber循环。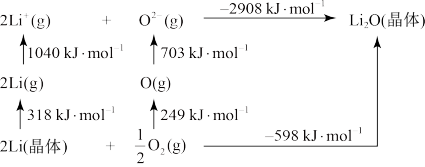
可知,Li原子的第一电离能为
 ,O=O键键能为
,O=O键键能为 。
。(5)下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据:
| 元素 | 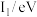 | 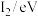 | 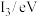 |
| 甲 | 5.7 | 47.1 | 71.8 |
| 乙 | 7.7 | 15.1 | 80.3 |
| 丙 | 13.0 | 23.9 | 40.0 |
| 丁 | 15.7 | 27.6 | 40.7 |
| A.甲的金属性比乙强 | B.乙的化合价为 价 价 |
| C.丙不可能为非金属元素 | D.丁一定为金属元素 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】光谱分析
通过原子发射光谱或吸收光谱___________ 元素,称为光谱分析。
通过原子发射光谱或吸收光谱
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】如图是锂、氦、汞原子的吸收光谱和发射光谱。其中图______ 是原子由基态转化为激发态时的光谱,图______ 是原子由激发态转化为基态时的光谱。不同元素的原子光谱上的特征谱线不同,请在图中将同种元素原子的吸收光谱和发射光谱连接起来______ 。
① ②
②
③ ④
④
⑤ ⑥
⑥
①
 ②
②
③
 ④
④
⑤
 ⑥
⑥
您最近一年使用:0次
【推荐3】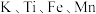 均为第四周期金属元素,它们的单质及化合物在诸多领域都有广泛的应用。回答下列问题:
均为第四周期金属元素,它们的单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钾在火焰上灼烧的紫光是一种_______ (填“吸收”或“发射”)光谱。
(2) 原子位于元素周期表中的
原子位于元素周期表中的_______ 区,基态 最高能层电子的电子云轮廓图为
最高能层电子的电子云轮廓图为_______ 形,其价电子排布式为_______ 。与 同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为_______ 。
(3)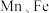 均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
锰元素位于第四周期第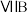 族。比较两元素的
族。比较两元素的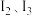 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,原因是
再失去1个电子难,原因是_______ 。
(4)琥珀酸亚铁片是用于预防和治疗缺铁性贫血的常见药物,临床建议服用维生素C促进亚铁的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是_______ 。
(5) 与
与 的半径大小关系为
的半径大小关系为
_______ (填“大于”或“小于”) 。
。
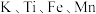 均为第四周期金属元素,它们的单质及化合物在诸多领域都有广泛的应用。回答下列问题:
均为第四周期金属元素,它们的单质及化合物在诸多领域都有广泛的应用。回答下列问题:(1)钾在火焰上灼烧的紫光是一种
(2)
 原子位于元素周期表中的
原子位于元素周期表中的 最高能层电子的电子云轮廓图为
最高能层电子的电子云轮廓图为 同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为
同周期的过渡元素中,未成对电子数最多的基态原子的价电子排布图为(3)
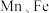 均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:| 元素 |  |  | |
电离能/ |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
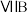 族。比较两元素的
族。比较两元素的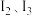 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,原因是
再失去1个电子难,原因是(4)琥珀酸亚铁片是用于预防和治疗缺铁性贫血的常见药物,临床建议服用维生素C促进亚铁的吸收,避免生成
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是(5)
 与
与 的半径大小关系为
的半径大小关系为
 。
。
您最近一年使用:0次



