许多金属及其化合物在生活、化工、医药、材料等各个领域有着广泛的应用。
(1)钛美誉为“未来钢铁”“战略金属”。基态钛原子中电子占据最高能级的符号为____ 。
(2)镓在周期表中的位置____ 。
(3)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因是____ 。
(4)下列Li原子电子排布图表示的状态中,能量最高的为____ (填字母)。
A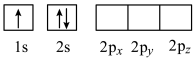 . B.
. B. 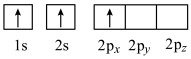 C.
C.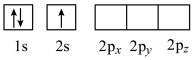
(5)Li+与H-具有相同的电子层结构,r(Li+)小于r(H-),原因是____ 。
(1)钛美誉为“未来钢铁”“战略金属”。基态钛原子中电子占据最高能级的符号为
(2)镓在周期表中的位置
(3)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因是
(4)下列Li原子电子排布图表示的状态中,能量最高的为
A
 . B.
. B.  C.
C.
(5)Li+与H-具有相同的电子层结构,r(Li+)小于r(H-),原因是
更新时间:2022-06-30 21:57:36
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
(1)②的最高价氧化物的分子式为_______ ;⑦的最高价氧化物对应水化物的分子式为_______ 。
(2)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:_______ 。
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是_______(填字母)。
(4)已知Cs元素位于元素周期表中第六周期第IA族,请回答下列问题:
①铯的原子序数为_______ 。
②铯单质与 反应的化学反应方程式为
反应的化学反应方程式为_______ 。
③预测铯单质的还原性比钠单质的还原性_______ (填“弱”或“强”)。
④下列推断正确的是_______ (填字母)。
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为_______ 。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(3)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是_______(填字母)。
| A.在化合物中最高正化合价为+6 | B.单质可以与 气体反应并置换出单质S 气体反应并置换出单质S |
| C.最高价氧化物对应水化物的酸性比硫酸弱 | D.单质在常温下可与氢气化合 |
①铯的原子序数为
②铯单质与
 反应的化学反应方程式为
反应的化学反应方程式为③预测铯单质的还原性比钠单质的还原性
④下列推断正确的是
A.与铯处于同一主族的元素都是金属元素
B.铯单质发生反应时,铯原子易失去电子
C.碳酸铯是一种可溶性碱
D.铯离子的氧化性强于钾离子
(5)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
【推荐2】元素周期表中锑元素的数据如图。

(1)根据锑的价层电子排布式5s25p3可知,锑在元素周期表中位于第___________ 周期,第___________ 族。
(2)基态锑原子中有___________ 个未成对电子,这些未成对电子具有___________ (填“相同”或“不同”)的自旋状态。
(3)基态锑原子的5s轨道形状为___________ 形,该原子最外层电子占有___________ 个轨道。
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。则两种元素的电负性Sb___________ Bi;原子半径Sb___________ Bi (填“>”或“<”)。

(1)根据锑的价层电子排布式5s25p3可知,锑在元素周期表中位于第
(2)基态锑原子中有
(3)基态锑原子的5s轨道形状为
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。则两种元素的电负性Sb
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】纯净物A、B、C、D、E均是中学常见的物质。其转化关系如图所示(图中某些生成物已略去),物质A与物质B之间的反应不在溶液中进行,通常状况下D为气体

请回答下列问题:
(1)若A、B、D均为短周期元素的单质,C为化合物且气体D就是物质B,又知D气体不可燃,则B的分子式是_______ ,化合物E的化学式为________ 。
(2)若A、C、D均为短周期元素的单质,B、E为氧化物,且化合物E通常状况下为气体,在一定条件下E还可以和氧气发生反应。则A位于在周期表中的________ 周期______ 族。A和B反应生成C的化学方程式是______ 。

请回答下列问题:
(1)若A、B、D均为短周期元素的单质,C为化合物且气体D就是物质B,又知D气体不可燃,则B的分子式是
(2)若A、C、D均为短周期元素的单质,B、E为氧化物,且化合物E通常状况下为气体,在一定条件下E还可以和氧气发生反应。则A位于在周期表中的
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)第四周期中,未成对电子数最多的元素是________ ,(填名称)它位于第________ 族;核外电子排布式是__________________ 。它有________ 种运动状态不同的电子,其价电子排布图为:______________ 。
(2)已知NH5为离子化合物,写出其电子式:________ 。
(3)某同学根据掌握的知识分析Mg的核外电子排布为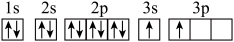 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了________ 。
(4)在基态14C原子中,核外存在________ 对自旋相反的电子。
(2)已知NH5为离子化合物,写出其电子式:
(3)某同学根据掌握的知识分析Mg的核外电子排布为
 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了(4)在基态14C原子中,核外存在
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】能量最低原理
原子的电子排布遵循_______ 能使整个原子的能量处于_______ 状态,简称能量最低原理。
原子的电子排布遵循
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】基态Fe原子价层电子的电子排布图(轨道表达式)为__ ,基态S原子电子占据最高能级的电子云轮廓图为__ 形。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】有几种元素的粒子核外电子排布式均为1s22s22p63s23p6,其中:
(1)某电中性微粒一般不和其他元素的原子反应,这种微粒的符号是___________ ;
(2)某微粒的盐溶液,能使溴水褪色,并出现浑浊,这种微粒的符号是___________ ;
(3)某微粒氧化性很弱,但得到电子后还原性很强,且这种原子有一个单电子,这种微粒的符号是___________ ;
(4)某微粒还原性虽弱,但失去电子后氧化性强,且这种元素的原子得到一个电子即达稳定结构,这种微粒的符号是___________ 。
(1)某电中性微粒一般不和其他元素的原子反应,这种微粒的符号是
(2)某微粒的盐溶液,能使溴水褪色,并出现浑浊,这种微粒的符号是
(3)某微粒氧化性很弱,但得到电子后还原性很强,且这种原子有一个单电子,这种微粒的符号是
(4)某微粒还原性虽弱,但失去电子后氧化性强,且这种元素的原子得到一个电子即达稳定结构,这种微粒的符号是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)基态Mn原子核外未成对电子有_______ 个。
(2)基态镁原子核外M层电子的自旋状态_______ (填“相同”或“相反”)。
(3)基态Ge原子有_______ 个未成对电子。
(4)镍元素基态原子的电子排布式为_______ ,3d能级上的未成对的电子数为_______ 。
(5)氮原子价层电子的轨道表达式(电子排布图)为_______ 。
(6)基态Fe原子价层电子的电子排布图(轨道表达式)为_______ ,基态S原子电子占据最高能级的电子云轮廓图为_______ 形。
(7)基态K原子中,核外电子占据的最高能层的符号是_______ ,占据该能层电子的电子云轮廓图形状为_______ 。
(8)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_______、_______(填标号)。
(9)下列基态原子或离子的价层电子排布图正确的是_______。
(1)基态Mn原子核外未成对电子有
(2)基态镁原子核外M层电子的自旋状态
(3)基态Ge原子有
(4)镍元素基态原子的电子排布式为
(5)氮原子价层电子的轨道表达式(电子排布图)为
(6)基态Fe原子价层电子的电子排布图(轨道表达式)为
(7)基态K原子中,核外电子占据的最高能层的符号是
(8)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_______、_______(填标号)。
A. | B. |
C.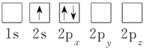 | D.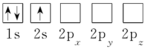 |
A.Fe2+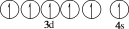 |
B.Cu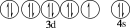 |
C.Fe3+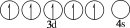 |
D.Cu+ |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】请填空:
(1)亚铁氰化钾(K4[Fe(CN)6])俗称黄血盐,是一种重要的化工原料。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝)+3KCl,回答问题:
①K4[Fe(CN)6]中的作用力除C、N原子间的共价键外,还有___________ 和___________ 。
②C、N、O的电负性由大到小的排序为___________ 。
(2)新型储氢材料是开发利用氢能的研究方向,Ti(BH4)3是一种储氢材料,可由LiBH4和TiCl4反应制得。
①基态Cl原子有___________ 种空间运动状态的电子,属于___________ 区(填“s”或“p”或“d”或“f”)
②LiBH4由Li+和BH 构成,与BH
构成,与BH 互为等电子体的分子为
互为等电子体的分子为___________ ,Li、Be、B元素的第一电离能由大到小排列顺序为___________ 。
③某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是___________ (填元素符号)。
(3)下列状态的镁中,电离最外层一个电子所需能量最大的是___________ (填标号)。
A.[Ne]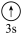 B.[Ne]
B.[Ne] 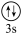 C.[Ne]
C.[Ne] 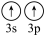 D.[Ne]
D.[Ne] 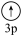
(1)亚铁氰化钾(K4[Fe(CN)6])俗称黄血盐,是一种重要的化工原料。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝)+3KCl,回答问题:
①K4[Fe(CN)6]中的作用力除C、N原子间的共价键外,还有
②C、N、O的电负性由大到小的排序为
(2)新型储氢材料是开发利用氢能的研究方向,Ti(BH4)3是一种储氢材料,可由LiBH4和TiCl4反应制得。
①基态Cl原子有
②LiBH4由Li+和BH
 构成,与BH
构成,与BH 互为等电子体的分子为
互为等电子体的分子为③某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 |
| 580 | 1820 | 2750 | 11600 |
(3)下列状态的镁中,电离最外层一个电子所需能量最大的是
A.[Ne]
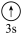 B.[Ne]
B.[Ne] 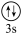 C.[Ne]
C.[Ne]  D.[Ne]
D.[Ne] 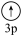
您最近一年使用:0次

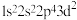 c.1s22s12p5 d.
c.1s22s12p5 d.


