在二氧化碳合成甲醇的研究中,催化剂是研究的关键。目前国内外研究主要集中于铜基催化剂,有学者提出了如图CO2的转化过程。下列说法错误的是
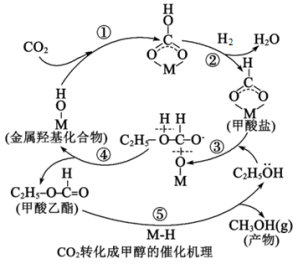

| A.铜元素位于周期表中的ds区 |
| B.步骤④中有化学键的断裂和形成 |
| C.甲酸乙酯是该过程的催化剂 |
D.总反应化学方程式为CO2+3H2 CH3OH+H2O CH3OH+H2O |
21-22高三上·湖北·阶段练习 查看更多[6]
湖北省十一校2021-2022学年高三上学期第一次联考(12月)化学试题(已下线)第十一单元 物质结构与性质(A卷 新题基础练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)(已下线)专题09 反应机理—2022年高考化学二轮复习讲练测(全国版)-测试(已下线)一轮巩固卷4-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(湖北专用)福建省南平高级中学2021-2022学年高三上学期12月月考化学试题四川省内江市第六中学2022-2023学年高二下学期入学考试化学试题
更新时间:2021-12-10 10:46:21
|
相似题推荐
【推荐1】煤可以直接液化,也可以间接液化。间接液化是将煤先转化为一氧化碳和氢气,再在催化剂作用下合成甲醇。已知CO(g)+2H2(g) CH3OH(g)过程中能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是
CH3OH(g)过程中能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是

 CH3OH(g)过程中能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是
CH3OH(g)过程中能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是
| A.该反应的△H=+91kJ•mol-1 |
| B.由于曲线Ⅱ的反应实际分两步进行,因此其反应速率比曲线Ⅰ的反应速率小 |
| C.如果该反应生成液态CH3OH,则△H增大 |
| D.煤的直接液化与上述工艺不同,其是将煤与氢气直接作用生成液体燃料 |
您最近一年使用:0次
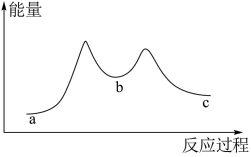
【推荐2】一定温度下,向一容积为2L的恒容密闭容器中充入2molA与3molB,在一定条件下反应:A(g)+B(g) C(g),△H>0,达到平衡后容器内压强是开始时的84%。若加入某种催化剂后反应的能量变化如图所示。下列说法正确的是( )
C(g),△H>0,达到平衡后容器内压强是开始时的84%。若加入某种催化剂后反应的能量变化如图所示。下列说法正确的是( )
 C(g),△H>0,达到平衡后容器内压强是开始时的84%。若加入某种催化剂后反应的能量变化如图所示。下列说法正确的是( )
C(g),△H>0,达到平衡后容器内压强是开始时的84%。若加入某种催化剂后反应的能量变化如图所示。下列说法正确的是( )
| A.由图可知,加入催化剂之后,原反应分成了两步第二步反应较慢 |
| B.若40s后达到平衡,则用A表示该反应的速率为0.01mol・L-1・min-1 |
C.当容器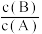 不再改变时,不能说明该反应达到了平衡状态 不再改变时,不能说明该反应达到了平衡状态 |
| D.达到平衡时,C的体积分数约为25% |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关化学键的说法错误的是
| A.化学键可以使离子结合,也可以使原子结合 | B. 分子中仅含有极性共价键 分子中仅含有极性共价键 |
C. 中既有离子键又有共价键 中既有离子键又有共价键 | D.有化学键断裂的过程不一定发生了化学变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列两种物质在变化过程中克服的作用力相同的是
| A.食盐、氯化氢溶于水 | B.固体碘、氯化铵受热产生气体 |
| C.液溴、酒精挥发 | D.生石灰、浓硫酸干燥吸水 |
您最近一年使用:0次
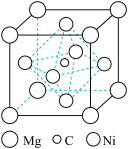
【推荐1】已知:由镍、镁、碳三种元素组成的一种物质,晶胞如图所示,其中面心上的镍原子构成正八面体,正八面体的边长为 ,设
,设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 ,设
,设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
A. 的价层电子排布式为 的价层电子排布式为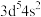 |
B.该物质可表示为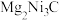 |
C.该晶体的摩尔体积为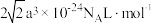 |
D.处于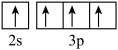 状态的 状态的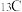 原子跃迁到基态时产生吸收光谱 原子跃迁到基态时产生吸收光谱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】氧化基纳米催化剂可用于CO2选择性加氢制备CH3OH,其反应机理如图所示,下列说法错误的是

| A.In为49号元素,其价层电子排布式为6s26p1 |
| B.该反应过程中存在极性键的断裂和形成 |
| C.CH3OH和CO2中,碳原子的杂化方式不同 |
D.该反应的总化学方程式为 |
您最近一年使用:0次


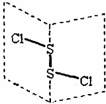
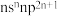 ,则该元素在周期表中的位置为
,则该元素在周期表中的位置为

