硫酸四氨合铜(Ⅱ)晶体[Cu(NH3)4]SO4·H2O(M=246g⋅mol-1)易溶于水,不溶于乙醇,常用作杀虫剂和媒染剂。以废铜(表面有油污)为原料制备[Cu(NH3)4]SO4·H2O,实验步骤如下:
I. CuSO4·5H2O

(1)步骤①中的“碱”是指一种钠盐,写出该物质的化学式___________ 。
(2)步骤②中铜溶解的离子方程式为___________ 。
(3)为加快过滤速度,使用的仪器是___________ (从“a”或“b”中选择)。
II.制备[Cu(NH3)4]SO4·H2O,实验装置图1所示。
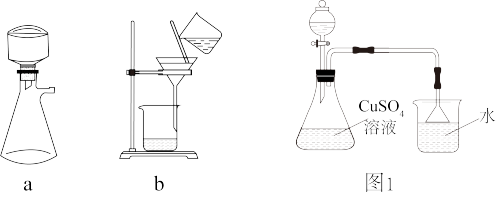
(4)用浓氨水调节硫酸铜浓溶液pH为10,有大量的浅蓝色沉淀出现;持续加入浓氨水,当蓝色沉淀完全消失后,加入乙醇,静置,过滤得到产品。
①将滤液用稀硫酸酸化后,___________ (填操作名称),可回收乙醇。
②可以使用下列哪种试剂代替乙醇来促进晶体析出:___________ 。(填标号)
a.浓H2SO4 b.稀氨水 c. Na2SO4固体 d.饱和NaCl溶液
(5)称取[Cu(NH3)4]SO4·H2O试样m1 g,用稀盐酸和BaCl2溶液处理后,获得m2 g洁净的沉淀,试样中[Cu(NH3)4]SO4·H2O的质量分数为___________ 。(列出计算式)
Ⅲ.检验[Cu(NH3)4]SO4·H2O的性质
(6)向饱和[Cu(NH3)4]SO4溶液中滴加少量0.1mol·L-1稀硫酸,溶液中立刻出现大量浅蓝色沉淀,经检验发现该沉淀为Cu2(OH)2SO4,写出生成Cu2(OH)2SO4沉淀的离子反应方程式:_______ 。
I. CuSO4·5H2O

(1)步骤①中的“碱”是指一种钠盐,写出该物质的化学式
(2)步骤②中铜溶解的离子方程式为
(3)为加快过滤速度,使用的仪器是
II.制备[Cu(NH3)4]SO4·H2O,实验装置图1所示。

(4)用浓氨水调节硫酸铜浓溶液pH为10,有大量的浅蓝色沉淀出现;持续加入浓氨水,当蓝色沉淀完全消失后,加入乙醇,静置,过滤得到产品。
①将滤液用稀硫酸酸化后,
②可以使用下列哪种试剂代替乙醇来促进晶体析出:
a.浓H2SO4 b.稀氨水 c. Na2SO4固体 d.饱和NaCl溶液
(5)称取[Cu(NH3)4]SO4·H2O试样m1 g,用稀盐酸和BaCl2溶液处理后,获得m2 g洁净的沉淀,试样中[Cu(NH3)4]SO4·H2O的质量分数为
Ⅲ.检验[Cu(NH3)4]SO4·H2O的性质
(6)向饱和[Cu(NH3)4]SO4溶液中滴加少量0.1mol·L-1稀硫酸,溶液中立刻出现大量浅蓝色沉淀,经检验发现该沉淀为Cu2(OH)2SO4,写出生成Cu2(OH)2SO4沉淀的离子反应方程式:
21-22高三·广东·阶段练习 查看更多[2]
更新时间:2021-12-13 18:27:44
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】明朝宋应星所著的《天工开物》中记载了世界上最早的炼锌技术:“罐中炉甘石熔化成团,冷定毁罐取出。每十耗其二,即倭铅也。”这里炉甘石即菱锌矿(含 ,其余为
,其余为 和
和 杂质)。硒化锌是一种半导体材料,以菱锌矿为原料制备硒化锌的流程如下:
杂质)。硒化锌是一种半导体材料,以菱锌矿为原料制备硒化锌的流程如下:
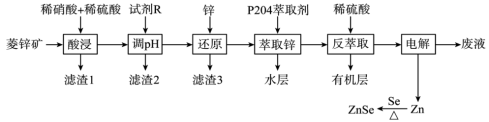
已知部分信息如下:
①常温下,几种离子形成氢氧化物的 如表所示。
如表所示。
②锌的性质和铝、铜相似,如 是两性氢氧化物,
是两性氢氧化物, 溶于氨水形成
溶于氨水形成 。回答下列问题:
。回答下列问题:
(1)为增大“酸浸”速率,可采取的措施是________ (填一条即可),“酸浸”中溶解 的离子方程式为
的离子方程式为___________ 。
(2)“滤渣1”的主要成分为________ (填化学式)。
(3)常温下,“调 ”的范围为
”的范围为________ 。
(4)“反萃取”中稀硫酸的主要作用是_________ 。
(5)“电解”中以石墨为电极,阳极的电极反应式为________ ,废液可以循环用于______ (填名称)工序。
(6)合成 宜在氩气氛围中进行,氩气的作用是
宜在氩气氛围中进行,氩气的作用是________ 。
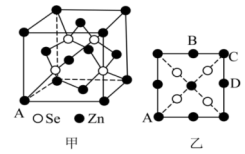
(7)硒化锌( )晶胞结构如图甲所示,乙图为甲图的俯视图,若A点坐标为
)晶胞结构如图甲所示,乙图为甲图的俯视图,若A点坐标为 ,B点坐标为
,B点坐标为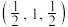 ,
, 点坐标为
点坐标为_______ 。在晶胞中距离 最近且等距离的
最近且等距离的 组成的空间结构为
组成的空间结构为_______ 形。
 ,其余为
,其余为 和
和 杂质)。硒化锌是一种半导体材料,以菱锌矿为原料制备硒化锌的流程如下:
杂质)。硒化锌是一种半导体材料,以菱锌矿为原料制备硒化锌的流程如下:
已知部分信息如下:
①常温下,几种离子形成氢氧化物的
 如表所示。
如表所示。| 金属离子 |  |  |  |  |  |
开始沉淀的 | 1.9 | 7.0 | 6.0 | 6.2 | 8.8 |
完全沉淀的 | 3.2 | 9.0 | 8.0 | 8.2 | 10.9 |
 是两性氢氧化物,
是两性氢氧化物, 溶于氨水形成
溶于氨水形成 。回答下列问题:
。回答下列问题:(1)为增大“酸浸”速率,可采取的措施是
 的离子方程式为
的离子方程式为(2)“滤渣1”的主要成分为
(3)常温下,“调
 ”的范围为
”的范围为(4)“反萃取”中稀硫酸的主要作用是
(5)“电解”中以石墨为电极,阳极的电极反应式为
(6)合成
 宜在氩气氛围中进行,氩气的作用是
宜在氩气氛围中进行,氩气的作用是(7)硒化锌(
 )晶胞结构如图甲所示,乙图为甲图的俯视图,若A点坐标为
)晶胞结构如图甲所示,乙图为甲图的俯视图,若A点坐标为 ,B点坐标为
,B点坐标为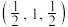 ,
, 点坐标为
点坐标为 最近且等距离的
最近且等距离的 组成的空间结构为
组成的空间结构为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】羟基自由基(·OH,电中性,O 为-1 价)是一种活性含氧微粒。常温下,利用·OH 处理含苯酚废水,可将其转化为无毒的氧化物。
(1)·OH 的电子式为________ 。
(2) pH=3 时 Fe2+催化 H2O2 的分解过程中产生·OH 中间体,催化循环反应如下。将方程式 ii 补充完整。
i.Fe2++ H2O2+H+ = Fe3++ H2O +·OH
ii.___ + ___ = ___ + O2↑+2H+
(3)已知:羟基自由基容易发生猝灭 2·OH = H2O2,从而活性降低.用 H2O2 分解产生的·OH 脱除苯酚,当其他条件不变时,不同温度下,苯酚的浓度随时间的变化如图 1 所示.0~20 min 时,温度从40℃上升到 50℃,反应速率基本不变的可能原因是________ 。

(4)利用电化学高级氧化技术可以在电解槽中持续产生·OH,使处理含苯酚废水更加高效,装置如图2所示。已知 a 极主要发生的反应是 O2 生成 H2O2,然后在电解液中产生·OH 并迅速与苯酚反应。
①b 极连接电源的________ 极(填“正”或“负”)。
②a 极的电极反应式为______ 。
③除电极反应外,电解液中主要发生的反应方程式有________ , _______ 。
(1)·OH 的电子式为
(2) pH=3 时 Fe2+催化 H2O2 的分解过程中产生·OH 中间体,催化循环反应如下。将方程式 ii 补充完整。
i.Fe2++ H2O2+H+ = Fe3++ H2O +·OH
ii.
(3)已知:羟基自由基容易发生猝灭 2·OH = H2O2,从而活性降低.用 H2O2 分解产生的·OH 脱除苯酚,当其他条件不变时,不同温度下,苯酚的浓度随时间的变化如图 1 所示.0~20 min 时,温度从40℃上升到 50℃,反应速率基本不变的可能原因是

(4)利用电化学高级氧化技术可以在电解槽中持续产生·OH,使处理含苯酚废水更加高效,装置如图2所示。已知 a 极主要发生的反应是 O2 生成 H2O2,然后在电解液中产生·OH 并迅速与苯酚反应。
①b 极连接电源的
②a 极的电极反应式为
③除电极反应外,电解液中主要发生的反应方程式有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】南山中学高二某班同学为了探究影响化学反应速率的外界因素,进行以下实验:实验一:向 稀硫酸中加入过量的锌粉,标准状况下测得数据累积值如下:
稀硫酸中加入过量的锌粉,标准状况下测得数据累积值如下:
(1)在0~1、1~2、2~3、3~4、4~5min各时间段中:反应速率最快的时间段是______  ,主要的原因可能是
,主要的原因可能是______ 。
(2)为了减缓反应速率但不减少产生氢气的量,可以在稀硫酸中加入______。
实验二:通过测定酸性 溶液褪色所需的时间探究浓度对反应速率的影响,某组同学在室温下完成以下实验:
溶液褪色所需的时间探究浓度对反应速率的影响,某组同学在室温下完成以下实验:
(3)该实验所涉及反应的离子方程式为______ 。
(4)
______ ,对比实验发现浓度对化学反应速率有何影响?请结合碰撞理论解释______ 。
(5)2号实验中,用 表示的反应速率为
表示的反应速率为______ 。(假设反应前后溶液的总体积不变)。
(6)在实验中发现开始一段时间反应速率较慢,溶液褪色不明显:但不久突然褪色,反应速率明显加快。从影响化学反应速率的因素看,你认为还可能是的______ 影响。若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要试剂最合理的是______ 。(填字母)。
a.硫酸钾 b.水 c.二氧化锰 d.硫酸锰
 稀硫酸中加入过量的锌粉,标准状况下测得数据累积值如下:
稀硫酸中加入过量的锌粉,标准状况下测得数据累积值如下:时间 | 1 | 2 | 3 | 4 | 5 |
| 氢气体积 | 50 | 120 | 232 | 290 | 310 |
 ,主要的原因可能是
,主要的原因可能是(2)为了减缓反应速率但不减少产生氢气的量,可以在稀硫酸中加入______。
A. 溶液 溶液 | B. 溶液 溶液 | C. 溶液 溶液 | D. 溶液 溶液 |
实验二:通过测定酸性
 溶液褪色所需的时间探究浓度对反应速率的影响,某组同学在室温下完成以下实验:
溶液褪色所需的时间探究浓度对反应速率的影响,某组同学在室温下完成以下实验:| 实验编号 | 1 | 2 | 3 | 4 |
水 | 10 | 5 | 0 |  |
 溶液 溶液 | 5 | 10 | 10 | 5 |
 溶液 溶液 | 5 | 5 | 10 | 10 |
时间 | 40 | 20 | 10 | — |
(4)

(5)2号实验中,用
 表示的反应速率为
表示的反应速率为(6)在实验中发现开始一段时间反应速率较慢,溶液褪色不明显:但不久突然褪色,反应速率明显加快。从影响化学反应速率的因素看,你认为还可能是的
a.硫酸钾 b.水 c.二氧化锰 d.硫酸锰
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】为了降低电子垃圾对环境构成的影响,将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
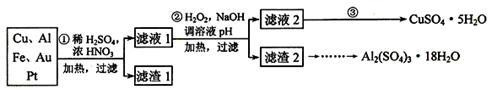
(1)第①步Cu与混酸反应的离子方程式为________________ 。得到滤渣1的主要成分为___________ 。
(2)第②步中加入H2O2的作用是__________________ ,使用H2O2的优点是_________ ;调溶液pH的目的是_________________ 。
(3)简述第③步由滤液2得到CuSO4·5H2O的方法是_________________________ 。
(4)由滤渣2制取Al2(SO4)3·18H2O ,设计了以下三种方案:
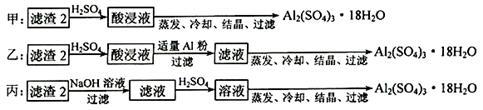
上述三种方案中,_______ 方案不可行,原因是________________ ;
从原子利用率角度考虑,_______ 方案更合理。
(5)用滴定法测定CuSO4·5H2O含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol·L-1EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL。滴定反应如下:Cu2++ H2Y2-→ CuY2-+ 2H+。写出计算CuSO4·5H2O质量分数的表达式ω=__________________ 。

(1)第①步Cu与混酸反应的离子方程式为
(2)第②步中加入H2O2的作用是
(3)简述第③步由滤液2得到CuSO4·5H2O的方法是
(4)由滤渣2制取Al2(SO4)3·18H2O ,设计了以下三种方案:

上述三种方案中,
从原子利用率角度考虑,
(5)用滴定法测定CuSO4·5H2O含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol·L-1EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液b mL。滴定反应如下:Cu2++ H2Y2-→ CuY2-+ 2H+。写出计算CuSO4·5H2O质量分数的表达式ω=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学习探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
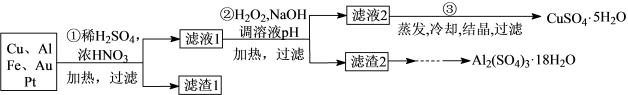
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为_________ ;
得到滤渣I的主要成分为____________________ ;
(2)第②步加H2O2的作用是__________________ ;
(3)用第③步所得CuSO4·5H2O制备无水CuSO4的方法是________ ;
(4)由滤渣2制取Al2(SO4)3·18H2O,探究小组设计了三种方案:
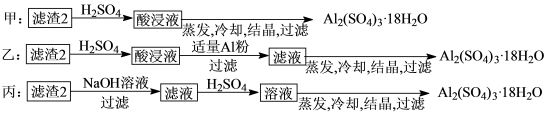
上述三种方案中,___ 方案不可行,原因是_____ ;从原子利用率角度考虑,___ 方案更合理。

请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为
得到滤渣I的主要成分为
(2)第②步加H2O2的作用是
(3)用第③步所得CuSO4·5H2O制备无水CuSO4的方法是
(4)由滤渣2制取Al2(SO4)3·18H2O,探究小组设计了三种方案:
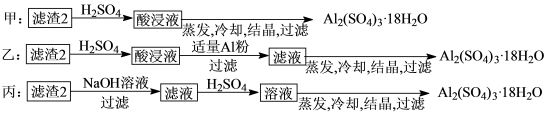
上述三种方案中,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】五水合硫酸铜(CuSO4·5H2O)是蓝色晶体,某学生实验小组利用铜屑制备CuSO4·5H2O,并进行了相关实验。具体合成路线如下:

回答下列问题:
(1)铜屑需经预处理除去表面油污,方法是___________ 。
(2)步骤①的实验装置如图(a)所示(夹持、加热仪器略),其中浓硝酸需要逐滴加入,其原因是___________ 。(写出两点即可)
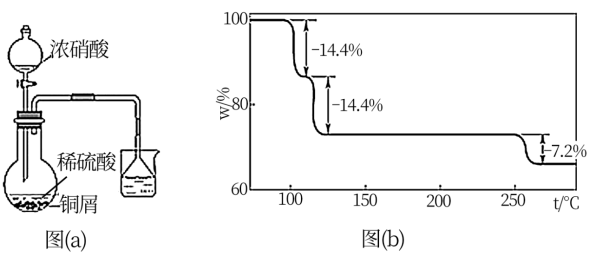
(3)CuSO4·5H2O在受热时质量分数(w)随温度的变化情况如图(b)所示。据此分析可知,CuSO4·5H2O受热过程可能发生的化学反应是___________ (填标号)。
A.

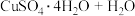
B.

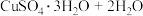
C.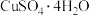

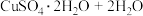
D.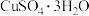


(4)制备过程中若加热不当会导致晶体发白,为了得到蓝色的CuSO4·5H2O晶体,步骤③最适宜采用___________ (填标号)加热。
A. 电热套B.
电热套B. 酒精灯C.
酒精灯C. 水浴锅 D.煤气灯
水浴锅 D.煤气灯
(5)CuSO4·5H2O保存不当会失水风化,为测定所得产品中结晶水的含量,学生小组进行了如下实验:
①准确称取产品(CuSO4·xH2O)mg置于250mL锥形瓶中,用适量水溶解,加入足量KI,得到白色沉淀和I2的棕黄色溶液,相应的离子方程式为___________ 。
②以淀粉为指示剂,用浓度为cmol·L-1的Na2S2O3标准溶液滴定上述反应中生成的I2,滴定终点时的颜色变化为___________ 。
③滴定达终点时消耗Na2S2O3溶液VmL,则x=___________ (列表达式)。
(已知:滴定反应的离子方程式为: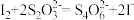 )
)
(6)请从原子经济性和环境友好的角度,设计由铜制备CuSO4·5H2O的合成路线___________ 。

回答下列问题:
(1)铜屑需经预处理除去表面油污,方法是
(2)步骤①的实验装置如图(a)所示(夹持、加热仪器略),其中浓硝酸需要逐滴加入,其原因是

(3)CuSO4·5H2O在受热时质量分数(w)随温度的变化情况如图(b)所示。据此分析可知,CuSO4·5H2O受热过程可能发生的化学反应是
A.


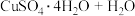
B.


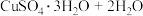
C.
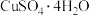

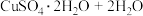
D.
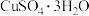


(4)制备过程中若加热不当会导致晶体发白,为了得到蓝色的CuSO4·5H2O晶体,步骤③最适宜采用
A.
 电热套B.
电热套B. 酒精灯C.
酒精灯C. 水浴锅 D.煤气灯
水浴锅 D.煤气灯
(5)CuSO4·5H2O保存不当会失水风化,为测定所得产品中结晶水的含量,学生小组进行了如下实验:
①准确称取产品(CuSO4·xH2O)mg置于250mL锥形瓶中,用适量水溶解,加入足量KI,得到白色沉淀和I2的棕黄色溶液,相应的离子方程式为
②以淀粉为指示剂,用浓度为cmol·L-1的Na2S2O3标准溶液滴定上述反应中生成的I2,滴定终点时的颜色变化为
③滴定达终点时消耗Na2S2O3溶液VmL,则x=
(已知:滴定反应的离子方程式为:
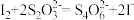 )
)(6)请从原子经济性和环境友好的角度,设计由铜制备CuSO4·5H2O的合成路线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】ZrO2常用作陶瓷材料,可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO2·SiO2,还含有少量Fe2O3、Al2O3、SiO2等杂质)通过如下方法制取。
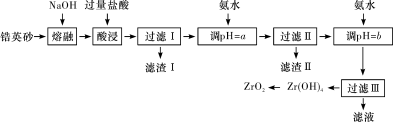
已知:①ZrO2能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如下表所示。
(1)“熔融”时ZrSiO4发生反应的化学方程式为________________________________ 。
(2)“滤渣Ⅰ”的化学式为________________ 。
(3)为使滤液Ⅰ中的杂质离子沉淀完全,需用氨水调pH=a,则a的范围是________ ;继续加氨水至pH=b时,所发生反应的离子方程式为__________________________________________ 。
(4)向“过滤Ⅲ”所得滤液中加入CaCO3粉末并加热,得到两种气体。该反应的离子方程式为____________________________ 。

已知:①ZrO2能与烧碱反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
②部分金属离子在实验条件下开始沉淀和完全沉淀的pH如下表所示。
| 金属离子 | Fe3+ | Al3+ | ZrO2+ |
| 开始沉淀时pH | 1.9 | 3.3 | 6.2 |
| 沉淀完全时pH | 3.2 | 5.2 | 8.0 |
(2)“滤渣Ⅰ”的化学式为
(3)为使滤液Ⅰ中的杂质离子沉淀完全,需用氨水调pH=a,则a的范围是
(4)向“过滤Ⅲ”所得滤液中加入CaCO3粉末并加热,得到两种气体。该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】一种以铝矿(主要成分为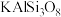 、
、 和
和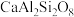 等)为原料生产金属铝的工艺流程如下:
等)为原料生产金属铝的工艺流程如下:

已知几种氯化物在常压时的熔、沸点:
回答下列问题:
(1)CaAl2Si2O8用氧化物形式可表示为____________ .
(2)“流化”阶段温度保持在900℃以上,使铝土矿中物质全部转化为氯化物。
①“流化过程中NaAlSi3O8发生的化学反应方程式为__________________ .
②Ⅱ级冷凝的温度不能高于______ ℃
(3)“操作Ⅱ”的名称是____________ ,“操作Ⅲ”的名称是____________ 。
(4)副产物A为____________ ;
(5)尾气含有剧毒的COCl2,它能被强碱溶液能吸收,其反应的离子方程式为____________ 。
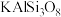 、
、 和
和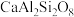 等)为原料生产金属铝的工艺流程如下:
等)为原料生产金属铝的工艺流程如下:
已知几种氯化物在常压时的熔、沸点:
物质 | SiCl4 | AlCl3 | NaCl | KCl | CaCl2 |
沸点/℃ | 58 | 180 | 1465 | — | 1935 |
熔点/℃ | -69 | — | 801 | 771 | 775 |
回答下列问题:
(1)CaAl2Si2O8用氧化物形式可表示为
(2)“流化”阶段温度保持在900℃以上,使铝土矿中物质全部转化为氯化物。
①“流化过程中NaAlSi3O8发生的化学反应方程式为
②Ⅱ级冷凝的温度不能高于
(3)“操作Ⅱ”的名称是
(4)副产物A为
(5)尾气含有剧毒的COCl2,它能被强碱溶液能吸收,其反应的离子方程式为
您最近一年使用:0次
【推荐3】信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu,25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:(友情提示:要将溶液中的 、
、 、
、 、
、 沉淀为氢氧化物,需溶液的pH分别为:6.4、6.4、3.7、4.7)
沉淀为氢氧化物,需溶液的pH分别为:6.4、6.4、3.7、4.7)

请回答下列问题:
(1)如何检验滤液1中是否含有 ?
?_______________ ;得到滤渣1的主要成分为____________ 。
(2)第2步加 的作用是
的作用是____________ ,使用 的优点是
的优点是____________ ;调溶液pH的目的是使____________ 生成沉淀。
(3)用第③步所得 制备无水
制备无水 的方法是
的方法是____________ 。
(4)由滤渣2制取 ,探究小组设计了三种方案:
,探究小组设计了三种方案:

上述三种方案中,______ 方案不可行,原因是_________ ;从原子利用率角度考虑,______ 方案更合理。
(5)结晶水的测定:将坩埚洗净,烘干至恒重,记录质量;在坩埚中加入研细的三草酸合铁酸钾晶体,称量并记录质量;加热至250℃,恒温一段时间,置于空气中冷却,称量并记录质量;计算结晶水含量。请纠正实验过程中的两处错误:______________ 、______________ 。
 、
、 、
、 、
、 沉淀为氢氧化物,需溶液的pH分别为:6.4、6.4、3.7、4.7)
沉淀为氢氧化物,需溶液的pH分别为:6.4、6.4、3.7、4.7)
请回答下列问题:
(1)如何检验滤液1中是否含有
 ?
?(2)第2步加
 的作用是
的作用是 的优点是
的优点是(3)用第③步所得
 制备无水
制备无水 的方法是
的方法是(4)由滤渣2制取
 ,探究小组设计了三种方案:
,探究小组设计了三种方案:
上述三种方案中,
(5)结晶水的测定:将坩埚洗净,烘干至恒重,记录质量;在坩埚中加入研细的三草酸合铁酸钾晶体,称量并记录质量;加热至250℃,恒温一段时间,置于空气中冷却,称量并记录质量;计算结晶水含量。请纠正实验过程中的两处错误:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】过二硫酸铵[ ]具有强氧化性,广泛用于蓄电池工业,其电解法制备的装置如图所示:
]具有强氧化性,广泛用于蓄电池工业,其电解法制备的装置如图所示:

(1)已知:电解效率η的定义为
①M膜为___________ (填“阳”或“阴”)离子交换膜,生成 的电极反应式是
的电极反应式是___________ 。
②向阳极室和阴极室各加入100mL溶液。经测定制备的 的物质的量浓度为
的物质的量浓度为 ,在电极a、b表面共收集到
,在电极a、b表面共收集到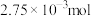 气体。则电极b表面收集到的气体是
气体。则电极b表面收集到的气体是___________ , 为
为___________ 。
(2)取电解后的b极室溶液少许于甲、乙两支试管中,进行下列实验:向甲试管中滴入酸化的KI和淀粉溶液并微热,溶液变蓝,说明过二硫酸铵具有___________ (填“氧化”或“还原”)性;向乙试管中滴入酸化的 溶液及1滴
溶液及1滴 溶液(催化)并微热,溶液变紫色,能说明该现象的离子方程式为
溶液(催化)并微热,溶液变紫色,能说明该现象的离子方程式为___________ 。
(3)以 为原料制备过二硫酸钾的主要流程如下:
为原料制备过二硫酸钾的主要流程如下:
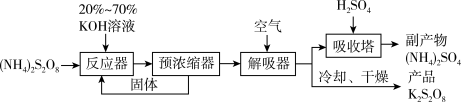
已知 受热分解可得
受热分解可得 、
、 等。
等。
①预浓缩得到的固体返回反应器再次与反应物作用的目的是___________ 。
②解吸器中通入空气的目的是___________ 。
 ]具有强氧化性,广泛用于蓄电池工业,其电解法制备的装置如图所示:
]具有强氧化性,广泛用于蓄电池工业,其电解法制备的装置如图所示:
(1)已知:电解效率η的定义为

①M膜为
 的电极反应式是
的电极反应式是②向阳极室和阴极室各加入100mL溶液。经测定制备的
 的物质的量浓度为
的物质的量浓度为 ,在电极a、b表面共收集到
,在电极a、b表面共收集到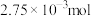 气体。则电极b表面收集到的气体是
气体。则电极b表面收集到的气体是 为
为(2)取电解后的b极室溶液少许于甲、乙两支试管中,进行下列实验:向甲试管中滴入酸化的KI和淀粉溶液并微热,溶液变蓝,说明过二硫酸铵具有
 溶液及1滴
溶液及1滴 溶液(催化)并微热,溶液变紫色,能说明该现象的离子方程式为
溶液(催化)并微热,溶液变紫色,能说明该现象的离子方程式为(3)以
 为原料制备过二硫酸钾的主要流程如下:
为原料制备过二硫酸钾的主要流程如下:
已知
 受热分解可得
受热分解可得 、
、 等。
等。①预浓缩得到的固体返回反应器再次与反应物作用的目的是
②解吸器中通入空气的目的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组欲用下图所示装置制备 SO2并探究其某些性质。___________________ ,该反应中,浓硫酸体现氧化性和酸性的物质的量之比为______________ 。
(2)为验证二氧化硫的漂白性,试管a中的现象是___________________ 。
(3)反应一段时间后,试管b 中溶液出现淡黄色沉淀,该现象说明二氧化硫具有___________ 性。
(4)为了验证试管c中 SO2与 Fe3+发生了氧化还原反应,在如图装置中通入过量 的 SO2后,取试管 c 中的溶液分成三份,并设计了如下实验:
方案I:向第一份溶液中加入酸性 KMnO4溶液,紫色褪去;
方案Ⅱ:向第二份溶液中加入 KSCN 溶液不变红,再加入新制的氯水,溶液变红;
方案Ⅲ:向第三份溶液中加入用盐酸酸化的 BaCl2溶液,产生白色沉淀。
指出上述不合理的方案并说明原因:_______________ 。
(5)为验证二氧化硫的还原性,反应一段时间后,将试管d中的溶液分成三份,分别进行如下实验。
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入 BaCl2溶液,产生白色沉淀。
上述方案合理的是___________ (填“I”“Ⅱ”或“Ⅲ”)。试管d中发生反应生成__________ 、___________ 。
(6)试管e中发生反应的离子方程式为_______________ 。试管f中装 NaOH 溶液的目的是_________________ 。
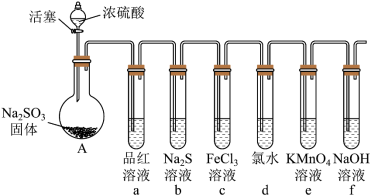
(2)为验证二氧化硫的漂白性,试管a中的现象是
(3)反应一段时间后,试管b 中溶液出现淡黄色沉淀,该现象说明二氧化硫具有
(4)为了验证试管c中 SO2与 Fe3+发生了氧化还原反应,在如图装置中通入
方案I:向第一份溶液中加入酸性 KMnO4溶液,紫色褪去;
方案Ⅱ:向第二份溶液中加入 KSCN 溶液不变红,再加入新制的氯水,溶液变红;
方案Ⅲ:向第三份溶液中加入用盐酸酸化的 BaCl2溶液,产生白色沉淀。
指出上述不合理的方案并说明原因:
(5)为验证二氧化硫的还原性,反应一段时间后,将试管d中的溶液分成三份,分别进行如下实验。
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入 BaCl2溶液,产生白色沉淀。
上述方案合理的是
(6)试管e中发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】工业上用木炭粉和水蒸气在高温条件下反应制取H2,同时生成CO2。某学习小组在实验室中模拟H2的工业生产过程并测定其产率,实验装置如下所示。
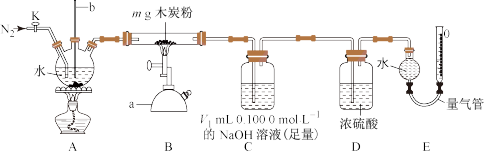
(1)仪器a的名称为_______________ 。仪器b的作用为________________ 。
(2)实验步骤:连接好装置,检查装置的气密性;___________ (按顺序填入下列步骤的序号)。
①向装置A、B、C、D中分别加入相应试剂,打开活塞K,通入一段时间N2。
②加热装置B处硬质玻璃管。
③关闭活塞K,连接盛有适量水的量气管。
④点燃装置A处酒精灯。
⑤待装置B处木炭粉完全反应后,停止加热。
(3)装置B处硬质玻璃管中发生的所有反应的化学方程式为________________ 。
(4)读取B气管读数时,应注意的事项为冷却至室温、____ 、视线与凹液面最低点相切;若仰视读取初始读数,则导致所测气体的体积_____ (填“偏大”或“偏小”)。
(5)实验后所得气体体积为V2 mL(标准状况);取装置C中液体,加入足量BaCl2溶液,过滤、洗涤,将滤液和洗涤液合并,以甲基橙为指示剂,用0.1000 mol·L−1的盐酸标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为V3mL。
①达到滴定终点时的现象为____________________ 。
②H2的产率为______________________ (列出代数式即可)。
③还可通过___________ ,得出装置C中所吸收产物的物质的量。
(6)从安全角度考虑,该实验装置的缺陷为___________________ 。

(1)仪器a的名称为
(2)实验步骤:连接好装置,检查装置的气密性;
①向装置A、B、C、D中分别加入相应试剂,打开活塞K,通入一段时间N2。
②加热装置B处硬质玻璃管。
③关闭活塞K,连接盛有适量水的量气管。
④点燃装置A处酒精灯。
⑤待装置B处木炭粉完全反应后,停止加热。
(3)装置B处硬质玻璃管中发生的所有反应的化学方程式为
(4)读取B气管读数时,应注意的事项为冷却至室温、
(5)实验后所得气体体积为V2 mL(标准状况);取装置C中液体,加入足量BaCl2溶液,过滤、洗涤,将滤液和洗涤液合并,以甲基橙为指示剂,用0.1000 mol·L−1的盐酸标准溶液滴定,达到滴定终点时,消耗标准溶液的体积为V3mL。
①达到滴定终点时的现象为
②H2的产率为
③还可通过
(6)从安全角度考虑,该实验装置的缺陷为
您最近一年使用:0次



