25℃时,有关物质的电离平衡常数如下:
(1)写出碳酸电离方程式___________ ,相同浓度的三种溶液,导电能力最强的是___________ 溶液。
(2)常温下, 的
的 溶液的电离度约为
溶液的电离度约为___________ ,体积为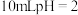 的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至
的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至 ,稀释后溶液的
,稀释后溶液的 ,前者
,前者___________ 后者(填“ ”“
”“ ”或“=”)。
”或“=”)。
(3)下列离子 在溶液中结合
在溶液中结合 的能力由大到小的顺序为
的能力由大到小的顺序为___________ 。
| 化学式 | CH3COOH | H2CO3 | H2SO3 |
| 电离平衡常数K | K=1.8×10-5 | K1=4.3×10-7,K2= 5.6×10-11 | K1=1.5×10-2, K2=1.02×10-7 |
(1)写出碳酸电离方程式
(2)常温下,
 的
的 溶液的电离度约为
溶液的电离度约为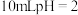 的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至
的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至 ,稀释后溶液的
,稀释后溶液的 ,前者
,前者 ”“
”“ ”或“=”)。
”或“=”)。(3)下列离子
 在溶液中结合
在溶液中结合 的能力由大到小的顺序为
的能力由大到小的顺序为
更新时间:2021-11-10 15:49:33
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】部分弱酸的电离平衡常数如下表:
(1)依据表格中三种酸的电离常数,判断三种酸酸性强弱的顺序为___________ 。
(2)向NaCN溶液中通入CO2气体,请写出反应的化学方程式___________ 。
| 弱酸 |  |  |  |
| 电离平衡常数 (25℃) | 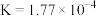 | 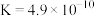 |   |
(1)依据表格中三种酸的电离常数,判断三种酸酸性强弱的顺序为
(2)向NaCN溶液中通入CO2气体,请写出反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】磷能形成次磷酸(H3PO2)、亚磷酸(H3PO3)等多种含氧酸。
(1)次磷酸(H3PO2)是一种精细化工产品,已知10mL 1mol·L-1H3PO2与20mL 1mol·L-1NaOH溶液充分反应后生成组成为NaH2PO2的盐,回答下列问题:
①NaH2PO2属于_____ (填“正盐”“酸式盐”或“无法确定”)。
②若25℃时,Ka(H3PO2)=1×10-2,则0.02mol·L-1的H3PO2溶液的pH=_____ 。
③设计两种实验方案,证明次磷酸是弱酸:_____ 。
(2)亚磷酸(H3PO3)是二元中强酸,某温度下,0.11mol·L-1的H3PO3溶液的pH为2,该温度下H3PO3的电离平衡常数Ka1约为_____ (Ka2=2×10-7,H3PO3的二级电离和水的电离忽略不计)。
(3)亚磷酸的结构式为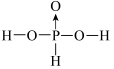 (式中P→O表示成键电子对全部由磷原子提供),含有两个“-OH”,分子中有两个可电离的氢原子,因而是二元酸,由此类推次磷酸分子中含有
(式中P→O表示成键电子对全部由磷原子提供),含有两个“-OH”,分子中有两个可电离的氢原子,因而是二元酸,由此类推次磷酸分子中含有____ 个“-OH”。
(4)向H3PO3溶液中滴加NaOH溶液:
①当恰好中和生成Na2HPO3时,所得溶液的pH____ 7(填“>”“<”或“=”,下同);
②当溶液呈中性时,所得溶液中c(Na+)_____ c(H2PO )+2c(HPO
)+2c(HPO );
);
③若用甲基橙做指示剂,用NaOH溶液滴定,达到滴定终点时,所得溶液中c(Na+)____ c(H2PO )+2c(HPO
)+2c(HPO )。
)。
(1)次磷酸(H3PO2)是一种精细化工产品,已知10mL 1mol·L-1H3PO2与20mL 1mol·L-1NaOH溶液充分反应后生成组成为NaH2PO2的盐,回答下列问题:
①NaH2PO2属于
②若25℃时,Ka(H3PO2)=1×10-2,则0.02mol·L-1的H3PO2溶液的pH=
③设计两种实验方案,证明次磷酸是弱酸:
(2)亚磷酸(H3PO3)是二元中强酸,某温度下,0.11mol·L-1的H3PO3溶液的pH为2,该温度下H3PO3的电离平衡常数Ka1约为
(3)亚磷酸的结构式为
 (式中P→O表示成键电子对全部由磷原子提供),含有两个“-OH”,分子中有两个可电离的氢原子,因而是二元酸,由此类推次磷酸分子中含有
(式中P→O表示成键电子对全部由磷原子提供),含有两个“-OH”,分子中有两个可电离的氢原子,因而是二元酸,由此类推次磷酸分子中含有(4)向H3PO3溶液中滴加NaOH溶液:
①当恰好中和生成Na2HPO3时,所得溶液的pH
②当溶液呈中性时,所得溶液中c(Na+)
 )+2c(HPO
)+2c(HPO );
);③若用甲基橙做指示剂,用NaOH溶液滴定,达到滴定终点时,所得溶液中c(Na+)
 )+2c(HPO
)+2c(HPO )。
)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)25时℃,0.2 mol/L的HF溶液中存在下述平衡:HF H++F-。加一定量的蒸馏水,平衡将
H++F-。加一定量的蒸馏水,平衡将____ (填“正向”、“逆向”或“不”)移动,溶液中的c(H+)将___ (填“增大”、“减小”或“不变”);加入少量0.2mol/L的盐酸,能___ (填“促进”或“抑制”)HF的电离,HF的电离平衡常数K将___ (填“增大”、“减小”或“不变”);
(2)下列物质属于电解质的是____ ;属于非电解质的是____ ;能导电的物质是____ ;其水溶液能够导电的物质____ 。
①CO2 ②铜 ③烧碱 ④NH3.H2O ⑤石墨 ⑥碳酸钠 ⑦CH3COOH ⑧蔗糖 ⑨氯气 ⑩盐酸
 H++F-。加一定量的蒸馏水,平衡将
H++F-。加一定量的蒸馏水,平衡将(2)下列物质属于电解质的是
①CO2 ②铜 ③烧碱 ④NH3.H2O ⑤石墨 ⑥碳酸钠 ⑦CH3COOH ⑧蔗糖 ⑨氯气 ⑩盐酸
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)同浓度的CH3COOH、H2CO3、HClO溶液的pH最大的是_____ .
(2)常温下0.1mol•L﹣1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是_____ (填字母序号,下同).
A.c(H+)
B.
C.c(H+)•c(OH﹣)
D.
E.
若该溶液升高温度,上述5种表达式的数据增大的是_________ .
(3)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:则HX的电离平衡常数_____ (填“大于”、“等于”或“小于”)醋酸的平衡常数.稀释后,HX溶液中有水电离出来的c(H+)_____ (填“大于”、“等于”或“小于”)醋酸的溶液中有水电离出来的c(H+),理由是___________ .

(4)已知100℃时,水的离子积为1×10﹣12,该温度下测得某溶液pH=7,该溶液显_____ (填“酸”、“碱”或“中”)性.将此温度下pH=1的H2SO4溶液aL与pH=11的NaOH溶液bL混合,若所得混合液PH=2,则a:b=_____ .
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10﹣4mol•L﹣1 | K1=4.4×10﹣6mol•L﹣1 K2=5.6×10﹣11mol•L﹣1 | 3.0×10﹣8 mol•L﹣1 |
请回答下列问题:
(1)同浓度的CH3COOH、H2CO3、HClO溶液的pH最大的是
(2)常温下0.1mol•L﹣1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是
A.c(H+)
B.

C.c(H+)•c(OH﹣)
D.

E.

若该溶液升高温度,上述5种表达式的数据增大的是
(3)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图:则HX的电离平衡常数

(4)已知100℃时,水的离子积为1×10﹣12,该温度下测得某溶液pH=7,该溶液显
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸。
(1)当三种酸物质的量浓度相同时,c平(H+)由大到小的顺序是___________ (用字母表示,下同)。
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是___________ 。
(3)若三者c平(H+)相同时,物质的量浓度由大到小的顺序是___________ 。
(4)将c平(H+)相同的三种酸均加水稀释至原来的100倍后,c平(H+)由大到小的顺序是___________ 。
(5)将c平(H+)相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为___________ 。
(1)当三种酸物质的量浓度相同时,c平(H+)由大到小的顺序是
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是
(3)若三者c平(H+)相同时,物质的量浓度由大到小的顺序是
(4)将c平(H+)相同的三种酸均加水稀释至原来的100倍后,c平(H+)由大到小的顺序是
(5)将c平(H+)相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,部分酸的电离常数如表所示
(1) 相同的三种酸,其酸的浓度从大到小顺序为
相同的三种酸,其酸的浓度从大到小顺序为_______ 。
(2)若HCN的起始浓度为 ,平衡时
,平衡时 约为
约为_______  。若使此溶液中HCN的电离程度增大且
。若使此溶液中HCN的电离程度增大且 也增大的方法是
也增大的方法是_______ 。
(3)中和等量的NaOH,消耗等pH的氢氟酸和硫酸的体积分别为a L、b L,则a_______ (填“大于”“小于”或“等于”,下同)b。
(4)向NaCN溶液中通入少量的 ,发生反应的离子方程式为
,发生反应的离子方程式为_______
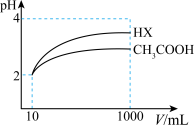
(5)25℃时,体积为10mL、pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图,则HX的电离平衡常数_______ (填“大于”“小于”或“等于”,下同)醋酸的电离平衡常数,稀释后,HX溶液中水电离出来的
_______ 醋酸溶液中水电离出来的 。
。
| 化学式 | HF | HCN |  |
| 电离常数 | 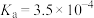 | 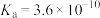 |  , , |
 相同的三种酸,其酸的浓度从大到小顺序为
相同的三种酸,其酸的浓度从大到小顺序为(2)若HCN的起始浓度为
 ,平衡时
,平衡时 约为
约为 。若使此溶液中HCN的电离程度增大且
。若使此溶液中HCN的电离程度增大且 也增大的方法是
也增大的方法是(3)中和等量的NaOH,消耗等pH的氢氟酸和硫酸的体积分别为a L、b L,则a
(4)向NaCN溶液中通入少量的
 ,发生反应的离子方程式为
,发生反应的离子方程式为(5)25℃时,体积为10mL、pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程pH变化如图,则HX的电离平衡常数

 。
。
您最近一年使用:0次



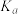
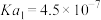
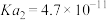




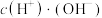
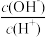
 的一组醋酸、醋酸钠混合溶液,溶液中
的一组醋酸、醋酸钠混合溶液,溶液中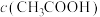 、
、 与pH的关系如下图所示。
与pH的关系如下图所示。
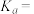
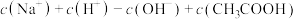 =
=

