已知:①C(s,石墨)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1,
②C(s,金刚石)+O2(g)=CO2(g) ΔH=-395.0kJ·mol-1,
则下列分析不正确的是
②C(s,金刚石)+O2(g)=CO2(g) ΔH=-395.0kJ·mol-1,
则下列分析不正确的是
| A.C(s,石墨)=C(s,金刚石) ΔH=+1.5kJ·mol-1 |
| B.等质量的石墨比金刚石能量低 |
| C.金刚石比石墨稳定 |
| D.等质量的金刚石、石墨完全转化为二氧化碳量,转移的电子数相同 |
更新时间:2021-11-13 10:24:30
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知下列反应的能量变化示意图如图,有关说法正确的是
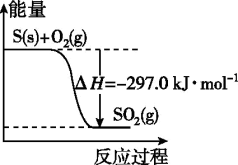
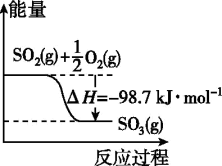


| A.1molS(g)与O2(g)完全反应生成SO2(g)放出的热量小于297.0kJ |
| B.在相同条件下,SO2(g)比SO3(g)稳定 |
C.S(s)与O2(g)反应生成SO3(g)的热化学方程式为S(s)+ O2(g)⇌SO3(g) ΔH=-395.7kJ·mol-1 O2(g)⇌SO3(g) ΔH=-395.7kJ·mol-1 |
D.一定条件下1molSO2(g)和 molO2(g)反应生成1molSO3(l)放出热量小于98.7kJ molO2(g)反应生成1molSO3(l)放出热量小于98.7kJ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
A.已知:  ,则碳的燃烧热 ,则碳的燃烧热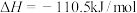 |
B.已知:C(石墨,s)=C(金刚石,s) 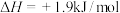 ,则金刚石比石墨稳定 ,则金刚石比石墨稳定 |
C.已知: ; ; ,则 ,则 |
D.已知: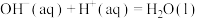 ; ;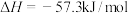 ,则 ,则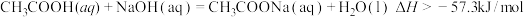 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关能量的判断和表示方法正确的是
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多 |
| B.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l) ΔH=-57.4 kJ·mol-1 |
C.已知HI(g)  H2(g)+ H2(g)+ I2(s) ΔH=-26.5 kJ·mol-1,由此可知1 mol HI气体在密闭容器中充分分解后可以放出26.5 kJ的热量 I2(s) ΔH=-26.5 kJ·mol-1,由此可知1 mol HI气体在密闭容器中充分分解后可以放出26.5 kJ的热量 |
| D.由C(s,石墨)=C(s,金刚石) ΔH=+1.9 kJ·mol-1,可知:石墨比金刚石更稳定 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列变化,属于吸热过程的是
| A.浓H2SO4溶于水 | B.甲烷燃烧 |
| C.CaO与水反应 | D.Ba(OH)2晶体与NH4Cl反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图所示为CFCl3破坏臭氧层的过程,下列说法不正确的是
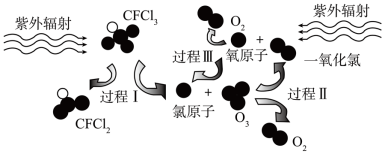

| A.过程Ⅰ中断裂极性键C-Cl键 |
| B.过程Ⅱ可用方程式表示为O3+Cl=ClO+O2 |
| C.过程Ⅲ中ClO+O=O2+Cl是吸热过程 |
| D.上述过程说明CFCl3是破坏臭氧层的催化剂 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】利用水煤气(主要成分 、CO)可将
、CO)可将 在高温下还原成硫单质,从而实现脱硫。主要发生了下列反应:
在高温下还原成硫单质,从而实现脱硫。主要发生了下列反应:
反应Ⅰ:
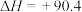 kJ⋅mol
kJ⋅mol
反应Ⅱ: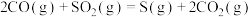
 kJ⋅mol
kJ⋅mol
在恒压条件下用水煤气还原 ,起始时
,起始时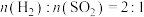 条件下,
条件下, 和
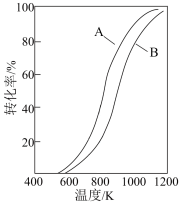
和 的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
 、CO)可将
、CO)可将 在高温下还原成硫单质,从而实现脱硫。主要发生了下列反应:
在高温下还原成硫单质,从而实现脱硫。主要发生了下列反应:反应Ⅰ:

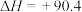 kJ⋅mol
kJ⋅mol
反应Ⅱ:
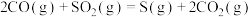
 kJ⋅mol
kJ⋅mol
在恒压条件下用水煤气还原
 ,起始时
,起始时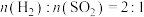 条件下,
条件下, 和
和 的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
的平衡转化率随温度变化的曲线如图所示。下列有关说法正确的是
A.反应Ⅰ的平衡常数可表示为 |
B.反应Ⅱ的 |
C.曲线B表示 的平衡转化率随温度的变化 的平衡转化率随温度的变化 |
D. 的 的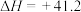 kJ⋅mol kJ⋅mol |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】氨气还原法可用于消除NO对环境的污染。
已知:①N2(g)+O2(g) 2NO(g) △H1=+180.50 kJ·mol-1
2NO(g) △H1=+180.50 kJ·mol-1
②4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H2=−905.48 kJ·mol-1
下列说法不正确的是
已知:①N2(g)+O2(g)
 2NO(g) △H1=+180.50 kJ·mol-1
2NO(g) △H1=+180.50 kJ·mol-1②4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H2=−905.48 kJ·mol-1
下列说法不正确的是
| A.反应①将电能转化成化学能 |
| B.反应②使用催化剂时的△H2不变 |
| C.反应①、②均属于氮的固定 |
| D.4NH3(g)+6NO(g)=5N2(g)+6H2O(g) △H=−1807.98 kJ·mol-1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】关于反应Na2S2O3+H2SO4=Na2SO4+S ↓+SO2↑ +H2O,下列说法不正确的是
| A.H2SO4发生还原反应 |
| B.Na2S2O3既是氧化剂又是还原剂 |
| C.氧化产物与还原产物的物质的量之比为1∶1 |
| D.1mol Na2S2O3发生反应,转移2mol电子 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】硫酸是重要的化工原料,我国工业上一般以黄铁矿为原料来制备硫酸。工业制硫酸涉及下列反应:① ;②
;② ;③
;③ 。生产中用浓硫酸代替水吸收
。生产中用浓硫酸代替水吸收 ,制得焦硫酸(
,制得焦硫酸( ,也可以表示为
,也可以表示为 ),将焦硫酸稀释后可制得密度为
),将焦硫酸稀释后可制得密度为 、质量分数为98%的浓硫酸。下列说法不正确的是
、质量分数为98%的浓硫酸。下列说法不正确的是
 ;②
;② ;③
;③ 。生产中用浓硫酸代替水吸收
。生产中用浓硫酸代替水吸收 ,制得焦硫酸(
,制得焦硫酸( ,也可以表示为
,也可以表示为 ),将焦硫酸稀释后可制得密度为
),将焦硫酸稀释后可制得密度为 、质量分数为98%的浓硫酸。下列说法不正确的是
、质量分数为98%的浓硫酸。下列说法不正确的是A.每生成1mol 时,转移5.5mol电子 时,转移5.5mol电子 |
B.焦硫酸钠( )的水溶液呈酸性 )的水溶液呈酸性 |
C.质量分数为98%的浓 ,物质的量浓度为18.4mol/L ,物质的量浓度为18.4mol/L |
D.浓硫酸吸收 生成焦硫酸的变化是物理变化 生成焦硫酸的变化是物理变化 |
您最近半年使用:0次

 2Fe+Al2O3
2Fe+Al2O3


