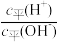用水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是
A. | B. |
C.NH 的浓度 的浓度 | D.OH-的物质的量 |
更新时间:2021-12-01 20:24:52
|
相似题推荐
多选题
|
较易
(0.85)
【推荐1】把1 L 0.1 mol·L-1醋酸溶液用蒸馏水稀释到10 L,下列叙述正确的是( )
A.[CH3COOH]变为原来的 |
B.c(H+)变为原来的 |
C. 的比值增大 的比值增大 |
| D.溶液的导电性减弱 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐2】向CH3COOH 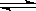 CH3COO-+ H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变大的是
CH3COO-+ H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变大的是
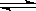 CH3COO-+ H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变大的是
CH3COO-+ H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变大的是| A.NH4Cl固体 | B.CH3COONa | C.NH3·H2O | D.Zn粉 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐1】下列不能证明 是弱电解质的是
是弱电解质的是
 是弱电解质的是
是弱电解质的是A.用 溶液做导电实验,灯泡很暗 溶液做导电实验,灯泡很暗 |
B.等pH等体积的盐酸、 溶液和足量锌反应, 溶液和足量锌反应, 放出的氢气较少 放出的氢气较少 |
C.0.1 mol/L的 溶液的 溶液的 |
D. 的 的 溶液稀释100倍, 溶液稀释100倍,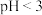 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐2】常温下,某 的一元酸
的一元酸 溶液中,
溶液中, 的电离百分数为
的电离百分数为 ,某0.1
,某0.1 的一元碱
的一元碱 溶液中
溶液中 与
与 之比为
之比为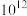 。将上述两种溶液等体积混合后,溶液显酸性,若混合时体积变化忽略不计,下列推论错误的是
。将上述两种溶液等体积混合后,溶液显酸性,若混合时体积变化忽略不计,下列推论错误的是
 的一元酸
的一元酸 溶液中,
溶液中, 的电离百分数为
的电离百分数为 ,某0.1
,某0.1 的一元碱
的一元碱 溶液中
溶液中 与
与 之比为
之比为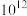 。将上述两种溶液等体积混合后,溶液显酸性,若混合时体积变化忽略不计,下列推论错误的是
。将上述两种溶液等体积混合后,溶液显酸性,若混合时体积变化忽略不计,下列推论错误的是A. 是一元强碱 是一元强碱 |
B.混合后, 的电离百分数大于a% 的电离百分数大于a% |
C.混合溶液中 小于 小于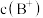 |
D. 与 与 之比值,原 之比值,原 溶液小于混合溶液 溶液小于混合溶液 |
您最近一年使用:0次
多选题
|
较易
(0.85)
解题方法
【推荐1】常温下,用0.100mol·L−1NaOH溶液分别滴定20.00mL0.100mol·L−1的HX和HY溶液,滴定曲线如图所示。下列说法正确的是
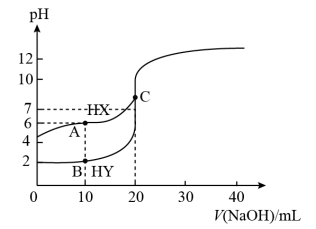

| A.Ka(HX)和Ka(HY)的数量级分别为10−8和10−4 |
| B.B点满足2c(H+)+c(HY)=2c(OH-)+c(Y-) |
| C.HX曲线上的A与C点混合,则存在c(X-)+c(HX)=2c(Na+) |
| D.A、B、C三点中由水电离出的c(H+)顺序为C>A>B |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐2】常温下,下列有关溶液的说法正确的是
A. 的电离常数 的电离常数 ,则等物质的量浓度的 ,则等物质的量浓度的 、 、 混合溶液中: 混合溶液中: |
B. 相等的① 相等的① ② ②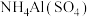 ③ ③ 溶液:浓度的大小顺序为①>②>③ 溶液:浓度的大小顺序为①>②>③ |
C. 溶液加水稀释, 溶液加水稀释, 与 与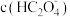 的比值将减 的比值将减 |
D.已知在相同条件下酸性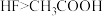 ,则浓度相等的 ,则浓度相等的 与 与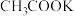 溶液中: 溶液中: |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐1】25℃时不断将水滴入0.1 mol/L的氨水中,下列图象变化合理的是
A. | B. |
C. | D. |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐2】向纯水中加入少量的KHSO4固体(温度不变),则溶液的
| A.pH值减小 | B.c(H+)和c(OH-)的乘积增大 |
| C.酸性减弱 | D.OH-离子浓度减小 |
您最近一年使用:0次

 的盐酸和醋酸溶液,与足量锌反应时,起始时产生氢气的速率一样快
的盐酸和醋酸溶液,与足量锌反应时,起始时产生氢气的速率一样快 的醋酸稀释1000倍后,溶液的
的醋酸稀释1000倍后,溶液的