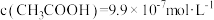常温下,用0.100mol·L−1NaOH溶液分别滴定20.00mL0.100mol·L−1的HX和HY溶液,滴定曲线如图所示。下列说法正确的是
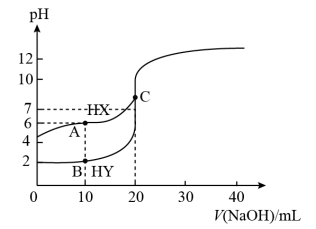

| A.Ka(HX)和Ka(HY)的数量级分别为10−8和10−4 |
| B.B点满足2c(H+)+c(HY)=2c(OH-)+c(Y-) |
| C.HX曲线上的A与C点混合,则存在c(X-)+c(HX)=2c(Na+) |
| D.A、B、C三点中由水电离出的c(H+)顺序为C>A>B |
更新时间:2021-12-31 12:40:09
|
相似题推荐
多选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法正确的是( )
| A.纯水在20℃和80℃时的pH,前者大 |
| B.Cl2、Ba(OH)2、CO2、HF 分别为非电解质、强电解质、非电解质、弱电解质 |
| C.强电解质在溶液中完全电离,不存在电离平衡 |
| D.在溶液中,导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质 |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
【推荐2】水的电离平衡曲线如图所示,下列说法错误的是


| A.图中四点Kw间的关系:A=D<C<B |
| B.若从A点到D点,可采用:温度不变在水中加入少量碱 |
| C.若从A点到C点,可采用:温度不变在水中加入少量NH4Cl固体 |
| D.若从A点到D点,可采用:温度不变在水中加入少量NH4Cl固体 |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
解题方法
【推荐1】在相同温度下,0.01mol/L的NaOH溶液和的0.01mol/L盐酸相比,下列说法正确的是
| A.由水电离出的c(H+)相等 |
B.由水电离出的c(H+)都是1.0×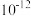 mol/L mol/L |
| C.由水电离出的c(OH-)都是0.01mol/L |
| D.两者都抑制了水的电离且抑制程度相同 |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
【推荐2】25℃时,某溶液中由水电离出的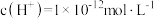 ,则该溶液的pH可能是
,则该溶液的pH可能是
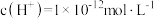 ,则该溶液的pH可能是
,则该溶液的pH可能是| A.13 | B.12 | C.2 | D.1 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐3】已知常温下溶液中CH3COOH和CH3COO-的物质的量分数与pH的关系如图所示。下列说法正确的是
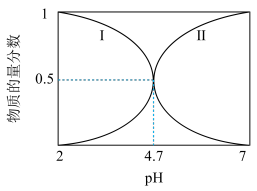

| A.图中曲线I表示的是CH3COO- |
| B.常温下,Ka(CH3COOH)=1×10-4.7 |
| C.0.1mol•L-1CH3COONa溶液中存在等式:c(Na+)+c(CH3COO-)=0.2mol•L-1 |
| D.常温下,pH=4的醋酸溶液中,由水电离产生的c(H+)=1×10-10mol•L-1 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐1】碳酸有两个电离常数Ki1、Ki2,分别对应碳酸的两步电离。关于Ki1和Ki2说法正确的是
A.Ki1的表达式为Ki1=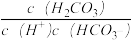 |
B.Ki2对应的电离过程是HCO3- + H2O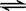 H3O++ CO32- H3O++ CO32- |
| C.当碳酸的电离平衡正向移动时,Ki1与Ki2均相应增大 |
| D.改变条件使Ki1减小,则Ki2一定也减小 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐2】常温下,某 的一元酸
的一元酸 溶液中,
溶液中, 的电离百分数为
的电离百分数为 ,某0.1
,某0.1 的一元碱
的一元碱 溶液中
溶液中 与
与 之比为
之比为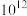 。将上述两种溶液等体积混合后,溶液显酸性,若混合时体积变化忽略不计,下列推论错误的是
。将上述两种溶液等体积混合后,溶液显酸性,若混合时体积变化忽略不计,下列推论错误的是
 的一元酸
的一元酸 溶液中,
溶液中, 的电离百分数为
的电离百分数为 ,某0.1
,某0.1 的一元碱
的一元碱 溶液中
溶液中 与
与 之比为
之比为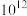 。将上述两种溶液等体积混合后,溶液显酸性,若混合时体积变化忽略不计,下列推论错误的是
。将上述两种溶液等体积混合后,溶液显酸性,若混合时体积变化忽略不计,下列推论错误的是A. 是一元强碱 是一元强碱 |
B.混合后, 的电离百分数大于a% 的电离百分数大于a% |
C.混合溶液中 小于 小于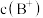 |
D. 与 与 之比值,原 之比值,原 溶液小于混合溶液 溶液小于混合溶液 |
您最近一年使用:0次
多选题
|
较易
(0.85)
【推荐3】用0.100mol·L-1HCl溶液滴定0.100mol·L-1Na2CO3溶液的滴定曲线如图,已知 。下列说法错误的是
。下列说法错误的是
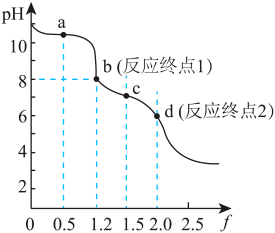
 。下列说法错误的是
。下列说法错误的是
| A.a点溶液中:c(CO32-)>c(HCO3-) |
| B.b点溶液中:c(Na+)>c(HCO3-)+c(CO32-)+c(H2CO3) |
| C.c点溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) |
| D.溶液中水的电离程度:a>b>c>d |
您最近一年使用:0次
多选题
|
较易
(0.85)
名校
【推荐1】25℃时,向20 mL 0.2 HF溶液中逐滴加入浓度为0.2
HF溶液中逐滴加入浓度为0.2  的NaOH溶液,溶液中
的NaOH溶液,溶液中 、pH、中和率(中和率=
、pH、中和率(中和率= )变化如图。下列说法正确的是
)变化如图。下列说法正确的是
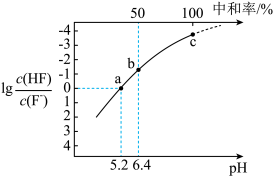
 HF溶液中逐滴加入浓度为0.2
HF溶液中逐滴加入浓度为0.2  的NaOH溶液,溶液中
的NaOH溶液,溶液中 、pH、中和率(中和率=
、pH、中和率(中和率= )变化如图。下列说法正确的是
)变化如图。下列说法正确的是
A.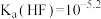 | B.水的电离程度:c点<b点 |
C.a点,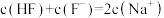 | D.b点,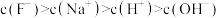 |
您最近一年使用:0次
多选题
|
较易
(0.85)
解题方法
【推荐2】苹果酸(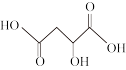 )是应用广泛的植物酸味剂,某同学利用电位滴定法滴加0.18 mol∙L−1的NaOH溶液以测定5.60mL苹果酸溶液中的苹果酸浓度。电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位(ERC)也产生了突跃,进而确定滴定终点的位置。滴定时电位滴定曲线如图所示。下列说法正确的是
)是应用广泛的植物酸味剂,某同学利用电位滴定法滴加0.18 mol∙L−1的NaOH溶液以测定5.60mL苹果酸溶液中的苹果酸浓度。电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位(ERC)也产生了突跃,进而确定滴定终点的位置。滴定时电位滴定曲线如图所示。下列说法正确的是
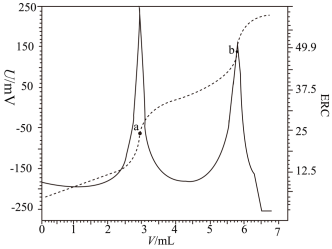
(注:——表示电极电位曲线图;……表示电极电压曲线图)
 )是应用广泛的植物酸味剂,某同学利用电位滴定法滴加0.18 mol∙L−1的NaOH溶液以测定5.60mL苹果酸溶液中的苹果酸浓度。电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位(ERC)也产生了突跃,进而确定滴定终点的位置。滴定时电位滴定曲线如图所示。下列说法正确的是
)是应用广泛的植物酸味剂,某同学利用电位滴定法滴加0.18 mol∙L−1的NaOH溶液以测定5.60mL苹果酸溶液中的苹果酸浓度。电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位(ERC)也产生了突跃,进而确定滴定终点的位置。滴定时电位滴定曲线如图所示。下列说法正确的是
(注:——表示电极电位曲线图;……表示电极电压曲线图)
| A.该滴定过程中需加入甲基橙作指示剂 |
| B.b点溶液中c(H+)<c(OH-) |
| C.原苹果酸溶液中c(C4H6O5)≈0.36 mol∙L−1 |
D.a点溶液中存在:c(OH-)+c(C4H6O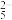 )=c(C4H6O5)+c(H+) )=c(C4H6O5)+c(H+) |
您最近一年使用:0次

 H++OH-;
H++OH-; 乙酸溶液中约有1.32%的乙酸分子发生电离。下列说法正确的是
乙酸溶液中约有1.32%的乙酸分子发生电离。下列说法正确的是 的数目约为
的数目约为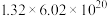
 减小
减小 溶液中,
溶液中,