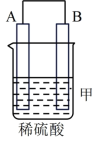
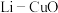 二次电池的比能量高、工作温度宽,性能优异,广泛用于军事和空间领域。
二次电池的比能量高、工作温度宽,性能优异,广泛用于军事和空间领域。(1)质量比容量是指消耗单位质量的电池所释放的电量,用来衡量电池的优劣。比较
 、
、 、
、 分别作为电极时,质量比容量由大到小的顺序为:
分别作为电极时,质量比容量由大到小的顺序为:通过如下过程制备
 。
。
(2)过程Ⅱ产生
 的离子方程式是
的离子方程式是(3)过程Ⅱ,将
 溶液加到
溶液加到 溶液中,研究二者不同物质的量之比与产品纯度的关系(用测定铜元素的百分含量来表征产品的纯度),结果如图1所示。
溶液中,研究二者不同物质的量之比与产品纯度的关系(用测定铜元素的百分含量来表征产品的纯度),结果如图1所示。
已知:
 中铜元素的百分含量为57.7%。二者比值为
中铜元素的百分含量为57.7%。二者比值为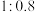 时,产品中可能含有的杂质是
时,产品中可能含有的杂质是(4)
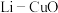 二次电池以含
二次电池以含 的有机溶液为电解质溶液,其工作原理为:
的有机溶液为电解质溶液,其工作原理为: 。装置示意图如图2所示。放电时,正极的电极反应式是
。装置示意图如图2所示。放电时,正极的电极反应式是(5)依据氧化还原反应:
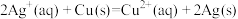 设计的原电池如图所示。电极
设计的原电池如图所示。电极 的材料是
的材料是 是
是 流向
流向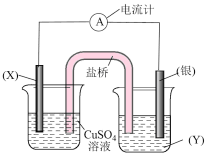
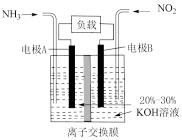
(6)利用原电池原理可将
 和
和 转化为无污染物质,其装置原理图如图丙所示,则负极反应式为
转化为无污染物质,其装置原理图如图丙所示,则负极反应式为
更新时间:2021-12-29 09:16:54
|
相似题推荐
【推荐1】氯及其化合物在工业生产生活中有很重要的作用。已知:实验室中可用KClO3与浓盐酸发生如下反应:
( ) KClO 3+( ) HCl(浓)-( ) KCl+( ) Cl2↑+( ) H2O,
(1)请配平该反应 ,并用双线桥法 标出电子转移的方向和数目。______________
(2)该反应中氧化剂为______ ;氧化剂与还原剂的物质的量之比为______ ;氧化产物与还原产物的物质的量之比为______ ;被氧化的元素和被还原的元素的质量之比为_________ 。
(3)浓盐酸在反应中表现出来的性质是________________ (填写编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸
(4)当此反应中产生标准状况下13.44L的Cl2 ,则该反应转移的电子的数目为_____ ;被氧化的盐酸的物质的量为______ mol,参加反应的盐酸的物质的量为______ mol。
(1)请
(2)该反应中氧化剂为
(3)浓盐酸在反应中表现出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸
(4)当此反应中产生标准状况下13.44L的Cl2 ,则该反应转移的电子的数目为
您最近一年使用:0次
【推荐2】请回答:
(1)写出CH3Cl的电子式____ 。
(2)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态水。已知室温下10g甲硅烷自燃放出热量473.5kJ,其热化学方程式是____ 。
(3)工业废水中加入难溶于水的FeS使其中的Cu2+离子转化为沉淀,写出该反应的离子方程式___ 。
(4)碱性条件下发生下列反应,配平该反应的离子方程式:__ ClO3﹣+__ Fe3++__ =__ Cl﹣+__ FeO42﹣+__ 。
(1)写出CH3Cl的电子式
(2)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态水。已知室温下10g甲硅烷自燃放出热量473.5kJ,其热化学方程式是
(3)工业废水中加入难溶于水的FeS使其中的Cu2+离子转化为沉淀,写出该反应的离子方程式
(4)碱性条件下发生下列反应,配平该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】用化学方程式或离子方程式表示相应的化学反应.
(1)工业生产上将氯气通入石灰乳,在一定条件下蒸干可制漂白粉.写出该过程的化学方程式:_____________________ .
(2)侯氏制碱法中最后利用小苏打固体可以制得纯碱,写出该过程的化学方程式:_____________________ .
(3)向水玻璃溶液(Na2SiO3溶液)中,加入稀盐酸可用于生产硅酸胶体.用离子方程式表示该生产原理:_____________________ .
(4)硫酸工业中用氨水吸收二氧化硫,写出氨水吸收过量二氧化硫的离子方程式_______________________ .
(5)NO是大气污染物之一,目前一种治理方法是在400℃左右、在催化剂的作用下用氨气还原,写出化学方程式_____________________ .
(1)工业生产上将氯气通入石灰乳,在一定条件下蒸干可制漂白粉.写出该过程的化学方程式:
(2)侯氏制碱法中最后利用小苏打固体可以制得纯碱,写出该过程的化学方程式:
(3)向水玻璃溶液(Na2SiO3溶液)中,加入稀盐酸可用于生产硅酸胶体.用离子方程式表示该生产原理:
(4)硫酸工业中用氨水吸收二氧化硫,写出氨水吸收过量二氧化硫的离子方程式
(5)NO是大气污染物之一,目前一种治理方法是在400℃左右、在催化剂的作用下用氨气还原,写出化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
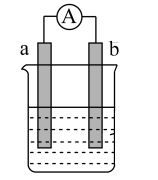
(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为___ ,H+移向___ 极(填“a”或“b”)。
(2)现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液,则甲烷应通入__ 极(填“a”或“b”)。
(3)利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池,该电池的电解质溶液是___ 。
(4)若这是氢氧燃料电池,当有20molH2反应时,则导线中通过电子的物质的量为___ mol。
(5)如果电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液,当反应中收集到标准状况下224mL气体时,消耗的电极质量为__ g。

(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为
(2)现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液,则甲烷应通入
(3)利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池,该电池的电解质溶液是
(4)若这是氢氧燃料电池,当有20molH2反应时,则导线中通过电子的物质的量为
(5)如果电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液,当反应中收集到标准状况下224mL气体时,消耗的电极质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】化学能和电能的相互转化是能量转换的重要形式,请按要求完成下列电化学相关问题。
(1)把A、B、C、D四种金属按表中装置进行实验。
根据表中信息判断四种金属活动性由大到小的顺序是___________ ;(用ABCD表示)
(2)盐桥式原电池的装置图如下___________ (填“正”或“负”)极。
②若装置中铜电极的质量增加3.2g,则导线中转移电子的数目为_________
③该装置的盐桥中除添加琼脂外,还要添加 饱和溶液,电池工作时,盐桥的作用是
饱和溶液,电池工作时,盐桥的作用是___________ 。
(3) 还原
还原 电化学法制备甲醇(
电化学法制备甲醇(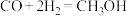 )的工作原理如图所示:
)的工作原理如图所示: 通过质子膜向
通过质子膜向___________ (填“左”或者“右”)移动,通 的一端发生的电极反应式为
的一端发生的电极反应式为___________ 。
(4)锂钊氧化物电池放电时的总反应: ,则其正极充电时的电极反应式为:
,则其正极充电时的电极反应式为:___________ 。
(5)以四甲基氯化铵[(CH3)4NCl]为原料,采用电渗析法合成四甲基氢氧化铵[(CH3)4NOH],其工作原理如图所示(a、b为石墨,c、d、e为离子交换膜),当制备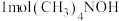 时,a、b两个极共产生
时,a、b两个极共产生___________  气体。
气体。
(1)把A、B、C、D四种金属按表中装置进行实验。
| 装置 |
|
|
|
| 电子从A到B | C电极的质量增加 | 金属D不断溶解 |
(2)盐桥式原电池的装置图如下
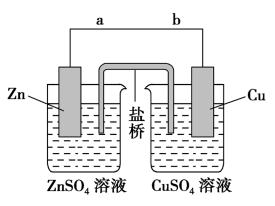
②若装置中铜电极的质量增加3.2g,则导线中转移电子的数目为
③该装置的盐桥中除添加琼脂外,还要添加
 饱和溶液,电池工作时,盐桥的作用是
饱和溶液,电池工作时,盐桥的作用是(3)
 还原
还原 电化学法制备甲醇(
电化学法制备甲醇(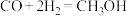 )的工作原理如图所示:
)的工作原理如图所示:
 通过质子膜向
通过质子膜向 的一端发生的电极反应式为
的一端发生的电极反应式为(4)锂钊氧化物电池放电时的总反应:
 ,则其正极充电时的电极反应式为:
,则其正极充电时的电极反应式为:(5)以四甲基氯化铵[(CH3)4NCl]为原料,采用电渗析法合成四甲基氢氧化铵[(CH3)4NOH],其工作原理如图所示(a、b为石墨,c、d、e为离子交换膜),当制备
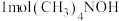 时,a、b两个极共产生
时,a、b两个极共产生 气体。
气体。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据所学有关知识,回答下列问题:
(1)下列说法错误的是_____ 。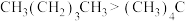
C.化学键的断裂和形成是化学反应中能量变化的主要原因
D.糖类、油脂、蛋白质都是高分子化合物
E.煤的气化、液化和干馏都是物理变化
F.用银来作催化剂,乙烯和氧气反应制取环氧乙烷,原子利用率100%,符合绿色化学理念
G.石英玻璃、碳化硅陶瓷、水泥、石墨烯都是新型无机非金属材料 、
、 、
、 、
、 中既可以用浓
中既可以用浓 干燥,又可以用
干燥,又可以用 固体干燥的是
固体干燥的是_____ 。
(3)三联苯的结构为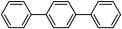 它的一氯代物有
它的一氯代物有_____ 种。
(4)等质量的三种有机物甲烷、乙烯和苯完全燃烧生成 和
和 ,消耗氧气的体积(相同状况下)最多的是
,消耗氧气的体积(相同状况下)最多的是_____ 。
(5)某有机物的键线式为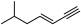 ,该分子最多有
,该分子最多有_____ 个碳原子共面,最多_____ 个碳原子共线。
(6)我国科学家以LiI为催化剂,通过改变盐浓度或溶剂调节锂-硫电流的放电性能。模型装置如图所示。放电时, 向
向_____ 极(填“a”或“b”)迁移,b极反应式为_____ 。
(1)下列说法错误的是
A. 和
和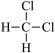 是同种物质,而
是同种物质,而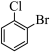 和
和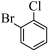 是同分异构体
是同分异构体
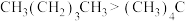
C.化学键的断裂和形成是化学反应中能量变化的主要原因
D.糖类、油脂、蛋白质都是高分子化合物
E.煤的气化、液化和干馏都是物理变化
F.用银来作催化剂,乙烯和氧气反应制取环氧乙烷,原子利用率100%,符合绿色化学理念
G.石英玻璃、碳化硅陶瓷、水泥、石墨烯都是新型无机非金属材料
H.乙烯分子的空间填充模型为
 、
、 、
、 、
、 中既可以用浓
中既可以用浓 干燥,又可以用
干燥,又可以用 固体干燥的是
固体干燥的是(3)三联苯的结构为
 它的一氯代物有
它的一氯代物有(4)等质量的三种有机物甲烷、乙烯和苯完全燃烧生成
 和
和 ,消耗氧气的体积(相同状况下)最多的是
,消耗氧气的体积(相同状况下)最多的是(5)某有机物的键线式为
 ,该分子最多有
,该分子最多有(6)我国科学家以LiI为催化剂,通过改变盐浓度或溶剂调节锂-硫电流的放电性能。模型装置如图所示。放电时,
 向
向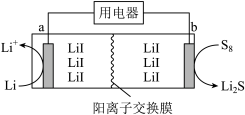
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硫酸是一种重要的化工产品。回答下列问题:
Ⅰ.实验室利用硫酸可以制备一系列气体。
(1)常温下,实验室制备下列气体选择的药品正确的是______(填标号)。
(2)实验室常用食盐和浓硫酸共热500℃制备HCl,另一种产物为正盐,该反应的化学方程式为________ 。不能用浓硫酸制备HBr、HI,其原因是__________________ 。
Ⅱ.硫酸是一种常用的酸性电解质。
(3)在Cu-Zn-H2SO4溶液构成的原电池中,物理量Y与转移电子的关系如图所示。
(4)铅蓄电池的装置如图所示。放电过程的电池反应:PbO2+Pb+2H2SO4=2PbSO4(难溶)+2H2O。________ (填化学式),该极发生_______ (填“氧化”或“还原”)反应。
②正极的电极反应式为______________ 。
③放电时,电解质溶液的pH________ (填“升高”“降低”或“不变”)。
Ⅰ.实验室利用硫酸可以制备一系列气体。
(1)常温下,实验室制备下列气体选择的药品正确的是______(填标号)。
| 选项 | 药品 | 气体 |
| A | FeS、稀硫酸 | H2S |
| B | Na2SO3、10%硫酸 | SO2 |
| C | 粗锌、浓硫酸 | H2 |
| D | 大理石、硫酸 | CO2 |
| A.A | B.B | C.C | D.D |
(2)实验室常用食盐和浓硫酸共热500℃制备HCl,另一种产物为正盐,该反应的化学方程式为
Ⅱ.硫酸是一种常用的酸性电解质。
(3)在Cu-Zn-H2SO4溶液构成的原电池中,物理量Y与转移电子的关系如图所示。
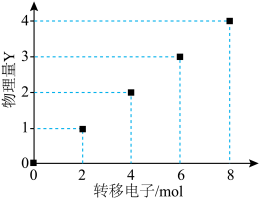
| A.n(Zn) | B.n(H2) | C.n( ) ) | D.n(Zn2+) |
(4)铅蓄电池的装置如图所示。放电过程的电池反应:PbO2+Pb+2H2SO4=2PbSO4(难溶)+2H2O。
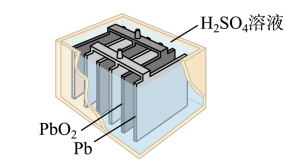
②正极的电极反应式为
③放电时,电解质溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示,A、 B、C、D均为石墨电极,E、F分别为短周期相邻两种活泼金属元素的单质,且E能与NaOH溶液反应。按图示接通电路,反应一段时间。
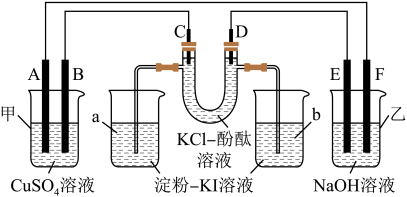
(1)C极为_______ (填“阴极”或 “阳极”), 电极反应式为_______ 。
(2)烧杯中溶液会变蓝的是_______ (填“a”或“b”)
(3)甲池中总反应的离子方程式为_______ 。
(4)乙池中总反应的化学方程式为_______ 。

(1)C极为
(2)烧杯中溶液会变蓝的是
(3)甲池中总反应的离子方程式为
(4)乙池中总反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】纯碱和食盐混合可作家用清洁剂,现欲测定一定质量该清洁剂样品中纯碱的质量分数。回答下列问题:
(1)甲同学利用如图所示装置进行实验。洗气瓶B中盛装的是_______ (填试剂名称),在实验完成时,需要获得的数据是_____ ,装置D的作用是______ 。
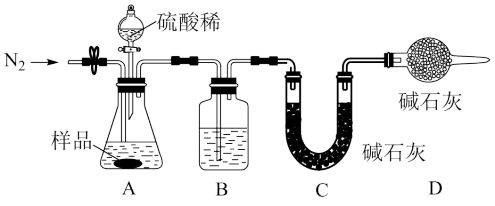
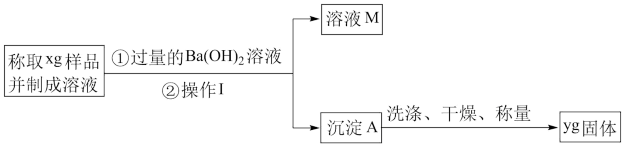
(2)乙同学按照下图所示步骤进行实验。“操作I”的名称为_____ ,“溶液M”中的溶质有_____ (填物质名称),样品中纯碱的质量分数为______ %(用含x、y的代数式表示)。
(1)甲同学利用如图所示装置进行实验。洗气瓶B中盛装的是

(2)乙同学按照下图所示步骤进行实验。“操作I”的名称为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】乙二酸 俗称草酸,在实验研究和化学工业中应用广泛。
俗称草酸,在实验研究和化学工业中应用广泛。
(1)25℃时,向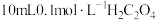 溶液中逐滴加入
溶液中逐滴加入 溶液,溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
溶液,溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:

① 等浓度的Na2C2O4和NaHC2O4混合溶液显_______ 性。(填“酸”“碱”或“中”);25℃时,草酸的电离平衡常数分别是 、
、 ,则
,则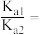
_______ 。
② a点溶液中,
_______ 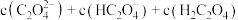 (填“>”“=”或“<”),此时溶液的pH=
(填“>”“=”或“<”),此时溶液的pH=_______ 。
(2)① 酸性高锰酸钾应该用_______ (填“酸式”或“碱式”)滴定管盛装。
② 若要测定草酸亚铁晶体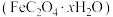 的x值,步骤如下:称取0.5400g草酸亚铁晶体溶于一定浓度的硫酸中,用
的x值,步骤如下:称取0.5400g草酸亚铁晶体溶于一定浓度的硫酸中,用 酸性溶液滴定,达到滴定终点时,消耗
酸性溶液滴定,达到滴定终点时,消耗 的酸性
的酸性 溶液18.00mL。则x=
溶液18.00mL。则x=_______ 。
 俗称草酸,在实验研究和化学工业中应用广泛。
俗称草酸,在实验研究和化学工业中应用广泛。(1)25℃时,向
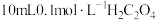 溶液中逐滴加入
溶液中逐滴加入 溶液,溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
溶液,溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
① 等浓度的Na2C2O4和NaHC2O4混合溶液显
 、
、 ,则
,则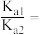
② a点溶液中,

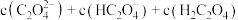 (填“>”“=”或“<”),此时溶液的pH=
(填“>”“=”或“<”),此时溶液的pH=(2)① 酸性高锰酸钾应该用
② 若要测定草酸亚铁晶体
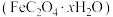 的x值,步骤如下:称取0.5400g草酸亚铁晶体溶于一定浓度的硫酸中,用
的x值,步骤如下:称取0.5400g草酸亚铁晶体溶于一定浓度的硫酸中,用 酸性溶液滴定,达到滴定终点时,消耗
酸性溶液滴定,达到滴定终点时,消耗 的酸性
的酸性 溶液18.00mL。则x=
溶液18.00mL。则x=
您最近一年使用:0次
填空题
|
适中
(0.65)
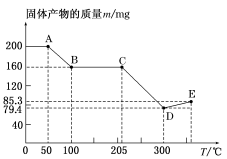
【推荐3】如图是200 mg MnC2O4·2H2O晶体放在坩埚里加热分解时,所得固体产物的质量(m)随温度(T)变化的曲线(已知草酸锰不稳定,但其中锰元素的化合价在300 ℃以下不变)。
试回答下列问题:
(1)写出B点固体产物的化学式:_________________________________________ 。
(2)从B点到C点过程中固体物质质量不变的原因是
________________________________________________________________________ 。
(3)通过计算确定D点产物的相对分子质量,并推断其合理的化学式:____________________________________________________________________________________ 。
(4)从D点到E点过程中固体物质质量增加的原因是___________________________________________________________________________________________________ 。

试回答下列问题:
(1)写出B点固体产物的化学式:
(2)从B点到C点过程中固体物质质量不变的原因是
(3)通过计算确定D点产物的相对分子质量,并推断其合理的化学式:
(4)从D点到E点过程中固体物质质量增加的原因是
您最近一年使用:0次