下表为元素周期表的短周期部分,①~⑦代表七种短周期元素。
已知:⑤的焰色试验火焰呈黄色。
请填写下列空白:
(1)②在元素周期表中的位置为___________ ;①的原子结构示意图为___________ ;③的核电荷数为___________ 。
(2)③的一种核素的中子数为10,其原子符号为___________ (用 形式表示)。
形式表示)。
(3)④和⑦中非金属性较弱的是___________ (填元素符号,下同),氢化物稳定性较强的是___________ 。
(4)①和⑤中原子半径较大的是___________ (填元素符号),⑤和③的最简单氢化物反应的离子方程式为___________ 。
(5)将⑥加入⑤的最高价氧化物对应水化物的溶液中,发生反应的离子方程式为___________ 。
| ① | ② | ③ | ④ | |||
| ⑤ | ⑥ | ⑦ |
请填写下列空白:
(1)②在元素周期表中的位置为
(2)③的一种核素的中子数为10,其原子符号为
 形式表示)。
形式表示)。(3)④和⑦中非金属性较弱的是
(4)①和⑤中原子半径较大的是
(5)将⑥加入⑤的最高价氧化物对应水化物的溶液中,发生反应的离子方程式为
更新时间:2022-01-05 18:02:41
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
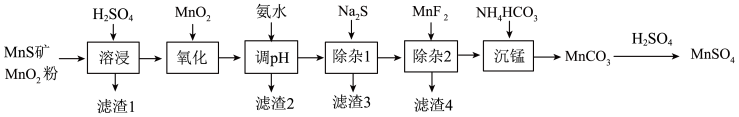
相关金属离子[c(Mn+)=0.1mol/L]形成氢氧化物沉淀的pH范围如下:
(1)Fe2+的价电子排布式为_______ ,在元素周期表中Zn处于_______ 区。
(2)“滤渣1”含有S和_______ ;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式_______ 。
(3)“氧化”中添加适量的MnO2的作用是_______ 。
(4)“调pH”除铁和铝,溶液的pH范围应调节为_______ ~6之间。
(5)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是_______ 。
(6)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_______ 。
(7)写出“沉锰”的离子方程式_______ 。
(8)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y= 时,z=
时,z=_______ 。

相关金属离子[c(Mn+)=0.1mol/L]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)Fe2+的价电子排布式为
(2)“滤渣1”含有S和
(3)“氧化”中添加适量的MnO2的作用是
(4)“调pH”除铁和铝,溶液的pH范围应调节为
(5)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是
(6)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
(7)写出“沉锰”的离子方程式
(8)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=
 时,z=
时,z=
您最近一年使用:0次
【推荐2】环境问题已成为全球普遍的热门话题。
(1)利用甲烷催化还原氨氧化物。已知:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g) △H1=-867kJ∙mol-1,CH4(g) +4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H2=-574kJ∙mol-1,则CH4将NO还原为N2的热化学方程式为___ 。
(2)用NH3催化还原NOX也可以消除氮氧化物的污染.如图采用NH3作还原剂,烟气以一定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物转化率),反应原理为:NO(g) +NO2(g) +2NH3(g) ⇌2N2(g)+3H2O(g)。
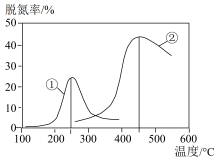
①该反应的△S___ 0,△H___ 0(填“>”、“=”或“<”)。
②对于气体反应,用某组分(B)的平衡压强(pB )代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则上述反应的Kp=______ 。
③以下说法正确的是___ (填标号)。
A.第②种催化剂比第①种催化剂脱氮率高
B.相同条件下,改变压强对脱氮率没有影响
C.催化剂①、②分别适合于250℃和450℃左右脱氮
(3)催化反硝化法和电化学沉解法可用于治理水中硝酸盐的污染。
①催化反硝化法中,用H2能NO3-还原为N2,一段时间后,溶液的碱性明显增强,则反应离子方程式为____ 。
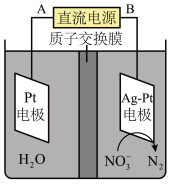
②电化学降解NO3-的原理如图所示。电源正极为______ (填A或B),阴极反应式为______ 。
(1)利用甲烷催化还原氨氧化物。已知:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g) △H1=-867kJ∙mol-1,CH4(g) +4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H2=-574kJ∙mol-1,则CH4将NO还原为N2的热化学方程式为
(2)用NH3催化还原NOX也可以消除氮氧化物的污染.如图采用NH3作还原剂,烟气以一定的流速通过两种不同催化剂,测量逸出气体中氮氧化物含量,从而确定烟气脱氮率(注:脱氮率即氮氧化物转化率),反应原理为:NO(g) +NO2(g) +2NH3(g) ⇌2N2(g)+3H2O(g)。

①该反应的△S
②对于气体反应,用某组分(B)的平衡压强(pB )代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则上述反应的Kp=
③以下说法正确的是
A.第②种催化剂比第①种催化剂脱氮率高
B.相同条件下,改变压强对脱氮率没有影响
C.催化剂①、②分别适合于250℃和450℃左右脱氮
(3)催化反硝化法和电化学沉解法可用于治理水中硝酸盐的污染。
①催化反硝化法中,用H2能NO3-还原为N2,一段时间后,溶液的碱性明显增强,则反应离子方程式为
②电化学降解NO3-的原理如图所示。电源正极为

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】有一包白色粉末A,由 、
、 、
、 、
、 、NaOH中的两种或两种以上物质混合而成,为探究其组成,进行如下实验:
、NaOH中的两种或两种以上物质混合而成,为探究其组成,进行如下实验:
①加水搅拌溶解,有白色沉淀B生成,过滤得无色溶液C;
②取白色沉淀B于试管中,加入足量的稀盐酸,沉淀全部溶解且有无色气体放出;
③另取无色溶液C,通入一定量的 ,有白色沉淀D生成,过滤得无色滤液E。
,有白色沉淀D生成,过滤得无色滤液E。
(1)以上实验可判断出原白色粉末中一定含有___________ (填化学式,下同),一定不含有___________ ;
(2)若无色滤液E中只含有一种溶质,该溶质为___________ 。
(3)白色沉淀D的化学式为___________ ;
(4)写出生成白色沉淀D的离子方程式___________ 。
 、
、 、
、 、
、 、NaOH中的两种或两种以上物质混合而成,为探究其组成,进行如下实验:
、NaOH中的两种或两种以上物质混合而成,为探究其组成,进行如下实验:①加水搅拌溶解,有白色沉淀B生成,过滤得无色溶液C;
②取白色沉淀B于试管中,加入足量的稀盐酸,沉淀全部溶解且有无色气体放出;
③另取无色溶液C,通入一定量的
 ,有白色沉淀D生成,过滤得无色滤液E。
,有白色沉淀D生成,过滤得无色滤液E。(1)以上实验可判断出原白色粉末中一定含有
(2)若无色滤液E中只含有一种溶质,该溶质为
(3)白色沉淀D的化学式为
(4)写出生成白色沉淀D的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】短周期主族元素A、B、C、D、E原子序数依次增大。A、E同主族,E原子最外层上的电子数是D原子最外层电子数的4倍,D离子与C2-具有相同核外电子排布。
试回答下列问题:
(1)元素E在元素周期表中的位置是______ 。
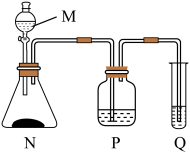
(2)A和E最高价氧化物对应的水化物,酸性较弱的为_____ 。若用图中装置验证这两种酸的酸性强弱,则在仪器P中加入的试剂为_____ ,Q中观察到的实验现象是_____ 。
(3)由以上五种元素组成的物质,其组成和结构信息如下表:
①a含有的化学键有_____ 。
②b与c反应的化学方程式为_____ 。

试回答下列问题:
(1)元素E在元素周期表中的位置是
(2)A和E最高价氧化物对应的水化物,酸性较弱的为
(3)由以上五种元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A、C、D的盐 |
| b | C、D组成的化合物,且原子数之比为1∶1 |
| c | 化学组成为AC2 |
②b与c反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)D﹣的结构示意图是______ 。
(2)C元素的气态氢化物的化学式为:_____ ;其检验方法:___ 。
(3)B元素在周期表中的位置___ ;离子半径:B___ A(填“大于”或“小于”)。
(4)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为_________
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(1)D﹣的结构示意图是
(2)C元素的气态氢化物的化学式为:
(3)B元素在周期表中的位置
(4)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】有A、B、C、D、E五种元素。其中A为第三周期主族元素,与D可形成原子个数比为1∶1和2∶1的化合物;B为第4周期过渡金属元素,且未成对电子数最多,最高化合价为+6价;C和A是同周期的元素,最高化合价为+7;D原子的价电子排布为nsnnpn+2,E元素的基态原子核外有7个原子轨道填充了电子。
(1)写出下面三种元素的元素符号:A___________ 、B___________ 、C___________ 。
(2)写出D2-的电子排布式:___________ 。基态E原子的外围电子排布图___________ 。
(3)C位于___________ 族,B位于___________ 区。
(1)写出下面三种元素的元素符号:A
(2)写出D2-的电子排布式:
(3)C位于
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】已知:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
MnCl2+Cl2↑+2H2O,2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
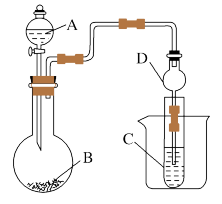
(1)仪器A的名称为_____ ,D的作用是_____ 。
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验,验证氯的非金属性强于硫的非金属性。装置A、B、C中所装药品分别为____ 、____ 、____ ,装置C中的实验现象为有淡黄色沉淀生成,C中发生的化学反应方程式为____ 。
 MnCl2+Cl2↑+2H2O,2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
MnCl2+Cl2↑+2H2O,2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
(1)仪器A的名称为
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验,验证氯的非金属性强于硫的非金属性。装置A、B、C中所装药品分别为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置。
Ⅰ.第一代电池的光电转换材料是单晶硅。某单晶硅制备工艺中涉及的主要物质转化如下:___________ (填字母)。
a.ⅰ中,C做还原剂
b.碳酸的酸性强于硅酸
c.碳酸的热稳定性弱于硅酸
(2)ⅱ中,1mol Si与3mol HCl反应转移4mol电子。
①该反应的化学方程式为___________ 。
② 中,H的化合价为
中,H的化合价为___________ ,由此推测Si的电负性比H的___________ (填“大”或“小”)。
(3)ⅲ中,利用沸点差异,可直接实现高纯硅与 的分离,从晶体类型角度解释其原因:
的分离,从晶体类型角度解释其原因:___________ 。
Ⅱ.第二代电池的光电转换材料是一种无机物薄膜,其光电转化率高于单晶硅。科学家在元素周期表中Si的附近寻找到元素A和D,并制成化合物AD的薄膜,其晶体结构类似单晶硅。Si、A、D在元素周期表中的位置关系如图所示。
(4)基态A原子核外电子排布式为___________ 。
(5)D的第一电离能比Se的大,从原子结构角度说明理由:___________ 。
Ⅰ.第一代电池的光电转换材料是单晶硅。某单晶硅制备工艺中涉及的主要物质转化如下:

a.ⅰ中,C做还原剂
b.碳酸的酸性强于硅酸
c.碳酸的热稳定性弱于硅酸
(2)ⅱ中,1mol Si与3mol HCl反应转移4mol电子。
①该反应的化学方程式为
②
 中,H的化合价为
中,H的化合价为(3)ⅲ中,利用沸点差异,可直接实现高纯硅与
 的分离,从晶体类型角度解释其原因:
的分离,从晶体类型角度解释其原因:Ⅱ.第二代电池的光电转换材料是一种无机物薄膜,其光电转化率高于单晶硅。科学家在元素周期表中Si的附近寻找到元素A和D,并制成化合物AD的薄膜,其晶体结构类似单晶硅。Si、A、D在元素周期表中的位置关系如图所示。
| Si | ||
| A | D |
(4)基态A原子核外电子排布式为
(5)D的第一电离能比Se的大,从原子结构角度说明理由:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】元素周期表是学习物质结构和性质的重要工具。下表是元素周期表的一部分,表中所列序号代表对应的元素。请回答下列问题:_______ (填元素符号),元素⑧在周期表中的位置是_______ 。
(2)由上述元素形成的最高价氧化物对应的水化物中,酸性最强的是_______ (填物质名称)。
(3)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是_______ (填离子符号)。
(4)①与⑤可形成 微粒,写出该微粒的电子式:
微粒,写出该微粒的电子式:_______ 。
(5)欲比较⑤与⑥的非金属性强弱,下列说法可作为判断依据的是_______ (填标号)。
a.比较⑤、⑥两种元素单质的沸点高低
b.比较⑤、⑥两种元素单质与 化合的难易程度
化合的难易程度
c.比较⑤、⑥两种元素气态氢化物的稳定性
d.比较⑤、⑥两种元素的氧化物对应水化物的酸性强弱
(6)元素③和④的金属性:③_______ ④(填“>”或“<”),元素④的单质可与元素③的最高价氧化物的水化物反应,写出该反应的化学方程式:_______ 。

(2)由上述元素形成的最高价氧化物对应的水化物中,酸性最强的是
(3)表中某些元素的原子可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是
(4)①与⑤可形成
 微粒,写出该微粒的电子式:
微粒,写出该微粒的电子式:(5)欲比较⑤与⑥的非金属性强弱,下列说法可作为判断依据的是
a.比较⑤、⑥两种元素单质的沸点高低
b.比较⑤、⑥两种元素单质与
 化合的难易程度
化合的难易程度c.比较⑤、⑥两种元素气态氢化物的稳定性
d.比较⑤、⑥两种元素的氧化物对应水化物的酸性强弱
(6)元素③和④的金属性:③
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】 、
、 、
、 、
、 、
、 是元素周期表中前20号的主族元素,它们的原子序数依次增大。
是元素周期表中前20号的主族元素,它们的原子序数依次增大。 原子的
原子的 层电子数是其
层电子数是其 层电子数的3倍,
层电子数的3倍, 是短周期金属性最强的元素,
是短周期金属性最强的元素, 是地壳中含量最多的金属元素,
是地壳中含量最多的金属元素, 与
与 同主族。回答下列问题:
同主族。回答下列问题:
(1) 在元素周期表中的位置为
在元素周期表中的位置为___________ ; 、
、 非金属性较强的是
非金属性较强的是___________ (填元素符号)。
(2) 、
、 简单离子半径较小的是
简单离子半径较小的是___________ (填离子符号)。
(3) 、
、 最高价氧化物对应水化物的碱性较弱的是
最高价氧化物对应水化物的碱性较弱的是___________ (填化学式)。
(4) 、
、 最高价氧化物对应水化物之间反应的化学方程式为
最高价氧化物对应水化物之间反应的化学方程式为___________ 。
 、
、 、
、 、
、 、
、 是元素周期表中前20号的主族元素,它们的原子序数依次增大。
是元素周期表中前20号的主族元素,它们的原子序数依次增大。 原子的
原子的 层电子数是其
层电子数是其 层电子数的3倍,
层电子数的3倍, 是短周期金属性最强的元素,
是短周期金属性最强的元素, 是地壳中含量最多的金属元素,
是地壳中含量最多的金属元素, 与
与 同主族。回答下列问题:
同主族。回答下列问题:(1)
 在元素周期表中的位置为
在元素周期表中的位置为 、
、 非金属性较强的是
非金属性较强的是(2)
 、
、 简单离子半径较小的是
简单离子半径较小的是(3)
 、
、 最高价氧化物对应水化物的碱性较弱的是
最高价氧化物对应水化物的碱性较弱的是(4)
 、
、 最高价氧化物对应水化物之间反应的化学方程式为
最高价氧化物对应水化物之间反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表是元素周期表一部分,针对表中的①~⑧种元素,请按要求填写下列空白:
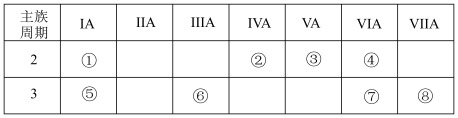
(1)在元素①⑤⑥对应的最高价氧化物对应水化物中,碱性最强的化合物电子式是:_______ 。
(2)④⑤⑥⑦四种元素的简单离子半径从大到小排序_______ (用离子符号表示)。
(3)写出元素⑥的最高价氧化物与元素⑤的最高价氧化物对应的水化物反应的离子反应方程式_______ 。
(4)写出元素③的常见氢化物和它的最高价氧化物对应的水化物反应的化学反应方程式_____ 。
(5)用电子式来表示⑤与⑦组成化合物的形成过程_______ 。

(1)在元素①⑤⑥对应的最高价氧化物对应水化物中,碱性最强的化合物电子式是:
(2)④⑤⑥⑦四种元素的简单离子半径从大到小排序
(3)写出元素⑥的最高价氧化物与元素⑤的最高价氧化物对应的水化物反应的离子反应方程式
(4)写出元素③的常见氢化物和它的最高价氧化物对应的水化物反应的化学反应方程式
(5)用电子式来表示⑤与⑦组成化合物的形成过程
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】下表列出了①~⑩十种元素在周期表中的位置。
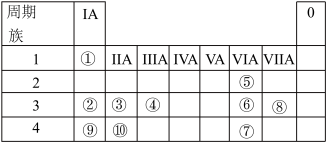
请用化学用语和必要的文字按要求回答下列问题:
(1)写出①的同位素氘的原子符号___ ;元素③和⑧形成的化合物中的化学键类型为___ ,用电子式表示其形成过程___ ;元素①、⑤和⑧形成的三原子化合物的电子式为___ 。
(2)①-⑩元素最高价氧化物对应的水化物酸性最强的是___ (填化学式),碱性最强的是___ (填化学式),呈两性的氧化物与强碱反应的离子方程式为___ 。
(3)元素⑤、⑥、⑦的单质氧化性依次___ (填“增强”或“减弱”),其气态氢化物中稳定性最弱的是___ 。(均填化学式)
(4)②③④⑥⑧元素原子半径由大到小的顺序为___ ;①~⑥元素能形成10电子简单离子中半径最大的是___ 。(均用化学符号表示)

请用化学用语和必要的文字按要求回答下列问题:
(1)写出①的同位素氘的原子符号
(2)①-⑩元素最高价氧化物对应的水化物酸性最强的是
(3)元素⑤、⑥、⑦的单质氧化性依次
(4)②③④⑥⑧元素原子半径由大到小的顺序为
您最近一年使用:0次



