有A、B、C、D、E五种元素。其中A为第三周期主族元素,与D可形成原子个数比为1∶1和2∶1的化合物;B为第4周期过渡金属元素,且未成对电子数最多,最高化合价为+6价;C和A是同周期的元素,最高化合价为+7;D原子的价电子排布为nsnnpn+2,E元素的基态原子核外有7个原子轨道填充了电子。
(1)写出下面三种元素的元素符号:A___________ 、B___________ 、C___________ 。
(2)写出D2-的电子排布式:___________ 。基态E原子的外围电子排布图___________ 。
(3)C位于___________ 族,B位于___________ 区。
(1)写出下面三种元素的元素符号:A
(2)写出D2-的电子排布式:
(3)C位于
更新时间:2024-05-08 21:36:42
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】短周期元素A、B、C、D,A元素的原子最外层电子数是内层电子数的两倍,B为地壳中含量最多的元素,C是原子半径最大的短周期主族元素,C与D形成的离子化合物CD是常用的调味品。填写下列空白:
(1)C元素在周期表中的位置是_______ 。
(2)B、C组成的一种化合物与水发生反应生成气体,其化学方程式为:_______ 。
(3)如图所示,电解质a溶液为含有CD的饱和溶液。X、Y均为石墨电极,接通直流电源。

X电极的电极反应式为_______ 。电解池总反应的离子方程式为:_______ 。
(1)C元素在周期表中的位置是
(2)B、C组成的一种化合物与水发生反应生成气体,其化学方程式为:
(3)如图所示,电解质a溶液为含有CD的饱和溶液。X、Y均为石墨电极,接通直流电源。

X电极的电极反应式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】X、Y、Z、R、Q是五种短周期元素,原子序数依次增大。X是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z为地壳中含量最多的元素,X、Y、R最外层电子数之和为8,Q的单质为黄绿色有害气体。请回答下列问题:
(1)Z在元素周期表中的位置为________ 。
(2)Y和Z元素的原子半径由大到小的顺序为_____ (写元素符号)。Y和Z的气态氢化物中稳定性较强的是_______ (填化学式)。
(3) Y单质的电子式为________ 。
(4)Y的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式_______ 。
(1)Z在元素周期表中的位置为
(2)Y和Z元素的原子半径由大到小的顺序为
(3) Y单质的电子式为
(4)Y的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式
您最近一年使用:0次
【推荐3】元素周期表前四周期的A、B、C、D、E五种元素,A元素的原子最外层电子排布式为ns1;B元素的原子价电子排布式为ns2np2;C元素位于第二周期且原子中p能级与s能级的电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素原子有5个未成对电子。
(1)写出下列元素的名称:
C___________ ;D_______ ;E_______ 。
(2)基态C原子的电子排布图为_____ 。
(3)当n=2时,B的最简单气态氢化物的电子式为_____ ,BC2分子的结构式为_____ ;当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是_________ 。
(4)若A元素的原子价电子排布式为2s1,B元素的原子价电子排布式为3s23p2,A、B、C、D四种元素的第一电离能由大到小的顺序是_____ (用元素符号表示)。
(5)E元素在元素周期表中的位置是______ ,其最高价氧化物的化学式是_____ 。
(1)写出下列元素的名称:
C
(2)基态C原子的电子排布图为
(3)当n=2时,B的最简单气态氢化物的电子式为
(4)若A元素的原子价电子排布式为2s1,B元素的原子价电子排布式为3s23p2,A、B、C、D四种元素的第一电离能由大到小的顺序是
(5)E元素在元素周期表中的位置是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题:
(1)与 同族且相邻周期的元素
同族且相邻周期的元素 的基态原子价电子排布式为
的基态原子价电子排布式为___________ 。与钛同周期元素的基态原子中,未成对电子数与钛相同的元素有___________ 种。
(2)①基态S原子的价电子中,两种自旋状态的电子数之比为___________ 。
②根据“相似相溶”规律推测硫单质易溶于下列哪些溶剂_________ 。
A.水 B. C.
C.
(3) 分子中B为
分子中B为 杂化,且存在两个硼氧单键,画出
杂化,且存在两个硼氧单键,画出 的结构式
的结构式___________ ,该分子的空间构型为___________ ;硼砂阴离子的结构如图所示,分析B原子的杂化方式为___________ 。
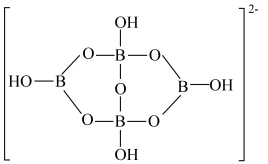
(1)与
 同族且相邻周期的元素
同族且相邻周期的元素 的基态原子价电子排布式为
的基态原子价电子排布式为(2)①基态S原子的价电子中,两种自旋状态的电子数之比为
②根据“相似相溶”规律推测硫单质易溶于下列哪些溶剂
A.水 B.
 C.
C.
(3)
 分子中B为
分子中B为 杂化,且存在两个硼氧单键,画出
杂化,且存在两个硼氧单键,画出 的结构式
的结构式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】X、Y、Z、W是元素周期表前四周期中的常见元素,其原子序数依次增大。X元素的一种核素的质量数为12,中子数为6;Y元素是动植物生长不可缺少的、构成蛋白质的重要组成元素;Z的基态原子核外9个原子轨道上填充了电子且有2个未成对电子,与X不同族;W是一种常见元素,可以形成3种氧化物,其中一种氧化物是具有磁性的黑色晶体。
(1)写出下列元素的名称:X_______ ,Y_______ ,Z_______ 。
(2)X—H和Y—H属于极性共价键,其中极性较强的是_______ (X、Y用元素符号表示)。X的第一电离能比Y的_______ (填“大”或“小”)。
(3)X的最简单氢化物的空间结构为_______ 形,该分子为_______ (填“极性分子”或“非极性分子”)。
(4)基态Y元素的核外未成对的电子有___ 个,基态Y元素的电子轨道表示式为_____ 。
(1)写出下列元素的名称:X
(2)X—H和Y—H属于极性共价键,其中极性较强的是
(3)X的最简单氢化物的空间结构为
(4)基态Y元素的核外未成对的电子有
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】请按要求填空:
(1)下列轨道表示式能表示基态氮原子的是___________(填标号)。
(2)HCHO的中心原子的价层电子对数为___________ ;其中基态氧原子的核外电子的空间运动状态有___________ 种。
(3)已知邻羟基苯甲酸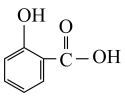 与对羟基苯甲酸
与对羟基苯甲酸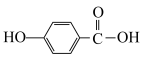 的沸点相差较大,根据结构分析,前者的沸点
的沸点相差较大,根据结构分析,前者的沸点___________ (填高于”或“低于”)后者,并解释原因:___________ 。
(4)普鲁士蓝{KFe[Fe(CN)6]}中不同价态铁元素的简单微粒较稳定的离子的简化核外电子排布式为___________ ,该离子更稳定的原因是___________ 。
(1)下列轨道表示式能表示基态氮原子的是___________(填标号)。
A.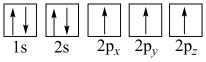 | B. |
C. | D. |
(2)HCHO的中心原子的价层电子对数为
(3)已知邻羟基苯甲酸
 与对羟基苯甲酸
与对羟基苯甲酸 的沸点相差较大,根据结构分析,前者的沸点
的沸点相差较大,根据结构分析,前者的沸点(4)普鲁士蓝{KFe[Fe(CN)6]}中不同价态铁元素的简单微粒较稳定的离子的简化核外电子排布式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】镓(Ga)是一种重要的金属,镓的化合物广泛应用于半导体、太阳能、液态合金、医疗化工等诸多领域,被称为电子工业的“脊梁”。
(1)基态Ga原子的价层电子的轨道表示式是___________________ 。
(2) 在270°C左右以二聚体
在270°C左右以二聚体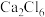 存在,结构式如图。
存在,结构式如图。
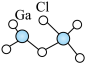
① 可以形成二聚体的原因是
可以形成二聚体的原因是__________________________ 。
② 和
和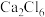 中Ga原子采用的杂化方式分别是
中Ga原子采用的杂化方式分别是_________________ 。
③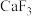 的熔点为1000℃,
的熔点为1000℃, 的熔点为77.9℃,
的熔点为77.9℃,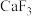 的熔点远远高于
的熔点远远高于 的熔点,从结构角度解释原因
的熔点,从结构角度解释原因_____ 。
(3) 可与
可与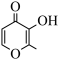 (甲基麦芽酚)形成配合物Ga(
(甲基麦芽酚)形成配合物Ga( )3。甲基麦芽酚的分子式是
)3。甲基麦芽酚的分子式是______________ ,甲基麦芽酚中,与 形成配位键的原子是
形成配位键的原子是________ 。
(1)基态Ga原子的价层电子的轨道表示式是
(2)
 在270°C左右以二聚体
在270°C左右以二聚体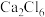 存在,结构式如图。
存在,结构式如图。
①
 可以形成二聚体的原因是
可以形成二聚体的原因是②
 和
和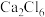 中Ga原子采用的杂化方式分别是
中Ga原子采用的杂化方式分别是③
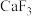 的熔点为1000℃,
的熔点为1000℃, 的熔点为77.9℃,
的熔点为77.9℃,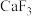 的熔点远远高于
的熔点远远高于 的熔点,从结构角度解释原因
的熔点,从结构角度解释原因(3)
 可与
可与 (甲基麦芽酚)形成配合物Ga(
(甲基麦芽酚)形成配合物Ga( )3。甲基麦芽酚的分子式是
)3。甲基麦芽酚的分子式是 形成配位键的原子是
形成配位键的原子是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】我国科研工作者研究的金属-氮-碳优异电催化CO2 还原催化剂取得新进展。回答下列问题:
(1)14C 可用于考古,该基态原子价层电子轨道表示式为_______ 。
(2)研究发现钴-氮-碳优异电催化CO2 还原催化剂活性最高,金属钴的核外电子排布式为_______ ;基态Co中未成对电子数为_______ 。
(3)基态N原子中,电子占据的最高能层符号为_______ ,该能层具有的原子轨道数为_______ ,电子数为_______ 。
(4)基态铝原子核外共有_______ 种不同能级的电子,有_______ 种不同运动状态的电子。
(1)14C 可用于考古,该基态原子价层电子轨道表示式为
(2)研究发现钴-氮-碳优异电催化CO2 还原催化剂活性最高,金属钴的核外电子排布式为
(3)基态N原子中,电子占据的最高能层符号为
(4)基态铝原子核外共有
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】由于铁氮化合物具有非常优异的磁性能、机械性能和耐腐蚀性,受到研究人员的广泛关注。γˊ−Fe4N是一种性能优异的铁氮化合物,其可由氨气与羰基铁粉[Fe(CO)5]反应得到。
(1)Fe变为Fe2+时是失去___________ 轨道电子,Fe3+价层电子排布图为___________ 。
(2)氨气中N的杂化类型是___________ ,NH3中H−N−H的键角比NH4+中H−N−H的键角___________ (填“大”或“小”),理由是___________ 。
(3) 与CO中均存在化学键的类型有
与CO中均存在化学键的类型有___________ (填标号)。
A.离子键 B.氢键 C.配位键 D.共价键 E.金属键
(4)羰基铁粉[Fe(CO)5]中铁元素的配位数是___________ ,配位原子为___________ 。
(5)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为___________ 。
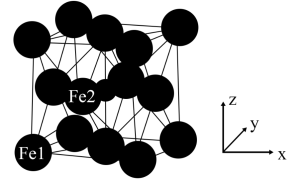
(6)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为( ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为___________ 。已知该晶体的密度为dg/cm3,阿伏加德罗常数的值为NA,则晶胞参数a为___________ nm(用含d和NA的代数式表示)。
(1)Fe变为Fe2+时是失去
(2)氨气中N的杂化类型是
(3)
 与CO中均存在化学键的类型有
与CO中均存在化学键的类型有A.离子键 B.氢键 C.配位键 D.共价键 E.金属键
(4)羰基铁粉[Fe(CO)5]中铁元素的配位数是
(5)氨气与羰基铁粉的反应中涉及元素电负性由大到小的顺序为
(6)γ−Fe4N的晶胞如图所示,设晶胞中Fe1点的原子坐标为(0,0,0),N点的原子坐标为(
 ,
, ,
, ),则Fe2点的原子坐标为
),则Fe2点的原子坐标为
您最近一年使用:0次



