面对新冠病毒,VB空气防护卡也成了“网红”,成为人们讨论的话题。商品介绍卡片中含有的主要活性成分——亚氯酸钠,在接触空气时可以释放安全可靠的低浓度二氧化氯( ),从而达到消除病毒、细菌活性的防护效果。
),从而达到消除病毒、细菌活性的防护效果。 的一种生产工艺如下:
的一种生产工艺如下:
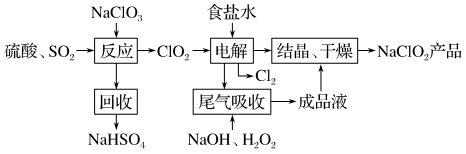
回答下列问题:
(1)写出“反应”步骤中生成 的化学反应方程式:
的化学反应方程式:_______ 。
(2)“电解”所用食盐水由粗盐水精制而成,精制时,为除去 、
、 、
、 ,要加入的试剂分别为
,要加入的试剂分别为_______ 、_______ 、_______ ,为得到纯净的NaCl溶液还需加入_______ (以上填写相应物质的化学式)。
(3)“电解”产生的 可用于工业制漂白液,写出离子反应方程式:
可用于工业制漂白液,写出离子反应方程式:_______ 。
(4)“尾气吸收”是吸收“电解”过程排出的少量 ,此吸收反应中,氧化剂与还原剂的物质的量之比为
,此吸收反应中,氧化剂与还原剂的物质的量之比为_______ ,该反应中还原产物是_______ 。
(5)有同学推测VB空气防护卡原理是因为 与空气中的
与空气中的 发生反应得到
发生反应得到 ,同时得到钠的两种正盐,试写出相应的化学反应方程式:
,同时得到钠的两种正盐,试写出相应的化学反应方程式:_______ 。
 ),从而达到消除病毒、细菌活性的防护效果。
),从而达到消除病毒、细菌活性的防护效果。 的一种生产工艺如下:
的一种生产工艺如下:
回答下列问题:
(1)写出“反应”步骤中生成
 的化学反应方程式:
的化学反应方程式:(2)“电解”所用食盐水由粗盐水精制而成,精制时,为除去
 、
、 、
、 ,要加入的试剂分别为
,要加入的试剂分别为(3)“电解”产生的
 可用于工业制漂白液,写出离子反应方程式:
可用于工业制漂白液,写出离子反应方程式:(4)“尾气吸收”是吸收“电解”过程排出的少量
 ,此吸收反应中,氧化剂与还原剂的物质的量之比为
,此吸收反应中,氧化剂与还原剂的物质的量之比为(5)有同学推测VB空气防护卡原理是因为
 与空气中的
与空气中的 发生反应得到
发生反应得到 ,同时得到钠的两种正盐,试写出相应的化学反应方程式:
,同时得到钠的两种正盐,试写出相应的化学反应方程式:
更新时间:2022-01-19 09:31:21
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】一化学兴趣小组的同学通过如下实验提取海带中的碘:
①粉碎海带,加一定量的氢氧化钾溶液后高温灰化;
②用水浸泡海带灰,过滤;
③用盐酸酸化滤液,加入碘酸钾(KIO3)氧化溶液中的碘离子(I—),生成碘单质;
④用四氯化碳溶液萃取水溶液中的碘。
请回答下列问题:
(1)实验步骤③中相关的化学反应的方程式为_____________________________
(2)实验步骤③中也可用H2O2代替KIO3,相关化学反应的方程式为_____________________________________________________________________________ 。
(3)检验用四氯化碳萃取碘后的水溶液是否还有碘单质的实验方法是__________________________________________________________________________________________ 。
①粉碎海带,加一定量的氢氧化钾溶液后高温灰化;
②用水浸泡海带灰,过滤;
③用盐酸酸化滤液,加入碘酸钾(KIO3)氧化溶液中的碘离子(I—),生成碘单质;
④用四氯化碳溶液萃取水溶液中的碘。
请回答下列问题:
(1)实验步骤③中相关的化学反应的方程式为
(2)实验步骤③中也可用H2O2代替KIO3,相关化学反应的方程式为
(3)检验用四氯化碳萃取碘后的水溶液是否还有碘单质的实验方法是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】碱式氧化镍是镍电池的正极活性材料。利用镍渣(主要含NiO,及少量 、CuO、CaO、
、CuO、CaO、 等杂质)制备碱式氧化镍的流程如下:
等杂质)制备碱式氧化镍的流程如下:
(2)浸渣的主要成分除CaSO4外还有______ 。
(3)“沉铜”过程中生成单质S的离子方程式为______ 。
(4)“氧化”中的目的是将 氧化为
氧化为 ,若试剂R选用
,若试剂R选用 ,写出“氧化”时反应的离子方程式:
,写出“氧化”时反应的离子方程式:_______ 。
(5)碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,电池的总反应为
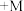 ,其工作时的正极电极反应式为
,其工作时的正极电极反应式为_______ 。
 、CuO、CaO、
、CuO、CaO、 等杂质)制备碱式氧化镍的流程如下:
等杂质)制备碱式氧化镍的流程如下:
| A.研磨废料 | B.加入大量水 | C.搅拌 | D.适当升高温度 |
(3)“沉铜”过程中生成单质S的离子方程式为
(4)“氧化”中的目的是将
 氧化为
氧化为 ,若试剂R选用
,若试剂R选用 ,写出“氧化”时反应的离子方程式:
,写出“氧化”时反应的离子方程式:(5)碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,电池的总反应为

 ,其工作时的正极电极反应式为
,其工作时的正极电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐3】硫酸亚铁是一种补铁剂,某兴趣小组利用经过初步处理的含有 的废液制备硫酸亚铁晶体,其流程如下:
的废液制备硫酸亚铁晶体,其流程如下:
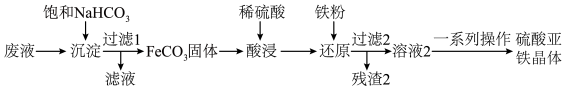
回答下列问题:
(1)配制250 mL 0.5 mol∙L−1 溶液时主要用到的玻璃仪器有250 mL容量瓶、烧杯、玻璃棒、量筒和
溶液时主要用到的玻璃仪器有250 mL容量瓶、烧杯、玻璃棒、量筒和_______ ,玻璃棒的作用为_______ 。
(2) 和
和 反应生成
反应生成 ,该反应为非氧化还原反应,反应的离子方程式为
,该反应为非氧化还原反应,反应的离子方程式为_______ 。
(3)“酸浸”时通常将 固体进行粉碎,原因为
固体进行粉碎,原因为_______ 。
(4)酸性条件下, 能被
能被 氧化,该反应的氧化产物与还原产物的物质的量之比为
氧化,该反应的氧化产物与还原产物的物质的量之比为_______ 。
(5)酸化的重铬酸钾溶液与 可发生反应:_______
可发生反应:_______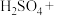 _______
_______ _______
_______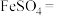 _______
_______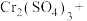 _______
_______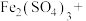 _______
_______ _______
_______ (未配平)。
(未配平)。
①配平上述化学方程式:_______ 。
②用单线桥法表示出电子转移的过程:_______ 。
 的废液制备硫酸亚铁晶体,其流程如下:
的废液制备硫酸亚铁晶体,其流程如下:
回答下列问题:
(1)配制250 mL 0.5 mol∙L−1
 溶液时主要用到的玻璃仪器有250 mL容量瓶、烧杯、玻璃棒、量筒和
溶液时主要用到的玻璃仪器有250 mL容量瓶、烧杯、玻璃棒、量筒和(2)
 和
和 反应生成
反应生成 ,该反应为非氧化还原反应,反应的离子方程式为
,该反应为非氧化还原反应,反应的离子方程式为(3)“酸浸”时通常将
 固体进行粉碎,原因为
固体进行粉碎,原因为(4)酸性条件下,
 能被
能被 氧化,该反应的氧化产物与还原产物的物质的量之比为
氧化,该反应的氧化产物与还原产物的物质的量之比为(5)酸化的重铬酸钾溶液与
 可发生反应:_______
可发生反应:_______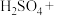 _______
_______ _______
_______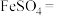 _______
_______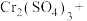 _______
_______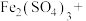 _______
_______ _______
_______ (未配平)。
(未配平)。①配平上述化学方程式:
②用单线桥法表示出电子转移的过程:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】过二硫酸钾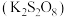 可用作消毒剂和织物漂白剂。回答下列问题:
可用作消毒剂和织物漂白剂。回答下列问题:
(1)加热条件下可用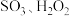 和
和 作原料制备过二硫酸钾,反应的化学方程式为
作原料制备过二硫酸钾,反应的化学方程式为___________ 。
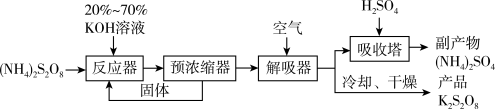
(2)以 (过二硫酸铵)为原料制备过二硫酸钾的主要流程如下:
(过二硫酸铵)为原料制备过二硫酸钾的主要流程如下:
已知 受热分解可得
受热分解可得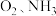 等。
等。
①预浓缩得到的固体返回反应器再次与反应物作用的目的是___________ 。
②解吸器中通入空气的目的是___________ 。
(3)电解法制取 的装置如图所示:
的装置如图所示:
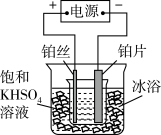
装置工作时,向阴极移动的离子是___________ ,阳极的电解反应式为___________ 。
(4)某同学通过下列实验探究 的性质。
的性质。
①取少量 放在试管中加热,产生的气体依次通过
放在试管中加热,产生的气体依次通过 溶液(有白色沉淀),再通入品红溶液(红色不褪)中,则分解产生的气态产物有
溶液(有白色沉淀),再通入品红溶液(红色不褪)中,则分解产生的气态产物有___________ 。
②向 溶液中加入
溶液中加入 溶液,再滴入1滴
溶液,再滴入1滴 (作催化剂),振荡,溶液变为紫色,该反应的离子方程式为
(作催化剂),振荡,溶液变为紫色,该反应的离子方程式为___________ 。
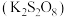 可用作消毒剂和织物漂白剂。回答下列问题:
可用作消毒剂和织物漂白剂。回答下列问题:(1)加热条件下可用
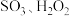 和
和 作原料制备过二硫酸钾,反应的化学方程式为
作原料制备过二硫酸钾,反应的化学方程式为(2)以
 (过二硫酸铵)为原料制备过二硫酸钾的主要流程如下:
(过二硫酸铵)为原料制备过二硫酸钾的主要流程如下:
已知
 受热分解可得
受热分解可得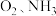 等。
等。①预浓缩得到的固体返回反应器再次与反应物作用的目的是
②解吸器中通入空气的目的是
(3)电解法制取
 的装置如图所示:
的装置如图所示:
装置工作时,向阴极移动的离子是
(4)某同学通过下列实验探究
 的性质。
的性质。①取少量
 放在试管中加热,产生的气体依次通过
放在试管中加热,产生的气体依次通过 溶液(有白色沉淀),再通入品红溶液(红色不褪)中,则分解产生的气态产物有
溶液(有白色沉淀),再通入品红溶液(红色不褪)中,则分解产生的气态产物有②向
 溶液中加入
溶液中加入 溶液,再滴入1滴
溶液,再滴入1滴 (作催化剂),振荡,溶液变为紫色,该反应的离子方程式为
(作催化剂),振荡,溶液变为紫色,该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】硫酸锌广泛应用于工农业生产中。工业上以粗氧化锌(含Zn、FeO、CuO等杂质)为原料生产 的一种流程的部分过程如下(各过程需控制适宜条件)。
的一种流程的部分过程如下(各过程需控制适宜条件)。
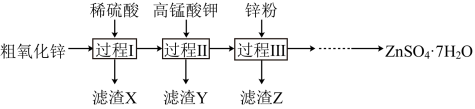
(1)过程I中,能与稀硫酸反应的物质有_______ 。
(2)过程I需要持续强制通风,原因是该过程中生成的氢气具有_______ 性。
(3)过程II中,滤渣Y含有 。加入高锰酸钾的主要目的是
。加入高锰酸钾的主要目的是_______ 。
(4)过程III中,滤渣Z含铜,生成铜的离子方程式为_______ 。
 的一种流程的部分过程如下(各过程需控制适宜条件)。
的一种流程的部分过程如下(各过程需控制适宜条件)。
(1)过程I中,能与稀硫酸反应的物质有
(2)过程I需要持续强制通风,原因是该过程中生成的氢气具有
(3)过程II中,滤渣Y含有
 。加入高锰酸钾的主要目的是
。加入高锰酸钾的主要目的是(4)过程III中,滤渣Z含铜,生成铜的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】化工产品中,含氯物质众多,其用途广泛。回答下列问题:
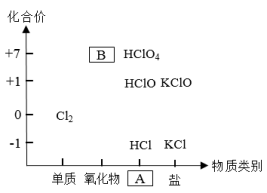
(1)如图为氯及其化合物的“价一类”二维图。缺失的类别A为___ 、物质B为___ (填化学式)。
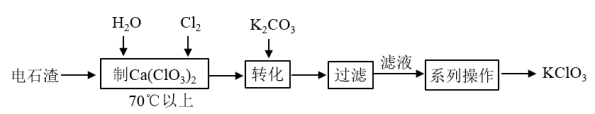
(2)电石渣[主要成分为CaOH2]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取KClO3的工艺流程如图所示:
已知CaClO32易溶于水。
①工业生产电石的反应为CaO+3C CaC2+CO,该反应中还原剂为
CaC2+CO,该反应中还原剂为_____ 。
②流程中“制CaClO32”的化学方程式为__ ;“转化”发生反应的离子方程式为___ 。
③上述流程中所用Cl2是用MnO2与浓盐酸反应制得。该反应的离子方程式是___ ,其中盐酸体现的性质为___ 性和____ 性。
(1)如图为氯及其化合物的“价一类”二维图。缺失的类别A为

(2)电石渣[主要成分为CaOH2]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取KClO3的工艺流程如图所示:

已知CaClO32易溶于水。
①工业生产电石的反应为CaO+3C
 CaC2+CO,该反应中还原剂为
CaC2+CO,该反应中还原剂为②流程中“制CaClO32”的化学方程式为
③上述流程中所用Cl2是用MnO2与浓盐酸反应制得。该反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】实验室可用NaClO3制取ClO2气体,再由ClO2制得NaClO2,实验装置如图所示:回答下列问题:
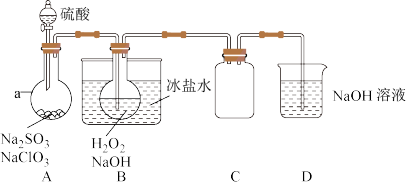
(1)仪器a的名称为___________ ;装置C的作用是___________ 。
(2)B中发生反应的化学方程式为___________ 。
(3)该实验必须使NaClO3稍微过量,目的是___________ 。
(4)证明NaClO2具有氧化性的方法是:取少量将B中溶液于试管中,先___________ ,再加入___________ (填序号,下同)酸化,最后加入___________ 检验。
①稀HNO3②稀H2SO4③K2SO3溶液④BaCl2溶液⑤FeCl2溶液⑥KSCN溶液

(1)仪器a的名称为
(2)B中发生反应的化学方程式为
(3)该实验必须使NaClO3稍微过量,目的是
(4)证明NaClO2具有氧化性的方法是:取少量将B中溶液于试管中,先
①稀HNO3②稀H2SO4③K2SO3溶液④BaCl2溶液⑤FeCl2溶液⑥KSCN溶液
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】2020年12月17日嫦娥五号返回器带回月球土壤样品。研究发现,月球土壤样品中存在铁、金、银、铅、锌、铜等矿物颗粒。中国科学家首次在月球上发现新矿物,并命名为“嫦娥石”,理想的化学式为(Ca8Y)Fe(PO4)7。请回答下列问题:
(1)基态Fe原子的价电子排布式为_______ 。
(2)从原子结构角度,Fe3+比Fe2+稳定原因是_______ 。
(3)“嫦娥石”中的阴离子 ,VSEPR模型的名称是
,VSEPR模型的名称是_______ 。
(4)我国科学家研究发现,十八胺在较高温度下具有一定的还原性,由于从十八胺中获得电子的能力不同,不同的金属盐在十八胺体系中反应可以得到不同的产物:
已知元素的电负性数据:
据此推测单一的金属(Au3+)盐在十八胺体系中反应的产物为_______ (写化学式)。
(1)基态Fe原子的价电子排布式为
(2)从原子结构角度,Fe3+比Fe2+稳定原因是
(3)“嫦娥石”中的阴离子
 ,VSEPR模型的名称是
,VSEPR模型的名称是(4)我国科学家研究发现,十八胺在较高温度下具有一定的还原性,由于从十八胺中获得电子的能力不同,不同的金属盐在十八胺体系中反应可以得到不同的产物:
| 单一金属盐 | Zn2+ | Ag+ |
| 在十八胺体系中的产物 | ZnO | Ag |
| 元素 | Zn | Ag | Au |
| 电负性(鲍林标度) | 1.6 | 1.9 | 2.4 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】 是一种常见的氧化剂和消毒剂,以软锰矿(主要成分为
是一种常见的氧化剂和消毒剂,以软锰矿(主要成分为 )为原料制备
)为原料制备 的方法如图所示:
的方法如图所示:
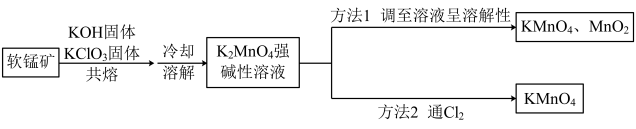
回答下列问题:
(1)共熔时能否用瓷坩埚做反应器___________ (填“能”或“否”)。
(2)方法1调至溶液呈弱碱性时反应的离子方程式为___________ 。
(3)方法2通 制备
制备 的装置如下图所示(夹持装置略):
的装置如下图所示(夹持装置略):
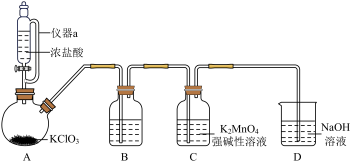
①仪器a的名称为___________ 。
②装置B中盛放的试剂为___________ (填试剂名称)。
③强碱性条件下,氧化性:
___________  (填“
(填“ ”或“
”或“ ”)。
”)。
④D中反应的离子方程式为___________ 。
 是一种常见的氧化剂和消毒剂,以软锰矿(主要成分为
是一种常见的氧化剂和消毒剂,以软锰矿(主要成分为 )为原料制备
)为原料制备 的方法如图所示:
的方法如图所示:
回答下列问题:
(1)共熔时能否用瓷坩埚做反应器
(2)方法1调至溶液呈弱碱性时反应的离子方程式为
(3)方法2通
 制备
制备 的装置如下图所示(夹持装置略):
的装置如下图所示(夹持装置略):
①仪器a的名称为
②装置B中盛放的试剂为
③强碱性条件下,氧化性:

 (填“
(填“ ”或“
”或“ ”)。
”)。④D中反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】高铁酸钾( )是一种高效多功能的新型非氯绿色消毒剂。其溶于水与水结合放出氧气并有絮状沉淀产生,常用作净水剂。其生产工艺如下:
)是一种高效多功能的新型非氯绿色消毒剂。其溶于水与水结合放出氧气并有絮状沉淀产生,常用作净水剂。其生产工艺如下:
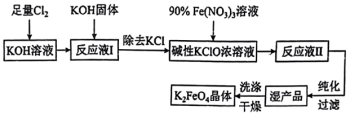
(1)高铁酸钾( )中铁元素的化合价为
)中铁元素的化合价为_______ 。
(2)写出 与KOH溶液反应的化学方程式
与KOH溶液反应的化学方程式_______ 。
(3)写出 溶液与碱性KClO溶液反应的离子方程式
溶液与碱性KClO溶液反应的离子方程式_______ 。
(4) 可作为新型多功能水处理剂的原因是
可作为新型多功能水处理剂的原因是_______ 。
(5)从“反应液Ⅱ”中分离出 后,副产品有
后,副产品有_______ (写化学式)。
(6)该工艺每得到1.98kg ,理论上消耗
,理论上消耗 的物质的量为
的物质的量为_______ mol。
 )是一种高效多功能的新型非氯绿色消毒剂。其溶于水与水结合放出氧气并有絮状沉淀产生,常用作净水剂。其生产工艺如下:
)是一种高效多功能的新型非氯绿色消毒剂。其溶于水与水结合放出氧气并有絮状沉淀产生,常用作净水剂。其生产工艺如下:
(1)高铁酸钾(
 )中铁元素的化合价为
)中铁元素的化合价为(2)写出
 与KOH溶液反应的化学方程式
与KOH溶液反应的化学方程式(3)写出
 溶液与碱性KClO溶液反应的离子方程式
溶液与碱性KClO溶液反应的离子方程式(4)
 可作为新型多功能水处理剂的原因是
可作为新型多功能水处理剂的原因是(5)从“反应液Ⅱ”中分离出
 后,副产品有
后,副产品有(6)该工艺每得到1.98kg
 ,理论上消耗
,理论上消耗 的物质的量为
的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】瑞典化学家舍勒是最早发现氯气的人,他在研究软锰矿矿石(主要成分是二氧化锰)时,把浓盐酸和软锰矿矿石混合加热,意外地得到了氯气。至今,实验室中还用这种方法制取氯气,装置如图所示,化学反应方程式为: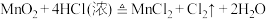
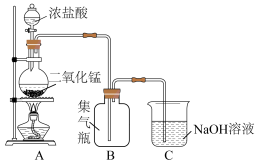
回答下列问题:
(1)实验室制取 的反应中,浓盐酸表现
的反应中,浓盐酸表现_________ (填“氧化性”、“还原性”或“酸性”)。
(2)请用单线桥表示该反应中电子转移的方向和数目_________ 。
(3)标况下,若生成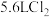 ,则转移电子的数目为
,则转移电子的数目为_________ 。
(4)装置C可吸收多余的 ,生成
,生成 和
和 ,写出离子方程式
,写出离子方程式_________ 。所用 溶液一般为
溶液一般为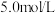 ,用
,用 固体配制
固体配制 该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、
该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、_________ 。
(5) 有强氧化性,某实验小组为探究
有强氧化性,某实验小组为探究 、
、 、
、 在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下
在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下 、
、 、
、 的氧化性由弱到强的顺序是
的氧化性由弱到强的顺序是_________ 。
(6)装置C中也可能生成 ,
, 和浓盐酸也可以制备
和浓盐酸也可以制备 ,试写出离子方程式
,试写出离子方程式_________ 。
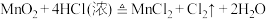

回答下列问题:
(1)实验室制取
 的反应中,浓盐酸表现
的反应中,浓盐酸表现(2)请用单线桥表示该反应中电子转移的方向和数目
(3)标况下,若生成
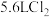 ,则转移电子的数目为
,则转移电子的数目为(4)装置C可吸收多余的
 ,生成
,生成 和
和 ,写出离子方程式
,写出离子方程式 溶液一般为
溶液一般为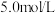 ,用
,用 固体配制
固体配制 该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、
该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、(5)
 有强氧化性,某实验小组为探究
有强氧化性,某实验小组为探究 、
、 、
、 在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下
在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下 、
、 、
、 的氧化性由弱到强的顺序是
的氧化性由弱到强的顺序是(6)装置C中也可能生成
 ,
, 和浓盐酸也可以制备
和浓盐酸也可以制备 ,试写出离子方程式
,试写出离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】氯酸钾 和次氯酸钠(NaClO)是氯元素重要的含氧酸盐,实验室中利用下图装置制备这两种盐。回答下列问题:
和次氯酸钠(NaClO)是氯元素重要的含氧酸盐,实验室中利用下图装置制备这两种盐。回答下列问题:
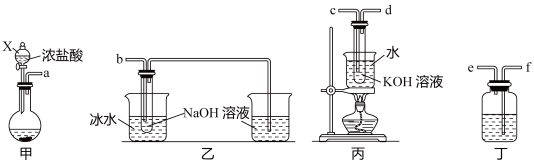
(1)仪器X名称是_______ ,甲装置圆底烧瓶中的试剂为 固体,写出发生反应的化学方程式
固体,写出发生反应的化学方程式_______ 。
(2)为达成实验目的,上述仪器口连接顺序依次为:a−____ 。
(3)丁装置中所盛试剂为___ ;乙装置中采用冰水浴冷却的目的是___ 。
(4)反应结束取出b中试管,经冷却结晶,___ ,____ ,干燥,到得到 晶体。
晶体。
(5)为进一步测定所得 晶体的纯度,设计了如下实验方案:
晶体的纯度,设计了如下实验方案:
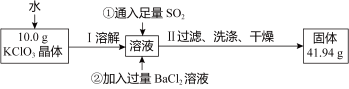
写出通入足量 时,溶液中发生反应的离子方程式
时,溶液中发生反应的离子方程式_______ 。依据上述实验结果,测得该晶体的纯度为_______ 。
 和次氯酸钠(NaClO)是氯元素重要的含氧酸盐,实验室中利用下图装置制备这两种盐。回答下列问题:
和次氯酸钠(NaClO)是氯元素重要的含氧酸盐,实验室中利用下图装置制备这两种盐。回答下列问题:
(1)仪器X名称是
 固体,写出发生反应的化学方程式
固体,写出发生反应的化学方程式(2)为达成实验目的,上述仪器口连接顺序依次为:a−
(3)丁装置中所盛试剂为
(4)反应结束取出b中试管,经冷却结晶,
 晶体。
晶体。(5)为进一步测定所得
 晶体的纯度,设计了如下实验方案:
晶体的纯度,设计了如下实验方案:
写出通入足量
 时,溶液中发生反应的离子方程式
时,溶液中发生反应的离子方程式
您最近一年使用:0次



