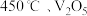 催化
催化 和
和 反应时、能量变化如图所示,反应机理如下:
反应时、能量变化如图所示,反应机理如下:反应①:
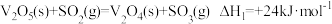
反应②:
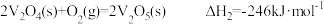

下列说法正确的是
A.反应①的 |
| B.反应②是慢反应,决定该反应速率 |
C.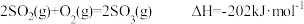 |
D.使用 可以降低反应的焓变 可以降低反应的焓变 |
更新时间:2022-01-21 20:58:21
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】硫是一种重要的非金属元素,正交硫(Orthogonal sulfur)是硫稳定存在的唯一形式,单斜硫是硫的同素异形体之一。下列说法不正确 的是
已知:①S(正交,s)+O2(g)=SO2(g)ΔH1=-296.83kJ•mol-1
②S(单斜,s)+O2(g)=SO2(g)ΔH2=-297.16kJ•mol-1
③S(单斜,s)=S(正交,s)ΔH3
已知:①S(正交,s)+O2(g)=SO2(g)ΔH1=-296.83kJ•mol-1
②S(单斜,s)+O2(g)=SO2(g)ΔH2=-297.16kJ•mol-1
③S(单斜,s)=S(正交,s)ΔH3
| A.硫黄是一种黄色晶体,不溶于水 |
| B.正交硫比单斜硫稳定 |
| C.ΔH3=-0.66kJ•mol -1, |
| D.1mol S(单斜,s)和1mol O2(g)的总能量高于1mol SO2(g)的能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知:① As(s)+ H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
② H2(g)+ O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
③ 2As(s)+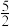 O2(g)=As2O5(s) ΔH3
O2(g)=As2O5(s) ΔH3
则反应As2O5(s)+3H2O(l)=2H3AsO4(s)的ΔH为( )
 H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1② H2(g)+
 O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2③ 2As(s)+
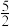 O2(g)=As2O5(s) ΔH3
O2(g)=As2O5(s) ΔH3则反应As2O5(s)+3H2O(l)=2H3AsO4(s)的ΔH为( )
| A.2ΔH1-ΔH3-3ΔH2 | B.ΔH3+3ΔH2-2ΔH1 |
| C.ΔH3+3ΔH2-2ΔH1 | D.2ΔH1-3ΔH2-ΔH3 |
您最近一年使用:0次
【推荐3】通过以下反应均可获取H2。下列说法错误的是
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+O2(g) ΔH1=571.6kJ∙mol–1
②焦炭与水反应制氢:C(s)+H2O(g)=CO(g)+H2(g) ΔH2=131.3kJ∙mol–1
③甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH3=206.1kJ∙mol–1
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+O2(g) ΔH1=571.6kJ∙mol–1
②焦炭与水反应制氢:C(s)+H2O(g)=CO(g)+H2(g) ΔH2=131.3kJ∙mol–1
③甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH3=206.1kJ∙mol–1
| A.反应①中光能转化为化学能 |
| B.反应③使用催化剂,ΔH3不变 |
| C.反应②为吸热反应 |
| D.反应CH4(g)=C(s)+2H2(g)的ΔH=-74.8kJ∙mol–1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知25℃、 下,
下, 水蒸发为水蒸气需要吸热
水蒸发为水蒸气需要吸热
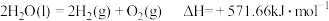
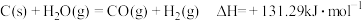
则反应2C(s)+O2(g)=2CO(g)的反应热为
 下,
下, 水蒸发为水蒸气需要吸热
水蒸发为水蒸气需要吸热
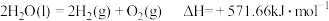
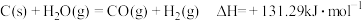
则反应2C(s)+O2(g)=2CO(g)的反应热为
| A.ΔH=-396.36kJ·mol-1 | B.ΔH=-110.53kJ·mol-1 |
| C.ΔH=-154.54kJ·mol-1 | D.ΔH=-221.06kJ·mol-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在常温常压下,已知:
①4Fe(s)+3O2(g)= 2Fe2O3(s) ΔH1
②4Al(s)+3O2(g)= 2Al2O3(s) ΔH2
③2Al(s)+Fe2O3(s)= Al2O3(s)+2Fe(s) ΔH3
则ΔH3与ΔH1、ΔH2之间的关系正确的是
①4Fe(s)+3O2(g)= 2Fe2O3(s) ΔH1
②4Al(s)+3O2(g)= 2Al2O3(s) ΔH2
③2Al(s)+Fe2O3(s)= Al2O3(s)+2Fe(s) ΔH3
则ΔH3与ΔH1、ΔH2之间的关系正确的是
A.ΔH3= (ΔH1+ΔH2) (ΔH1+ΔH2) | B.ΔH3=(ΔH2-ΔH1) |
| C.ΔH3=2(ΔH1+ΔH2) | D.ΔH3= (ΔH2-ΔH1) (ΔH2-ΔH1) |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】我国科研人员提出了由 和
和 转化为高附加值产品
转化为高附加值产品 的催化反应历程,该历程示意图如下所示。
的催化反应历程,该历程示意图如下所示。
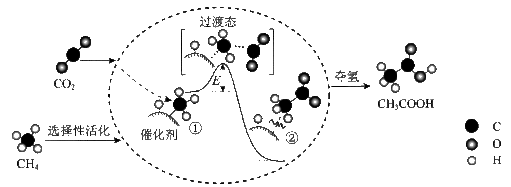
下列说法不正确的是
 和
和 转化为高附加值产品
转化为高附加值产品 的催化反应历程,该历程示意图如下所示。
的催化反应历程,该历程示意图如下所示。
下列说法不正确的是
A.生成 总反应的原子利用率为 总反应的原子利用率为 |
| B.降低温度,降低反应物分子中活化分子的百分数,减少有效碰撞的次数 |
| C.增大反应体系的压强,可以增加反应物分子中活化分子的百分数 |
| D.该反应的催化剂能改变反应历程,降低反应的活化能,增加活化分子的数目 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】反应2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是
CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是
 CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是
CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是| A.上述反应在任何温度下均可自发进行 |
| B.上述反应反应物的总能量大于生成物的总能量 |
C.上述反应平衡常数K=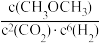 |
| D.上述反应达到平衡后,加入催化剂,平衡正向移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】与下列图示相关的说法正确的是


A.图甲表示某温度下,在 密闭容器内发生反应 密闭容器内发生反应 时, 时,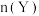 和 和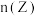 随时间变化的情况。该图说明前 随时间变化的情况。该图说明前 内,反应速率 内,反应速率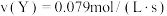 |
B.图乙表示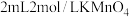 酸性溶液与 酸性溶液与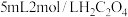 溶液混合时, 溶液混合时, 随时间变化的情况。该图说明生成的 随时间变化的情况。该图说明生成的 一定对该反应有催化作用 一定对该反应有催化作用 |
C.图丙表示一定温度下,溴化银的沉淀溶解平衡曲线。此时, 点代表的溶液是饱和溶液 点代表的溶液是饱和溶液 |
D.图丁表示室温时分别向盛有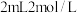 盐酸和醋酸的相同锥形瓶中各加入 盐酸和醋酸的相同锥形瓶中各加入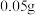 相同的镁条,立即塞紧塞子时,瓶中压强随时间的变化情况。该图说明曲线 相同的镁条,立即塞紧塞子时,瓶中压强随时间的变化情况。该图说明曲线 对应的是醋酸 对应的是醋酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法错误的是
| A.内能是系统内物质各种能量的总和,与温度、压强、聚集状态等有关 |
| B.熵是描述系统混乱度的物理量,熵增反应一定是自发反应 |
| C.碰撞理论认为,升高温度能增大活化分子百分数,增加有效碰撞几率,加快反应速率 |
| D.过滤态理论认为,催化剂能降低反应所需的活化能,同等程度地提高正、逆反应速率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法中,正确的是
| A.需要加热才能发生的反应一定是吸热反应 |
| B.放热反应在常温下一定能很容易发生 |
| C.吸热反应在一定条件下也能自发进行 |
| D.氧化还原反应一定是放热反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】通过2NO(g)+2CO(g)⇌2CO2(g)+N2(g) ΔH=-746.5kJ·mol-1催化还原的方法,可将汽车尾气中有害气体转化为无害气体。下列说法正确的是
| A.该反应在任何条件下都能自发进行 |
B.反应的平衡常数可表示为K=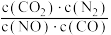 |
C.其它条件不变,增大 的值,NO的转化率下降 的值,NO的转化率下降 |
| D.使用高效的催化剂可以降低反应的焓变 |
您最近一年使用:0次



