电解质溶液有许多奇妙之处,只有深入思考,才能体会到它的乐趣。下列关于电解质溶液的叙述中正确的是
| A.Na2CO3、NaHCO3两种盐溶液中,离子种类相同 |
| B.常温下,1 mol·L-1的CH3COOH溶液与 1 mol·L-1的NaOH溶液等体积混合后,所得混合液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
C.物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,c( )前者大于后者 )前者大于后者 |
| D.常温下,某溶液中由水电离出的c(H+)=10-5 mol·L-1,则此溶液可能是盐酸 |
更新时间:2022/02/20 14:58:34
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】常温下,下列各组离子一定能在指定溶液中大量共存的是
A.在中性溶液中:Na+、Ba2+、SO 、Cl- 、Cl- |
B.与Al反应能放出H2的溶液中:Fe2+、K+、NO 、SO 、SO |
C.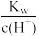 =1×10-13mol·L-1的溶液中:NH =1×10-13mol·L-1的溶液中:NH 、Na+、Cl-、NO 、Na+、Cl-、NO |
D.水电离的c(H+)=1×10-13mol·L-1的溶液中:K+、Na+、AlO 、CO 、CO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于电解质溶液说法错误的是
| A.室温下,pH相同的NaOH溶液和CH3COONa溶液,水的电离程度后者大 |
B.pH相同的a.CH3COONa溶液 b.NaHCO3溶液 c. 溶液,溶液中c(Na+)的大小顺序是a>b>c 溶液,溶液中c(Na+)的大小顺序是a>b>c |
C.pH=2的H2C2O4和pH=12的NaOH溶液以任意比例混合:c(Na+)+c(H+)=c(OH-)+c( )+2c( )+2c( ) ) |
D.向  CH3COOH溶液中加入少量水,溶液中的所有离子的浓度都减小 CH3COOH溶液中加入少量水,溶液中的所有离子的浓度都减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,下列说法正确的是( )
| A.pH相等的盐酸和醋酸,加水稀释相同倍数后,c(C1-)=c(CH3COO-) |
| B.0.1 mol/L氨水的pH=a,加入适量的氯化铵固体可使溶液pH=a+1 |
C.物质的量浓度相等的(NH4)2SO4溶液与(NH4)2CO3溶液中, 前者大于后者 前者大于后者 |
| D.等物质的量浓度等体积的醋酸溶液和盐酸溶液,与足量氢氧化钠反应,放出的热量相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关平衡常数(K、Ka、Kw)的说法中不正确 的是
| A.平衡常数的大小能说明反应(或电离、溶解)进行的程度 |
| B.若各平衡常数(K、Ka、Kw)的值发生变化,则平衡一定发生移动 |
| C.若温度升高,则各平衡常数一定增大 |
| D.某一可逆反应的平衡常数越大,表明反应(或电离、溶解)进行的程度越大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下在20 mL 0.1 mol/L Na2CO3溶液中逐渐滴加入0.1 mol/L HCl溶液40 mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示,下列说法不正确的是
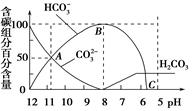

| A.0.1 mol/L Na2CO3溶液中c(OH-)-c(H+)=2c(H2CO3)+c(HCO3-) |
| B.在A点c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| C.常温下CO2饱和溶液的pH约为5.6 |
| D.0.05 mol/L NaHCO3溶液的pH=8 |
您最近一年使用:0次



