下列操作、现象和结论都正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 将 的氨水稀释成 的氨水稀释成 ,测量稀释前后溶液pH,发现稀释后pH减小 ,测量稀释前后溶液pH,发现稀释后pH减小 | 稀释后 电离程度减小 电离程度减小 |
| B | 向含有酚酞的 溶液中加入少量 溶液中加入少量 固体,观察到溶液红色变浅 固体,观察到溶液红色变浅 | 证明 溶液中存在水解平衡 溶液中存在水解平衡 |
| C | 25℃时用pH试纸测得: 溶液的pH约为8, 溶液的pH约为8, 溶液的pH约为9 溶液的pH约为9 |  电离出 电离出 的能力比 的能力比 的弱 的弱 |
| D | 在一支50mL酸式滴定管中装入盐酸,液面恰好在10mL刻度处,把管内液体全部放出盛入量筒内 | 量筒内所得液体体积是40.0mL |
| A.A | B.B | C.C | D.D |
更新时间:2022-03-30 21:01:20
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】关注“实验室化学”并加以实践能有效提高同学们的实验素养。用如图所示装置(部分夹持装置省略)进行实验,不能达到实验目的的是
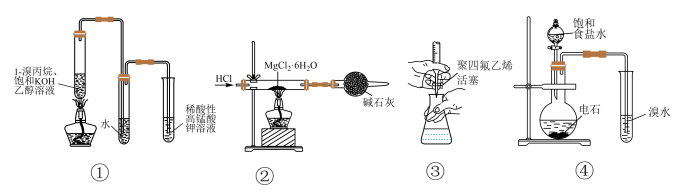
| A.利用装置①验证1-溴丙烷发生了消去反应 |
B.利用装置②制备无水 |
| C.图③操作可用于氢氧化钠标准溶液滴定未知浓度的盐酸 |
| D.图④装置可用于实验室制取乙炔并进行相关的性质检验 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在标有“ ”的滴定管内,液面的读数为46.00,如果将管内液体全部放入量筒内,那么量筒内溶液的体积
”的滴定管内,液面的读数为46.00,如果将管内液体全部放入量筒内,那么量筒内溶液的体积
 ”的滴定管内,液面的读数为46.00,如果将管内液体全部放入量筒内,那么量筒内溶液的体积
”的滴定管内,液面的读数为46.00,如果将管内液体全部放入量筒内,那么量筒内溶液的体积A.等于 | B.大于 | C.小于 | D.无法判断 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关说法正确的是
| A.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H>0 |
B.0.1mol·L-1氨水加水稀释后,溶液中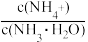 的值减小 的值减小 |
| C.用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更小 |
| D.精炼铜时,两电极经过电量相等,其质量改变量也相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法不正确的是
| A.1L浓度为0.1mol/L的NH4Cl溶液阳离子数目多于氯离子数目 |
| B.比较浓度均为0.1mol·L-1的HI和醋酸溶液的导电能力可判断HI为强酸 |
| C.常温下,pH=3的醋酸溶液水加稀释1000倍后溶液的pH<6 |
| D.常温下,同体积的pH=9的NaClO溶液和pH=5的NH4Cl溶液水电离的OH-数相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某同学在两个相同的特制容器中分别加入 溶液和
溶液和 溶液,再分别用
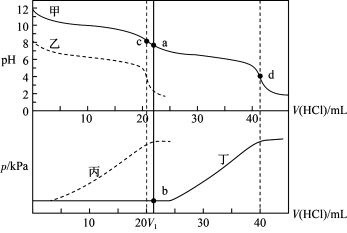
溶液,再分别用 盐酸滴定,利用pH计和压力传感器检测,得到如图曲线。下列说法正确的是
盐酸滴定,利用pH计和压力传感器检测,得到如图曲线。下列说法正确的是
 溶液和
溶液和 溶液,再分别用
溶液,再分别用 盐酸滴定,利用pH计和压力传感器检测,得到如图曲线。下列说法正确的是
盐酸滴定,利用pH计和压力传感器检测,得到如图曲线。下列说法正确的是
A.图中甲、丁线表示向 溶液中滴加盐酸,乙、丙线表示向 溶液中滴加盐酸,乙、丙线表示向 溶液中滴加盐酸 溶液中滴加盐酸 |
B.当滴加盐酸的体积为 时(a点、b点),所发生的反应用离子方程式表示为: 时(a点、b点),所发生的反应用离子方程式表示为: |
C.根据 图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点 图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点 |
D. 和 和 溶液中均满足: 溶液中均满足: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据下列实验操作和现象得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向浓度均为0.1mol∙L-1的NaCl和NaI混合溶液中滴加少量AgNO3溶液,先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 将丁烷裂解气通入到溴的四氯化碳溶液中,溶液褪色 | 裂解气中一定含有乙烯 |
| C | 镀锌铁钉和普通铁钉同时投入相同浓度的盐酸中,镀锌铁钉产生气泡更快 | 镀锌后的铁更易发生析氢腐蚀 |
| D | 用pH计测定相同温度下,相同物质的量浓度的NaHCO3溶液和NaCN溶液,发现NaHCO3溶液的pH小于NaCN溶液的pH | Ka1(H2CO3)<Ka(HCN) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 分别为
分别为 、
、 、
、 ,则
,则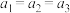
 ,
, ,
, ,则
,则
 、
、 、
、 ,则
,则
 的速率分别为
的速率分别为 、
、 、
、 ,则
,则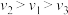
 溶液的性质。下列实验方案能达到探究目的的是
溶液的性质。下列实验方案能达到探究目的的是 是否发生电离
是否发生电离 溶液中加入一小块钠,观察溶液中是否有气泡产生
溶液中加入一小块钠,观察溶液中是否有气泡产生 试纸上,测出溶液的
试纸上,测出溶液的



