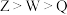下列描述中正确的是
A.基态碳原子的轨道表示式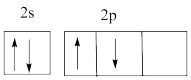 |
| B.第四周期中未成对电子数最多的原子为Mn |
| C.基态核外电子的排布为1s22s22p63s23p4的原子,3p能级有一个空轨道 |
| D.磷元素的第一电离能大于硫元素的第一电离能 |
更新时间:2022-04-19 16:17:31
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】几种短周期元素的原子半径及主要化合价如图所示,下列叙述不正确的是

| A.第一电离能:X>Y |
| B.Z的电负性小于W |
| C.Y元素原子核外共有5种不同运动状态的电子 |
| D.X的单质可分别与Z、W的单质发生氧化还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列基态原子的电子排布式或电子排布图,正确的是
A.12Mg原子: | B.8O原子: |
| C.24Cr原子:[Ar]3d44s2 | D.26Fe2+离子:[Ar]3d6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列叙述正确的是
| A.所有的σ键的强度都比π键的大 |
| B.常规晶胞的顶角原子是8个晶胞共用的 |
| C.第一电离能的大小可以作为判断元素金属性强弱的依据 |
| D.基态原子的核外电子填充在6个轨道中的元素有3种 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】NH3和N2H4是重要的化工原料,可用于某些配合物的制备,如NiSO4溶于氨水形成[Ni(NH3)6]SO4,下列有关的说法正确的是
| A.[Ni(NH3)6]SO4的配体为NH3,中心体的外围电子排布式为3d84s2 |
| B.1mol[Ni(NH3)6]2+中σ键的数目为18mol |
| C.[Ni(NH3)6]2+中H-N-H的键角大于NH3中的键角 |
| D.由于[Ni(NH3)6]SO4是配合物,故向其中滴加BaCl2溶液不会生成沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】反应 是目前大规模制取氢气的方法之一。下列有关说法正确的是
是目前大规模制取氢气的方法之一。下列有关说法正确的是
 是目前大规模制取氢气的方法之一。下列有关说法正确的是
是目前大规模制取氢气的方法之一。下列有关说法正确的是A.中子数为8的碳原子: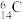 | B.基态氧原子轨道表示式: |
C. 的电子式为 的电子式为 | D. 的空间构型为四面体形 的空间构型为四面体形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】前四周期元素X、Y、Z、M、W的原子序数依次增大,基态X原子的电子层数、能级数目和轨道数目均相等,Z可与X形成X2Z2、X2Z两种无色化合物,基态时M原子2p原子轨道上有5个电子,Y、W均满足最高能级的轨道处于半满状态,但Y的内层轨道全充满,W的成单电子数在前四周期元素中是最多的。下列说法正确的是
| A.原子半径:r(X)<r(Y)<r(Z)<r(M)<r(W) |
| B.Y、Z、M的氢化物沸点是同周期非金属元素形成的氢化物中沸点最高的 |
| C.Y的第一电离能比同周期相邻元素的大 |
| D.基态W原子的价电子轨道表达式为3d54s1 |
您最近一年使用:0次
【推荐1】氨基酸是构成人体必备蛋白质的基础,某氨基酸的结构简式如图所示。下列有关说法正确的是
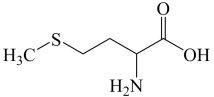
| A.第一电离能:O>N>C>H |
| B.基态氧原子的电子有8种运动状态 |
C.该分子中碳原子的杂化类型有sp、 和 和 |
| D.该分子间不能形成氢键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某离子与其检验试剂GBHA的反应如下图所示,其中M、W、X、Y、Z为电负性依次增大的分属不同三个周期的前20号元素,下列说法正确的是
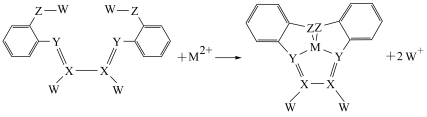

| A.同周期第一电离能介于X和Z之间的元素有1种 |
B.键角: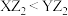 |
| C.氢化物的沸点:X<Z |
D.可通过电解熔融 获得M的单质 获得M的单质 |
您最近一年使用:0次

 [B(OH)4]-+H+
[B(OH)4]-+H+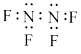



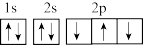
 、Q简单氢化物的水溶液pH分别为11、1,以下有关说法正确的是
、Q简单氢化物的水溶液pH分别为11、1,以下有关说法正确的是