据《科学》报道,中国科学家首次实现超导体(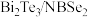 )中分段费米面。回答下列问题:
)中分段费米面。回答下列问题:
(1)Bi与P位于同主族,基态P原子的价层电子排布式为_______ 。基态Se原子核外电子云轮廓图呈哑铃形的能级上共有_______ 个电子
(2)二氯二茂铌的组成为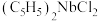 环戊二烯阴离子(
环戊二烯阴离子(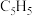 )的平面结构简式如图所示:
)的平面结构简式如图所示:
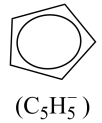
① 中C原子的杂化类型是
中C原子的杂化类型是_______ 。
②已知分子中的大π键可以用 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则 中大π键可以表示为
中大π键可以表示为_______ 。
(3) 的空间构型为
的空间构型为_______ 。
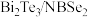 )中分段费米面。回答下列问题:
)中分段费米面。回答下列问题:(1)Bi与P位于同主族,基态P原子的价层电子排布式为
(2)二氯二茂铌的组成为
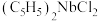 环戊二烯阴离子(
环戊二烯阴离子(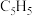 )的平面结构简式如图所示:
)的平面结构简式如图所示:
①
 中C原子的杂化类型是
中C原子的杂化类型是②已知分子中的大π键可以用
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则 中大π键可以表示为
中大π键可以表示为(3)
 的空间构型为
的空间构型为
更新时间:2022-04-22 16:00:17
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】我国科学家研发的新型光学材料(Sn7Br10S2)可替代传统光学材料硫镓银(AgGaS2)和磷锗锌(ZnGeP2)。请回答下列问题:
(1)基态硫原子核外电子云轮廓图呈哑铃形的能级上占据的电子总数为___________ 。
(2)SF6可用作高压发电系统的绝缘气体,其分子呈正八面体结构,如图所示。
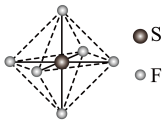
①SF6是___________ (填“极性”或“非极性”)分子。
②1molSF6分子中含___________ molσ键。
(3)HF、HCl、HBr的酸性由强到弱的顺序为___________ (填化学式,下同);沸点由高到低的顺序为___________ ;还原性由强到弱的顺序为___________ 。
(4)Ga(CH3)3和NH3在一定条件下可合成半导体材料GaN和CH4。Ga(CH3)3分子中Ga原子和C原子构成的空间构型是___________ ,碳原子的杂化类型是___________ 。
(5)四卤化锡的熔点如下表所示:
它们熔点递变的主要原因是___________ 。
(1)基态硫原子核外电子云轮廓图呈哑铃形的能级上占据的电子总数为
(2)SF6可用作高压发电系统的绝缘气体,其分子呈正八面体结构,如图所示。

①SF6是
②1molSF6分子中含
(3)HF、HCl、HBr的酸性由强到弱的顺序为
(4)Ga(CH3)3和NH3在一定条件下可合成半导体材料GaN和CH4。Ga(CH3)3分子中Ga原子和C原子构成的空间构型是
(5)四卤化锡的熔点如下表所示:
| 物质 | SnCl4 | SnBr4 | SnI4 |
| 熔点/℃ | ﹣33 | 31 | 144.5 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】现有五种元素A、B、C、D、E,其中A、B、C为三个不同周期的短周期元素,E为第四周期元素.请根据下列相关信息,回答下列问题:
(1)C基态原子中能量最高的电子,其电子云在空间有____ 个方向,原子轨道呈__________ 形,C简单离子核外有______ 种运动状态不同的电子.
(2) 难溶于
难溶于 ,简要说明理由:
,简要说明理由:________________ .
(3) 分子的空间构型为
分子的空间构型为__________ ,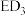 分子的
分子的 模型名称为
模型名称为__________ .
(4)下列气态分子 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为_______________ .
| 元素 | 相关信息 |
| A | 核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 原子核外p电子数与s电子数相等 |
| C | 基态原子的价电子排布为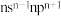 |
| D | 能层数与C相同,且电负性比C大 |
| E | 元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
(2)
 难溶于
难溶于 ,简要说明理由:
,简要说明理由:(3)
 分子的空间构型为
分子的空间构型为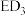 分子的
分子的 模型名称为
模型名称为(4)下列气态分子
 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为
您最近一年使用:0次
【推荐3】磷酸亚铁锂( )和锰酸锂(
)和锰酸锂( )均可用作锂离子电池正极材料。回答下列问题:
)均可用作锂离子电池正极材料。回答下列问题:
(1)基态Li原子核外电子所占据最高能级的电子云轮廓图为________ 形。
(2)Fe元素位于周期表_____ 周期_____ 族;原子核外电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为
表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为___________ 。
(3)基态Mn2+的价电子排布式为___________ ,锰的第三电离能高于铁的第三电离能,其原因是___________ 。
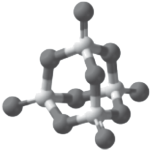
(4)P4S10的分子结构如图所示,其中含有________ 个六元环;______ g P4S10含有8molσ键。
 )和锰酸锂(
)和锰酸锂( )均可用作锂离子电池正极材料。回答下列问题:
)均可用作锂离子电池正极材料。回答下列问题:(1)基态Li原子核外电子所占据最高能级的电子云轮廓图为
(2)Fe元素位于周期表
 和
和 表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为
表示,称为电子的白旋磁量子数,基态Fe原子的价电子自旋磁量子数的代数和为(3)基态Mn2+的价电子排布式为
(4)P4S10的分子结构如图所示,其中含有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】元素H、N、O、S、Ni、Fe之间可形成多种化合物。请回答下列问题:
(1)基态Fe2+原子的价电子排布式为____________ ;Fe原子最外层电子的电子云形状为__________ 。
(2)N、O、S三种元素的第一电离能由大到小的顺序为___________ ;下列状态的O中,最容易失去最外层电子的是___________ (填字母)。
A.1s22s22p3 B.1s22s22p4 C.1s22s22p33s1 D.1s22s22p23s1
(3)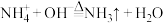 ,
, 转化为NH3的过程中,没有发生变化的有
转化为NH3的过程中,没有发生变化的有________ (填字母)。
A.键角 B.粒子的空间构型 C.杂化轨道类型
(4)已知单质铁有如图所示的三种堆积方式的晶胞结构:

①若晶胞a中Fe原子直径为d pm,设该晶胞边长x,则x=_________ cm。(用含d的代数式表示)。
②晶胞b中与一个Fe原子最邻近的Fe原子共有_________ 个。
③若晶胞c的密度为ρ g/cm3,则铁的原子半径r=_________ cm。(NA表示阿伏加德罗常数的值,用含ρ、NA的式子表示)。
(1)基态Fe2+原子的价电子排布式为
(2)N、O、S三种元素的第一电离能由大到小的顺序为
A.1s22s22p3 B.1s22s22p4 C.1s22s22p33s1 D.1s22s22p23s1
(3)
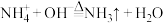 ,
, 转化为NH3的过程中,没有发生变化的有
转化为NH3的过程中,没有发生变化的有A.键角 B.粒子的空间构型 C.杂化轨道类型
(4)已知单质铁有如图所示的三种堆积方式的晶胞结构:

①若晶胞a中Fe原子直径为d pm,设该晶胞边长x,则x=
②晶胞b中与一个Fe原子最邻近的Fe原子共有
③若晶胞c的密度为ρ g/cm3,则铁的原子半径r=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】碱金属(Li、Na、K、Rb、Cs)及其化合物在生产、生活中有着重要的应用。
请回答:
(1)基态K原子核外有___________ 种不同的电子运动状态。
(2)卤化物CsICl2受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。解释X的熔点比Y高的原因:___________
(3)已知RbH2PO2是次磷酸的正盐,H3PO2的结构式为___________ ,其中P原子采取___________ 杂化方式。
(4)Al、B、H电负性分别为1.5、2.0、2.1,简要说明LiAlH4还原性比NaBH4强的原因:___________
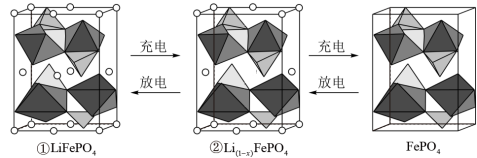
(5)锂离子电池电极材料是LiFePO4,其晶胞结构示意图如①所示。其中O围绕Fe和P分别形成4个正八面体和4个正四面体。电池充电时,LiFePO4脱出部分Li+形成Li(1-x)FePO4,其结构示意图如②所示,则Li(1-x)FePO4晶胞中n(Fe2+):n(Fe3+)=_________ 。
请回答:
(1)基态K原子核外有
(2)卤化物CsICl2受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。解释X的熔点比Y高的原因:
(3)已知RbH2PO2是次磷酸的正盐,H3PO2的结构式为
(4)Al、B、H电负性分别为1.5、2.0、2.1,简要说明LiAlH4还原性比NaBH4强的原因:
(5)锂离子电池电极材料是LiFePO4,其晶胞结构示意图如①所示。其中O围绕Fe和P分别形成4个正八面体和4个正四面体。电池充电时,LiFePO4脱出部分Li+形成Li(1-x)FePO4,其结构示意图如②所示,则Li(1-x)FePO4晶胞中n(Fe2+):n(Fe3+)=

您最近一年使用:0次
【推荐3】硫铁矿(主要成分FeS2)是接触法制硫酸的主要原料,请回答:
(1)基态下Fe2+共有_____ 种不同空间运动状态的电子。
(2)Fe2+形成的配合物亚铁氰化钾K4[Fe(CN)6]又称黄血盐,可用于检验Fe3+,与CN-互为等电子体的阴离子为_________ (任写一种);含有120molσ键的K4[Fe(CN)6]的物质的量为_____ mol。
(3)H 2SO4的酸性强于H2SO3酸性的原因是_______ 。
(4)FeS2晶体的晶胞结构如图所示。在晶胞中,Fe2+位于 所形成的
所形成的______ (填“正四面体”或“正八面体”)空隙;若晶胞参数为 a nm,密度为ρg∙cm−3,阿伏加德罗常数的值为NA ,则FeS2的摩尔质量 M=_______ (用含 a、ρ、 NA的代数式表示)。

(1)基态下Fe2+共有
(2)Fe2+形成的配合物亚铁氰化钾K4[Fe(CN)6]又称黄血盐,可用于检验Fe3+,与CN-互为等电子体的阴离子为
(3)H 2SO4的酸性强于H2SO3酸性的原因是
(4)FeS2晶体的晶胞结构如图所示。在晶胞中,Fe2+位于
 所形成的
所形成的
您最近一年使用:0次
【推荐1】铜及其化合物有许多特殊用途,最近科研人员用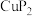 作电极电催化
作电极电催化 ,
, 经甲酸盐、乙醛最终转化为1-丁醇,铜则转化为
经甲酸盐、乙醛最终转化为1-丁醇,铜则转化为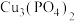 和
和 。回答下列问题:。
。回答下列问题:。
(1)基态磷原子的价电子排布图为_______ ,基态Cu原子电子占据最高能级的电子云轮廓图为_______ 形。
(2)Cu、O、P三种元素中,电负性由大到小的顺序为_______ 。
(3) 的空间构型为
的空间构型为_______ ,其中P采取_______ 杂化方式。
(4)1-丁醇、1-氯丁烷的沸点依次为118℃、78.2℃,前者沸点较高的原因是_______ 。
(5)Cu、Mn、Al形成的一种金属间化合物的晶体结构如图所示。已知晶胞参数为apm,内部正方形的边长为bpm,NA表示阿伏加德罗常数。

该晶体的密度为_______ (用含a、NA的代数式表示,不用化简);P、Q间的距离为_______ pm(要求同上)。
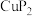 作电极电催化
作电极电催化 ,
, 经甲酸盐、乙醛最终转化为1-丁醇,铜则转化为
经甲酸盐、乙醛最终转化为1-丁醇,铜则转化为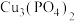 和
和 。回答下列问题:。
。回答下列问题:。(1)基态磷原子的价电子排布图为
(2)Cu、O、P三种元素中,电负性由大到小的顺序为
(3)
 的空间构型为
的空间构型为(4)1-丁醇、1-氯丁烷的沸点依次为118℃、78.2℃,前者沸点较高的原因是
(5)Cu、Mn、Al形成的一种金属间化合物的晶体结构如图所示。已知晶胞参数为apm,内部正方形的边长为bpm,NA表示阿伏加德罗常数。

该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铁(26Fe)、镍(28Ni)的单质及其化合物在医药、材料等领域有着广泛的应用。回答下列问题:
(1)基态Fe原子核外电子排布式为___________ ,Ni位于元素周期表的___________ 区。
(2)乳酸亚铁口服液是缺铁人群补铁保健品,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度分析,Fe2+易被氧化成Fe3+的原因是___________ 。
(3)FeCl3常用作净水剂、刻蚀剂等。
①FeCl3的熔点(306℃)显著低于FeF3的熔点(1000℃)的原因是___________ 。
②FeCl3水溶液中Fe3+可水解生成双核阳离子[Fe2(H2O)8(OH)2]4+,结构如下图,分析其能够形成双核阳离子的原因:___________ 。___________ 。
(1)基态Fe原子核外电子排布式为
(2)乳酸亚铁口服液是缺铁人群补铁保健品,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度分析,Fe2+易被氧化成Fe3+的原因是
(3)FeCl3常用作净水剂、刻蚀剂等。
①FeCl3的熔点(306℃)显著低于FeF3的熔点(1000℃)的原因是
②FeCl3水溶液中Fe3+可水解生成双核阳离子[Fe2(H2O)8(OH)2]4+,结构如下图,分析其能够形成双核阳离子的原因:


您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】下表列出了核电荷数为21~25的元素的最高正化合价,回答下列问题:
(1)写出下列元素基态原子的核外电子排布式:
Sc_______ ;Ti_______ ;Cr_______ ;Mn_______ 。
(2)已知基态铬原子的电子排布式是1s22s22p63s23p63d54s1,并不符合构造原理。人们常常会碰到客观事实与理论不相吻合的问题,当你遇到这样的问题时,你的态度是_______ 。
| 元素名称 | 钪 | 钛 | 钒 | 铬 | 锰 |
| 元素符号 | Sc | Ti | V | Cr | Mn |
| 核电荷数 | 21 | 22 | 23 | 24 | 25 |
| 最高正化合价 | +3 | +4 | +5 | +6 | +7 |
(1)写出下列元素基态原子的核外电子排布式:
Sc
(2)已知基态铬原子的电子排布式是1s22s22p63s23p63d54s1,并不符合构造原理。人们常常会碰到客观事实与理论不相吻合的问题,当你遇到这样的问题时,你的态度是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E均为短周期元素,非金属元素A的最外层电子数与其周期数相等,B的成对电子与未成对电子所占据的原子轨道数相等。单质B在单质C中充分燃烧生成BC2。 D+与C2-具有相同的电子数。A在E中燃烧,产物溶于水会得到一种强酸。
(1)B在元素周期表中的位置是________ ,写出一种工业制备单质E的化学方程式:_____ 。
(2)B、C、D组成的一种盐中,B的质量分数为17. 91%,D的质量分数为34. 3 3%。该盐的化学式为________ ,其阴离子中B原子的杂化方式为__________ 。
(3)由这些元素组成的某些物质的组成和结构信息如下表:
a的电子式为_________ ;b的化学式为________ ;c的空间构型为___________ 。
(1)B在元素周期表中的位置是
(2)B、C、D组成的一种盐中,B的质量分数为17. 91%,D的质量分数为34. 3 3%。该盐的化学式为
(3)由这些元素组成的某些物质的组成和结构信息如下表:
| 物质 | 组成和结构 |
| a | A、D两元素组成的离子化合物 |
| b | 由C、D两元素组成的含有非极性键的离子化合物 |
| c | 化学组成为BCE2 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】JohnB.Goodenough等三位科学家因在发展锂离子电池方面做出的贡献而获得了诺贝尔化学奖。回答下列问题:
(1)锰酸锂(LiMn2O4)电池具有原料成本低合成工艺简单等优点。原子中运动的电子有两种相反的身旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为___________ 。基态Mn原子核外价层电子的运动状态有___________ 种。
(2)锂离子电池的电解液一般为溶有LiPF6的碳酸酯类有机溶剂,LiPF6遇水反应生成PF3和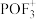 ,
,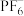 中心原子的价层电子对数为
中心原子的价层电子对数为___________ ,POF3的空间构型为___________ 。
(3)已知第三电离能数据:I3(Mn)=3246kJ·mol-1,I3(Fe)=2957kJ·mol-1.锰的第三电离能大于铁的第三电离能,其主要原因是___________ 。
(4)铋化锂被认为是很有潜力的正极材料,晶胞结构如图所示。
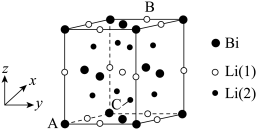
①晶胞可以看作是由铋原子构成的面心立方晶格,锂原子填充在其中的四面体和八面体空隙处,晶体的化学式为___________ 。
②图中原子坐标参数:A为(0,0,0),B为(1,0.5,1),则C的坐标为___________ ,Bi与Li(1)和Li(2)之间的最短距离的比为___________ 。
(1)锰酸锂(LiMn2O4)电池具有原料成本低合成工艺简单等优点。原子中运动的电子有两种相反的身旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Li原子,其核外电子自旋磁量子数的代数和为(2)锂离子电池的电解液一般为溶有LiPF6的碳酸酯类有机溶剂,LiPF6遇水反应生成PF3和
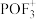 ,
,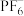 中心原子的价层电子对数为
中心原子的价层电子对数为(3)已知第三电离能数据:I3(Mn)=3246kJ·mol-1,I3(Fe)=2957kJ·mol-1.锰的第三电离能大于铁的第三电离能,其主要原因是
(4)铋化锂被认为是很有潜力的正极材料,晶胞结构如图所示。

①晶胞可以看作是由铋原子构成的面心立方晶格,锂原子填充在其中的四面体和八面体空隙处,晶体的化学式为
②图中原子坐标参数:A为(0,0,0),B为(1,0.5,1),则C的坐标为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】X、Y、Z均为短周期元素,可形成X2Z和YZ2两种化合物。X、Y、Z的原子序数依次增大,X原子的K层的电子数目只有一个,Y位于X的下一周期,它的最外层电子数比K层多2个,而Z原子核外的最外层电子数比次外层电子数少2个。
(1)它们的元素符号分别为X___________ 、Y___________ 、Z___________ 。
(2)用价电子对互斥理论判断:
(1)它们的元素符号分别为X
(2)用价电子对互斥理论判断:
| 物质 | 价电子对数 | 轨道杂化形式 | 分子的形状 | |
| 成键电子对数 | 孤电子对数 | |||
| X2Z | ||||
| YZ2 | ||||
您最近一年使用:0次



