钛白粉(纳米级)可作为白色无机颜料,广泛应用于功能陶瓷、催化剂、化妆品和光敏材料等行业。一种由硫酸制取白色颜料钛白粉 的生产工艺如下。【原料钛铁矿
的生产工艺如下。【原料钛铁矿 中往往含有
中往往含有 、
、 、
、 、
、 、
、 等杂质】
等杂质】
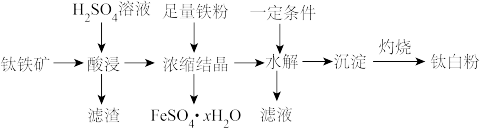
已知:①“酸浸”后,钛主要以 形式存在,
形式存在, 在热水中易水解。
在热水中易水解。
②饱和 溶液在低于
溶液在低于 时,析出
时,析出 ;在
;在 时,析出
时,析出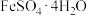 ;在高于
;在高于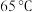 时,析出
时,析出 。
。
③ 不溶于水和稀酸。
不溶于水和稀酸。
回答下列问题:
(1) 中钛的化合价为
中钛的化合价为_______ ,“一定条件”是_______ 。
(2)
_______ ,为了得到较纯净的副产品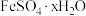 ,在“浓缩结晶”之前要进行的操作是
,在“浓缩结晶”之前要进行的操作是_______ 。
(3)“滤渣”的主要成分为_______ (填化学式)。
(4)写出“沉淀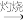 钛白粉”的化学方程式:
钛白粉”的化学方程式:_______ 。
(5)用氧化还原滴定法测定 的质量分数:一定条件下,将
的质量分数:一定条件下,将 溶解并还原为
溶解并还原为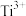 ,再以
,再以 溶液作指示剂,用新配制的
溶液作指示剂,用新配制的 标准溶液滴定
标准溶液滴定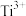 至全部生成
至全部生成 。滴定分析时,称取
。滴定分析时,称取 (摩尔质量为
(摩尔质量为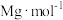 )样品
)样品 ,消耗
,消耗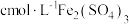 标准溶液
标准溶液 :
:
①写出用 标准溶液滴定
标准溶液滴定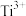 至全部生成
至全部生成 时发生反应的离子方程式:
时发生反应的离子方程式:_______ 。
②达到滴定终点的现象为_______ 。
③ 的质量分数为
的质量分数为_______ (用含M、w、c、V的代数式表示)。
 的生产工艺如下。【原料钛铁矿
的生产工艺如下。【原料钛铁矿 中往往含有
中往往含有 、
、 、
、 、
、 、
、 等杂质】
等杂质】
已知:①“酸浸”后,钛主要以
 形式存在,
形式存在, 在热水中易水解。
在热水中易水解。②饱和
 溶液在低于
溶液在低于 时,析出
时,析出 ;在
;在 时,析出
时,析出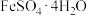 ;在高于
;在高于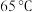 时,析出
时,析出 。
。③
 不溶于水和稀酸。
不溶于水和稀酸。回答下列问题:
(1)
 中钛的化合价为
中钛的化合价为(2)

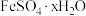 ,在“浓缩结晶”之前要进行的操作是
,在“浓缩结晶”之前要进行的操作是(3)“滤渣”的主要成分为
(4)写出“沉淀
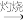 钛白粉”的化学方程式:
钛白粉”的化学方程式:(5)用氧化还原滴定法测定
 的质量分数:一定条件下,将
的质量分数:一定条件下,将 溶解并还原为
溶解并还原为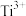 ,再以
,再以 溶液作指示剂,用新配制的
溶液作指示剂,用新配制的 标准溶液滴定
标准溶液滴定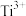 至全部生成
至全部生成 。滴定分析时,称取
。滴定分析时,称取 (摩尔质量为
(摩尔质量为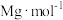 )样品
)样品 ,消耗
,消耗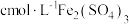 标准溶液
标准溶液 :
:①写出用
 标准溶液滴定
标准溶液滴定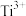 至全部生成
至全部生成 时发生反应的离子方程式:
时发生反应的离子方程式:②达到滴定终点的现象为
③
 的质量分数为
的质量分数为
更新时间:2022-05-01 21:13:17
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】含氯物质在生产生活中有重要作用。
(一)实验室利用下面的装置制备氯水和漂白液(尾气处理装置略)
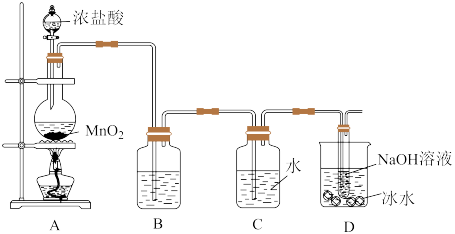
(1)盛放 粉末的仪器名称是
粉末的仪器名称是___________ ,A中发生反应的化学方程式为___________ 。
(2)装置B的作用是___________ 。
(3)D中可以得到漂白液,反应的离子方程式是___________ ,采用冰水浴冷却的目的是___________ 。
(二)测定漂白液中NaClO的含量
步骤①:取20mL制得的漂白液,加入过量盐酸酸化的KI溶液,充分反应;
步骤②:加入淀粉做指示剂,用 标准溶液滴定至终点,发生反应:
标准溶液滴定至终点,发生反应: 。
。
(4)步骤①中发生反应的离子方程式为___________ ;最终平均用去 标准溶液,测得NaClO的含量为
标准溶液,测得NaClO的含量为___________  (结果保留2位小数)。
(结果保留2位小数)。
(三)探究氯水的性质
(5)装置C中得到饱和的氯水,往淀粉-KI溶液中逐滴加入氯水至氯水过量,观察到溶液先变蓝后褪色。某组同学对褪色原因进行探究。
①查阅资料知道:氯水不能氧化淀粉;氯水不能氧化由 和淀粉形成的蓝色化合物。
和淀粉形成的蓝色化合物。
②提出假设: 被过量的氯水氧化为
被过量的氯水氧化为 ;
;
请帮助该组同学设计实验证明该假设成立:___________ 。
③有同学在实验过程中没有看到蓝色,而是看到了蓝褐色;经分析可能是发生了反应: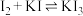 (棕红色络合物),干扰实验现象的观察。请帮助该同学设计实验证明上述分析:
(棕红色络合物),干扰实验现象的观察。请帮助该同学设计实验证明上述分析:___________ 。
(一)实验室利用下面的装置制备氯水和漂白液(尾气处理装置略)

(1)盛放
 粉末的仪器名称是
粉末的仪器名称是(2)装置B的作用是
(3)D中可以得到漂白液,反应的离子方程式是
(二)测定漂白液中NaClO的含量
步骤①:取20mL制得的漂白液,加入过量盐酸酸化的KI溶液,充分反应;
步骤②:加入淀粉做指示剂,用
 标准溶液滴定至终点,发生反应:
标准溶液滴定至终点,发生反应: 。
。(4)步骤①中发生反应的离子方程式为
 标准溶液,测得NaClO的含量为
标准溶液,测得NaClO的含量为 (结果保留2位小数)。
(结果保留2位小数)。(三)探究氯水的性质
(5)装置C中得到饱和的氯水,往淀粉-KI溶液中逐滴加入氯水至氯水过量,观察到溶液先变蓝后褪色。某组同学对褪色原因进行探究。
①查阅资料知道:氯水不能氧化淀粉;氯水不能氧化由
 和淀粉形成的蓝色化合物。
和淀粉形成的蓝色化合物。②提出假设:
 被过量的氯水氧化为
被过量的氯水氧化为 ;
;请帮助该组同学设计实验证明该假设成立:
③有同学在实验过程中没有看到蓝色,而是看到了蓝褐色;经分析可能是发生了反应:
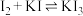 (棕红色络合物),干扰实验现象的观察。请帮助该同学设计实验证明上述分析:
(棕红色络合物),干扰实验现象的观察。请帮助该同学设计实验证明上述分析:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】某化学兴趣小组拟实验探究锡及其化合物的部分性质。经查阅资料知:Sn 的熔点为231 °C;SnCl2易被氧化,且易水解; Sn(OH)2常温下易分解; SnCl4常温下为无色液体,熔点为.-33°C,沸点为114°C,易水解。回答下列问题:
(1)该小组用以下流程制备SnSO4晶体:
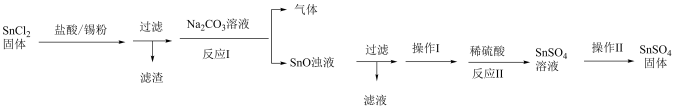
①Sn为50号元素,请写出Sn在元素周期表的位置___________________ ;
②在上述流程中,加入锡粉的作用为________________ ;
③反应Ⅰ的离子方程式为_______________________ ;
④操作Ⅰ为沉淀的洗涤,请简述如何判断沉淀已洗涤干净?________ ;操作Ⅱ中,实验操作包括_______ 、过滤、洗涤、干燥等一系列操作。
(2)用熔融的锡与干燥的氯气制备SnCl4,实验装置如下:
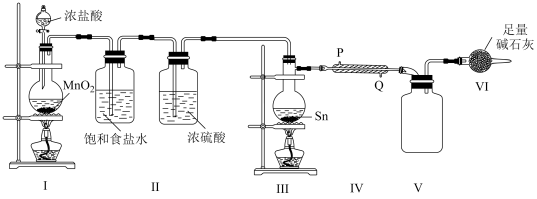
①SnCl4是______ 分子(填“极性”或“非极性”)。
②装置Ⅲ中盛装药品Sn的仪器名称是_______ ;装置Ⅵ中碱石灰的作用为______ 。
(3)该小组通过下列方法测定所用锡粉的纯度:取锡粉1.226g溶于稀硫酸中,加入过量的FeCl3溶液,再用0.1000mol·L-1的K2Cr2O7溶液滴定含有Fe2+的溶液,消耗K2Cr2O7溶液32.00mL。已知①Sn+H+→H2↑+Sn2+; ②Sn2++ Fe3+→Sn4+ + Fe2+;③ + Fe2+→Cr3++Fe3+ (方程式均未配平)。则锡粉的质量分数为(杂质不参与反应)
+ Fe2+→Cr3++Fe3+ (方程式均未配平)。则锡粉的质量分数为(杂质不参与反应)______ (结果保留三位有效数字)。
(1)该小组用以下流程制备SnSO4晶体:

①Sn为50号元素,请写出Sn在元素周期表的位置
②在上述流程中,加入锡粉的作用为
③反应Ⅰ的离子方程式为
④操作Ⅰ为沉淀的洗涤,请简述如何判断沉淀已洗涤干净?
(2)用熔融的锡与干燥的氯气制备SnCl4,实验装置如下:

①SnCl4是
②装置Ⅲ中盛装药品Sn的仪器名称是
(3)该小组通过下列方法测定所用锡粉的纯度:取锡粉1.226g溶于稀硫酸中,加入过量的FeCl3溶液,再用0.1000mol·L-1的K2Cr2O7溶液滴定含有Fe2+的溶液,消耗K2Cr2O7溶液32.00mL。已知①Sn+H+→H2↑+Sn2+; ②Sn2++ Fe3+→Sn4+ + Fe2+;③
 + Fe2+→Cr3++Fe3+ (方程式均未配平)。则锡粉的质量分数为(杂质不参与反应)
+ Fe2+→Cr3++Fe3+ (方程式均未配平)。则锡粉的质量分数为(杂质不参与反应)
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】Ⅰ.工业废水中常含有一定量氧化性较强的 ,利用滴定原理测定
,利用滴定原理测定 含量的方法如下:
含量的方法如下:
步骤一:量取30.00mL废水于锥形瓶中,加入适量稀硫酸酸化。
步骤二:加入过量的碘化钾溶液充分反应: 。
。
步骤三:向锥形瓶中滴入几滴指示剂。用滴定管量取0.1000mol/L 溶液进行滴定,数据记录如表:(
溶液进行滴定,数据记录如表:( )
)
(1)步骤Ⅰ量取30.00mL废水选择的仪器是___________ 。
(2)步骤Ⅲ中滴定达到终点时的实验现象是___________ 。
(3)步骤Ⅲ中a的读数如图所示,则:___________ mL。
②计算废水中 含量为
含量为___________ mol/L。
(4)以下操作会造成废水中 含量测定值偏高的是___________(填字母)。
含量测定值偏高的是___________(填字母)。
Ⅱ.佛尔哈德法可测定经过提纯后的产品中 的含量:准确称取1.705g样品在水解瓶中摇动至完全水解,将水解液配成100mL,取10.00mL于锥形瓶中,加
的含量:准确称取1.705g样品在水解瓶中摇动至完全水解,将水解液配成100mL,取10.00mL于锥形瓶中,加 的
的 溶液20.00mL(
溶液20.00mL(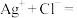
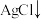 ),再加少许硝基苯,用力振荡,使沉淀被有机物覆盖,加入指示剂,用
),再加少许硝基苯,用力振荡,使沉淀被有机物覆盖,加入指示剂,用 KSCN标准溶液滴定过量的
KSCN标准溶液滴定过量的 至终点(
至终点( )。
)。
已知: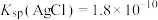 ,
,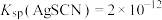
(5) 水解方程式为
水解方程式为___________ 。
(6)实验中,若不加硝基苯,测定 的纯度将
的纯度将___________ (填“偏大”“偏小”或“无影响”)。
 ,利用滴定原理测定
,利用滴定原理测定 含量的方法如下:
含量的方法如下:步骤一:量取30.00mL废水于锥形瓶中,加入适量稀硫酸酸化。
步骤二:加入过量的碘化钾溶液充分反应:
 。
。步骤三:向锥形瓶中滴入几滴指示剂。用滴定管量取0.1000mol/L
 溶液进行滴定,数据记录如表:(
溶液进行滴定,数据记录如表:( )
)| 滴定次数 |  溶液起始读数/mL 溶液起始读数/mL |  溶液终点读数/mL 溶液终点读数/mL |
| 第一次 | 1.02 | 19.03 |
| 第二次 | 2.00 | 19.99 |
| 第三次 | 0.20 | a |
(1)步骤Ⅰ量取30.00mL废水选择的仪器是
(2)步骤Ⅲ中滴定达到终点时的实验现象是
(3)步骤Ⅲ中a的读数如图所示,则:

②计算废水中
 含量为
含量为(4)以下操作会造成废水中
 含量测定值偏高的是___________(填字母)。
含量测定值偏高的是___________(填字母)。| A.滴定开始时滴定管尖嘴处有气泡,滴定后气泡消失 |
B.量取 溶液的滴定管用蒸馏水洗后未用标准液润洗 溶液的滴定管用蒸馏水洗后未用标准液润洗 |
| C.滴定终点读数时,俯视滴定管的刻度 |
| D.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗 |
Ⅱ.佛尔哈德法可测定经过提纯后的产品中
 的含量:准确称取1.705g样品在水解瓶中摇动至完全水解,将水解液配成100mL,取10.00mL于锥形瓶中,加
的含量:准确称取1.705g样品在水解瓶中摇动至完全水解,将水解液配成100mL,取10.00mL于锥形瓶中,加 的
的 溶液20.00mL(
溶液20.00mL(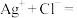
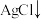 ),再加少许硝基苯,用力振荡,使沉淀被有机物覆盖,加入指示剂,用
),再加少许硝基苯,用力振荡,使沉淀被有机物覆盖,加入指示剂,用 KSCN标准溶液滴定过量的
KSCN标准溶液滴定过量的 至终点(
至终点( )。
)。已知:
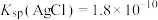 ,
,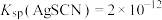
(5)
 水解方程式为
水解方程式为(6)实验中,若不加硝基苯,测定
 的纯度将
的纯度将
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】稀土在电子、激光、核工业、超导等诸多高科技领域有广泛的应用。钪(Sc)是一种稀土金属,利用钛尾矿回收金属钪和草酸的工艺流程如图1所示。回答下列问题:

已知:①xNH4Cl·yScF3·zH2O是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。
②“脱水除铵”是复盐沉淀的热分解过程。
③25℃时,部分物质的相关信息如表所示:
(1)“焙烧”过程生成Sc2O3的化学方程式为___________ 。
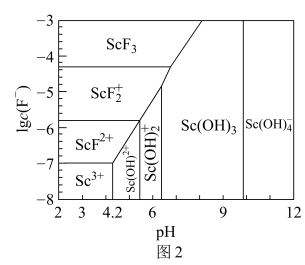
(2)含钪元素的微粒与lgc(F-)、pH的关系如下图所示,用氨水调节溶液的pH值,控制pH的范围是3.5<pH<___________ 。
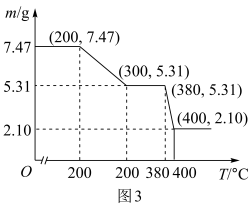
(3)“脱水除铵”过程中固体质量与温度的关系如下图所示,其中在380-400℃过程中会有白烟冒出,保温至无烟气产生,即得到 ScF3,由图3中数据可得x:z=___________ 。
(4)传统制备ScF3的方法是先得到ScF3·6H2O沉淀,再高温脱水得ScF3,但通常含有ScOF杂质,原因是___________ 。(用化学方程式表示)。流程中“沉钪”后“脱水除铵”可制得纯度很高的ScF3,其原因是___________ 。
(5)将1.8mol PbSO4加到1L含有0.12mol/L H2C2O4的废水中。发生的离子反应为PbSO4(s)+H2C2O4(aq) PbC2O4(s)+2H+(aq)+ SO
PbC2O4(s)+2H+(aq)+ SO (aq),该反应的平衡常数K=
(aq),该反应的平衡常数K=___________ 。滤饼经浓硫酸处理后的“沉淀”是___________ (化学式)。

已知:①xNH4Cl·yScF3·zH2O是“沉钪”过程中ScF3与氯化物形成的复盐沉淀,在强酸中部分溶解。
②“脱水除铵”是复盐沉淀的热分解过程。
③25℃时,部分物质的相关信息如表所示:
| Ksp(PbSO4) | Ksp(PbC2O4) | Ka1(H2C2O4) | Ka2(H2C2O4) |
| 2.0×10-8 | 5.0×10-10 | 6.0×10-2 | 6.25×10-5 |
(2)含钪元素的微粒与lgc(F-)、pH的关系如下图所示,用氨水调节溶液的pH值,控制pH的范围是3.5<pH<

(3)“脱水除铵”过程中固体质量与温度的关系如下图所示,其中在380-400℃过程中会有白烟冒出,保温至无烟气产生,即得到 ScF3,由图3中数据可得x:z=

(4)传统制备ScF3的方法是先得到ScF3·6H2O沉淀,再高温脱水得ScF3,但通常含有ScOF杂质,原因是
(5)将1.8mol PbSO4加到1L含有0.12mol/L H2C2O4的废水中。发生的离子反应为PbSO4(s)+H2C2O4(aq)
 PbC2O4(s)+2H+(aq)+ SO
PbC2O4(s)+2H+(aq)+ SO (aq),该反应的平衡常数K=
(aq),该反应的平衡常数K=
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】亚硫酰氯(SOCl2)又名氯化亚砜,是一种无色或淡黄色发烟液体,有强烈刺激性气味,其熔点-105℃,沸点79℃,140℃以上时易分解。遇水剧烈反应生成SO2和另一种酸性气体,常用作脱水剂,主要用于制造酰基氯化物,还用于医药、农药、染料等的生产。
实验室合成SOCl2的原理之一为SO2+Cl2+SCl2 2SOCl2,部分装置(夹持、加热装置略去)如图所示。
2SOCl2,部分装置(夹持、加热装置略去)如图所示。
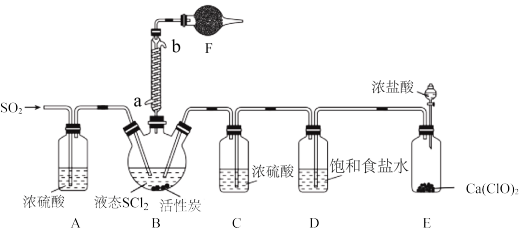
(1)①仪器F的名称为_______ ,所盛的试剂是______ ;
②装置A、C除干燥气体外,另一作用可能是__________________________________ ;
如果没有A、C,二氧化硫与氯气在装置B中会有副反应发生,该反应的离子方程式为_________
③E中反应的化学方程式:_______________________________ 。
(2)甲同学认为SOCl2和FeCl3∙6H2O混合加热可制得无水FeCl3,但乙同学认为该实验可能发生副反应使产品不纯。乙同学设计如下实验判断副反应的可能性:取少量FeCl3∙6H2O于试管中,加入足量SOCl2,充分反应后向试管中加水溶解,用四支试管各取溶解后的溶液少许,分别进行下列实验,通过现象能验证发生副反应的是_______ (填选项字母)。
a.滴加BaCl2溶液 b.滴加K3[Fe(CN)6]溶液
c.滴加酸性KMnO4溶液 d.滴加溴水
(3)分离产物后,向获得的SOCl2中加入足量NaOH溶液,振荡、静置得到无色溶液,检验该溶液中存在Cl-的需要用到的试剂是_______________________
实验室合成SOCl2的原理之一为SO2+Cl2+SCl2
 2SOCl2,部分装置(夹持、加热装置略去)如图所示。
2SOCl2,部分装置(夹持、加热装置略去)如图所示。
(1)①仪器F的名称为
②装置A、C除干燥气体外,另一作用可能是
如果没有A、C,二氧化硫与氯气在装置B中会有副反应发生,该反应的离子方程式为
③E中反应的化学方程式:
(2)甲同学认为SOCl2和FeCl3∙6H2O混合加热可制得无水FeCl3,但乙同学认为该实验可能发生副反应使产品不纯。乙同学设计如下实验判断副反应的可能性:取少量FeCl3∙6H2O于试管中,加入足量SOCl2,充分反应后向试管中加水溶解,用四支试管各取溶解后的溶液少许,分别进行下列实验,通过现象能验证发生副反应的是
a.滴加BaCl2溶液 b.滴加K3[Fe(CN)6]溶液
c.滴加酸性KMnO4溶液 d.滴加溴水
(3)分离产物后,向获得的SOCl2中加入足量NaOH溶液,振荡、静置得到无色溶液,检验该溶液中存在Cl-的需要用到的试剂是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ.(1)在2L定容密闭容器中通入1molN2(g)和3molH2(g),发生反应:
3H2(g)+N2(g) 2NH3(g)△H<0,测得压强一时间图象如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图象。
2NH3(g)△H<0,测得压强一时间图象如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图象。
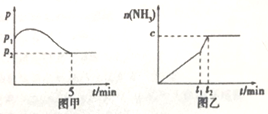
①若图中c=1.6mol,则改变的条件是__________ (填字母,下同);
A.升温 B.降温 C.加压 D.减压 E.加催化剂
②若图中c<1.6mol,则改变的条件是__________ (填字母);此时该反应的平衡常数__________ (填“增大”、“减小”、“不变”)。
(2)如图甲,平衡时氢气的转化率为____________ 。
Ⅱ.粗制的CuCl2·2H2O晶体中常含有Fe3+、Fe2+杂质,为制得纯净的氯化铜晶体,首先将其制成水溶液,再按下图所示的操作步骤进行提纯。
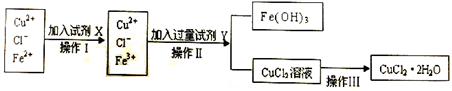
(1)操作Ⅰ时,常先加入合适的氧化剂,将Fe2+氧化为Fe3+,下列可选用的氧化剂是__________ 。
A.KMnO4 B.H2O2 C.Cl2 D.HNO3
(2)操作Ⅱ调整溶液的pH的Y试剂可选用下列中的__________ 。
A.NaOH(s) B.氨水 C.CuO(s) D.Cu(OH)2(s)
(3)已知溶度积常数如下表:
将溶液的pH调至pH=4时,使Fe3+完全转化为Fe(OH)3沉淀而除去,此时c(Fe3+)=__________ 。
(4)若将CuCl2溶液蒸干后,再灼烧,得到的固体是__________ (填化学式);操作Ⅲ后由CuCl2·2H2O晶体得到纯净无水CuCl2的合理操作是_____________________________________ 。
3H2(g)+N2(g)
 2NH3(g)△H<0,测得压强一时间图象如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图象。
2NH3(g)△H<0,测得压强一时间图象如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图象。
①若图中c=1.6mol,则改变的条件是
A.升温 B.降温 C.加压 D.减压 E.加催化剂
②若图中c<1.6mol,则改变的条件是
(2)如图甲,平衡时氢气的转化率为
Ⅱ.粗制的CuCl2·2H2O晶体中常含有Fe3+、Fe2+杂质,为制得纯净的氯化铜晶体,首先将其制成水溶液,再按下图所示的操作步骤进行提纯。

(1)操作Ⅰ时,常先加入合适的氧化剂,将Fe2+氧化为Fe3+,下列可选用的氧化剂是
A.KMnO4 B.H2O2 C.Cl2 D.HNO3
(2)操作Ⅱ调整溶液的pH的Y试剂可选用下列中的
A.NaOH(s) B.氨水 C.CuO(s) D.Cu(OH)2(s)
(3)已知溶度积常数如下表:
| 物质 | Cu(OH) | Fe(OH)2 | Fe(OH)3 |
| Ksp | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
将溶液的pH调至pH=4时,使Fe3+完全转化为Fe(OH)3沉淀而除去,此时c(Fe3+)=
(4)若将CuCl2溶液蒸干后,再灼烧,得到的固体是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】钛白粉(纳米级)广泛应用于功能陶瓷、催化剂、化妆品和光敏材料等白色无机颜料。是白色颜料中着色力最强的一种,具有优良的遮盖力和着色牢度,适用于不透明的白色制品。制备原料钛铁矿( )中往往含有
)中往往含有 、
、 、
、 、
、 、
、 等杂质。一种硫酸法制取白色颜料钛白粉(
等杂质。一种硫酸法制取白色颜料钛白粉( )生产工艺如下:
)生产工艺如下:
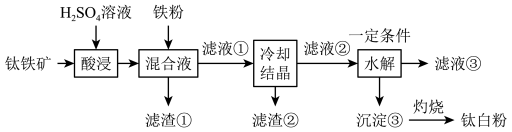
已知:①酸浸后,钛主要以 形式存在;
形式存在;
②强电解质 在溶液中仅能电离出
在溶液中仅能电离出 和一种阳离子。
和一种阳离子。
③ 不溶于水和稀酸。
不溶于水和稀酸。
(1)要提高酸浸速率,可采取的措施是___________ (写出一条即可)。
(2)滤渣①中除铁粉外,还可能含有的成分是___________ 。
(3)酸浸过程中, 发生反应的离子方程式
发生反应的离子方程式___________ 。
(4)加入铁粉的目的是还原体系中的 。为探究最佳反应条件,某实验室做了如下尝试。
。为探究最佳反应条件,某实验室做了如下尝试。
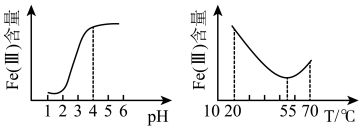
①在其它条件不变的情况下,体系中 (Ⅲ)[指
(Ⅲ)[指 和
和 等含正三价铁元素的微粒]含量随
等含正三价铁元素的微粒]含量随 变化如图1,试分析,在
变化如图1,试分析,在 介于4~6之间时,
介于4~6之间时, (Ⅲ)主要以
(Ⅲ)主要以___________ (填微粒化学式)形式存在。
②保持其它条件不变,体系中 (Ⅲ)含量随温度变化如图2,请从化学平衡原理角度分析,55℃后,
(Ⅲ)含量随温度变化如图2,请从化学平衡原理角度分析,55℃后, (Ⅲ)含量增大的原因是
(Ⅲ)含量增大的原因是___________ 。
(5)“水解”过程中得到的沉淀③的化学式为___________ 。
 )中往往含有
)中往往含有 、
、 、
、 、
、 、
、 等杂质。一种硫酸法制取白色颜料钛白粉(
等杂质。一种硫酸法制取白色颜料钛白粉( )生产工艺如下:
)生产工艺如下:
已知:①酸浸后,钛主要以
 形式存在;
形式存在;②强电解质
 在溶液中仅能电离出
在溶液中仅能电离出 和一种阳离子。
和一种阳离子。③
 不溶于水和稀酸。
不溶于水和稀酸。(1)要提高酸浸速率,可采取的措施是
(2)滤渣①中除铁粉外,还可能含有的成分是
(3)酸浸过程中,
 发生反应的离子方程式
发生反应的离子方程式(4)加入铁粉的目的是还原体系中的
 。为探究最佳反应条件,某实验室做了如下尝试。
。为探究最佳反应条件,某实验室做了如下尝试。①在其它条件不变的情况下,体系中
 (Ⅲ)[指
(Ⅲ)[指 和
和 等含正三价铁元素的微粒]含量随
等含正三价铁元素的微粒]含量随 变化如图1,试分析,在
变化如图1,试分析,在 介于4~6之间时,
介于4~6之间时, (Ⅲ)主要以
(Ⅲ)主要以②保持其它条件不变,体系中
 (Ⅲ)含量随温度变化如图2,请从化学平衡原理角度分析,55℃后,
(Ⅲ)含量随温度变化如图2,请从化学平衡原理角度分析,55℃后, (Ⅲ)含量增大的原因是
(Ⅲ)含量增大的原因是
(5)“水解”过程中得到的沉淀③的化学式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:
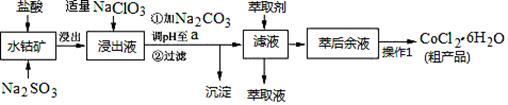
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式_________________ 。
(2)写出NaClO3发生反应的主要离子方程式________________ ;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式_________________ 。
(3)“加Na2CO3调pH至a”,过滤所得到的沉淀成分为___________________ 。
(4)“操作1”中包含3个基本实验操作,它们依次是_____________ 、____________ 和过滤。制得的CoCl2·6H2O在烘干时需减压烘干的原因是__________________ 。
(5)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的目的是______________ ;其使用的最佳pH范围是_________ 。
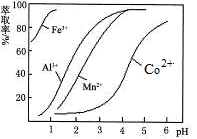
A.2.0~2.5 B.3.0~3.5
C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是______________________ 。(答一条即可)

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2·6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中Co2O3发生反应的离子方程式
(2)写出NaClO3发生反应的主要离子方程式
(3)“加Na2CO3调pH至a”,过滤所得到的沉淀成分为
(4)“操作1”中包含3个基本实验操作,它们依次是
(5)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的目的是

A.2.0~2.5 B.3.0~3.5
C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl2·6H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】有关物质间有如图所示的转化关系。已知B、D、G是常见的金属单质,E为常见的非金属单质,H常温下为无色液体,K为红棕色气体。
(1)F的电子式为______________ ,写出其与CO2反应的化学方程式并用双线桥标出电子转移的方向和数目:_________________________________
(2)反应①的离子方程式为____________________________________________ 。
(3)C与足量G反应的化学方程式为_____________________________________ 。其中,还原剂与氧化剂的物质的量之比为____________ ,检验反应中生成的金属离子的试剂为______________ 。
(4)Al能与A发生置换反应,生成物溶质与Na2CO3不能在溶液中大量共存,用离子方程式表示其原因:__________________________________
(5)I可由某种氢化物催化氧化得到,其反应的化学方程式为_______________________________ 。
(6) 漂白粉和F都应密封保存,写出漂白粉露置于空气中失效的化学方程式:________________________________________________________________________

(1)F的电子式为
(2)反应①的离子方程式为
(3)C与足量G反应的化学方程式为
(4)Al能与A发生置换反应,生成物溶质与Na2CO3不能在溶液中大量共存,用离子方程式表示其原因:
(5)I可由某种氢化物催化氧化得到,其反应的化学方程式为
(6) 漂白粉和F都应密封保存,写出漂白粉露置于空气中失效的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】氯化铈常用于石油催化剂、汽车尾气催化剂、中间化合物等行业。为充分利用资源,以废料(主要含 ,还含少量的
,还含少量的 、
、 、
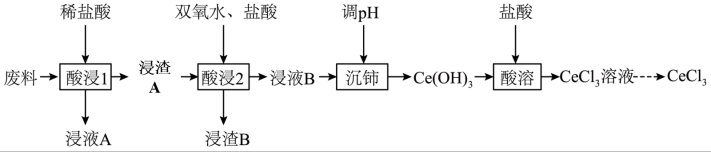
、 )为原料制备氯化铈的工艺流程如图所示:
)为原料制备氯化铈的工艺流程如图所示:
已知: 具有强氧化性,通常情况下不和无机酸反应。
具有强氧化性,通常情况下不和无机酸反应。
回答下列问题:
(1)加入过量稀盐酸后“浸渣A”的成分为___________ (填化学式),“浸渣B”的主要用途为___________ (填一种)。
(2)“酸浸2”中发生反应的离子方程式为___________ 。
(3) 及其氧化产物
及其氧化产物 可用于处理硝酸厂烟气中的氮氧化物(
可用于处理硝酸厂烟气中的氮氧化物( ),将烟气与
),将烟气与 的混合气体通入
的混合气体通入 与
与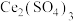 的混合溶液中,其转化过程如下图:
的混合溶液中,其转化过程如下图:

该处理过程中可减少下列环境问题产生___________ (填序号)。
①酸雨 ②光化学烟雾 ③白色污染
(4)取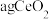 ,经铝热反应可得
,经铝热反应可得 ,该铝热反应的化学方程式为
,该铝热反应的化学方程式为___________ ,该反应中铈的产率为___________ (用含a、b的代数式表示)。
 ,还含少量的
,还含少量的 、
、 、
、 )为原料制备氯化铈的工艺流程如图所示:
)为原料制备氯化铈的工艺流程如图所示:
已知:
 具有强氧化性,通常情况下不和无机酸反应。
具有强氧化性,通常情况下不和无机酸反应。回答下列问题:
(1)加入过量稀盐酸后“浸渣A”的成分为
(2)“酸浸2”中发生反应的离子方程式为
(3)
 及其氧化产物
及其氧化产物 可用于处理硝酸厂烟气中的氮氧化物(
可用于处理硝酸厂烟气中的氮氧化物( ),将烟气与
),将烟气与 的混合气体通入
的混合气体通入 与
与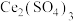 的混合溶液中,其转化过程如下图:
的混合溶液中,其转化过程如下图:
该处理过程中可减少下列环境问题产生
①酸雨 ②光化学烟雾 ③白色污染
(4)取
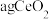 ,经铝热反应可得
,经铝热反应可得 ,该铝热反应的化学方程式为
,该铝热反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】乳酸亚铁晶体([CH3CH(OH)COO]2Fe·3H2O ,相对分子质量为288)易溶于水,是一种很好的补铁剂,可由乳酸[CH3CH(OH)COOH]与FeCO3反应制得。I.碳酸亚铁的制备(装置如图所示)

(1)仪器B的名称是______ ;实验操作如下:打开k1、k2,加入适量稀硫酸,关闭k1,使反应进行一段时间,其目的是______ 。
(2)接下来要使仪器C中的制备反应发生,需要进行的操作是______ ,其反应的离子方程式为______ 。
(3)仪器C中混合物经过滤、洗涤得到FeCO3沉淀,检验其是否洗净的方法是____ 。
Ⅱ乳酸亚铁的制备及铁元素含量测定
(4)向纯净FeCO3固体中加入足量乳酸溶液,在75℃下搅拌使之充分反应,经过滤,在______ 的条件下,经低温蒸发等操作后,获得乳酸亚铁晶体。
(5)两位同学分别用不同的方案进行铁元素含量测定:
①甲同学通过KMnO4滴定法测定样品中Fe2+的含量计算样品纯度。在操作均正确的前提下,所得纯度总是大于100%,其原因可能是______
②乙同学经查阅资料后改用碘量法测定铁元素的含量计算样品纯度。称取3.000g样品,灼烧完全灰化,加足量盐酸溶解,取所有可溶物配成100mL溶液。吸取 25.00mL该溶液加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用0.100 mol·L-1硫代硫酸钠溶液滴定(已知: I2+2S2O32-=S4O62-+2I-),当溶液______ ,即为滴定终点;平行滴定3次,硫代硫酸钠溶液的平均用量为24.80 mL,则样品纯度为______ %保留1位小数 。

(1)仪器B的名称是
(2)接下来要使仪器C中的制备反应发生,需要进行的操作是
(3)仪器C中混合物经过滤、洗涤得到FeCO3沉淀,检验其是否洗净的方法是
Ⅱ乳酸亚铁的制备及铁元素含量测定
(4)向纯净FeCO3固体中加入足量乳酸溶液,在75℃下搅拌使之充分反应,经过滤,在
(5)两位同学分别用不同的方案进行铁元素含量测定:
①甲同学通过KMnO4滴定法测定样品中Fe2+的含量计算样品纯度。在操作均正确的前提下,所得纯度总是大于100%,其原因可能是
②乙同学经查阅资料后改用碘量法测定铁元素的含量计算样品纯度。称取3.000g样品,灼烧完全灰化,加足量盐酸溶解,取所有可溶物配成100mL溶液。吸取 25.00mL该溶液加入过量KI溶液充分反应,然后加入几滴淀粉溶液,用0.100 mol·L-1硫代硫酸钠溶液滴定(已知: I2+2S2O32-=S4O62-+2I-),当溶液
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】实验室采用三氟化硼(BF3)与氯化铝(AlCl3)加热的方法制备三氯化硼(BCl3),装置如图所示(夹持装置及加热装置略)。
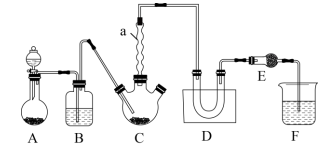
已知:Ⅰ.相关物质的沸点如下表
Ⅱ.三氯化硼(BCl3)易水解。
回答下列问题:
(1)将氟硼酸钾(KBF4)和硼酐(B2O3)一起研磨均匀加入 A 中的圆底烧瓶,滴入浓硫酸并加热,除产生BF3气体外,还生成一种酸式盐,则发生反应的化学方程式为___________ 。
(2)实验开始时,A、C两处加热装置应先加热 A 处,原因是___________ 。
(3)装置B中浓硫酸的作用是______ 和观察气泡,控制气体流速。
(4)装置C中仪器a的作用是防止产品中混有________ (填化学式),影响纯度。
(5)装置D进行________ (填“冰水浴”或“热水浴”)可得到产品。如果缺少装置E,造成的影响为_____ 。
(6)C中2.50g无水氯化铝完全反应后,取下U形管并注入水,完全反应生成盐酸和硼酸( H3BO3是一元弱酸),将所得溶液加水稀释到100mL,取10mL加入锥形瓶中滴入2滴酚酞溶液,用0.50mol/L的NaOH溶液滴定至终点,消耗NaOH溶液的体积为12.00 mL,则BCl3的产率为_______ %。

已知:Ⅰ.相关物质的沸点如下表
| 物质 | BF3 | BCl3 | AlCl3 | AlF3 |
| 沸点 | -99.9℃ | 12.5℃ | 180℃升华 | 1276℃升华 |
回答下列问题:
(1)将氟硼酸钾(KBF4)和硼酐(B2O3)一起研磨均匀加入 A 中的圆底烧瓶,滴入浓硫酸并加热,除产生BF3气体外,还生成一种酸式盐,则发生反应的化学方程式为
(2)实验开始时,A、C两处加热装置应先加热 A 处,原因是
(3)装置B中浓硫酸的作用是
(4)装置C中仪器a的作用是防止产品中混有
(5)装置D进行
(6)C中2.50g无水氯化铝完全反应后,取下U形管并注入水,完全反应生成盐酸和硼酸( H3BO3是一元弱酸),将所得溶液加水稀释到100mL,取10mL加入锥形瓶中滴入2滴酚酞溶液,用0.50mol/L的NaOH溶液滴定至终点,消耗NaOH溶液的体积为12.00 mL,则BCl3的产率为
您最近一年使用:0次



