回答下列问题:
(1)配离子[Cu(NH3)4]2+中存在配位键,NH3分子将孤电子对(N原子最外层未参与成键的电子对)单向提供给Cu2+。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是____ 。
(2)已知顺丁烯二酸的结构为 ,反丁烯二酸的结构为
,反丁烯二酸的结构为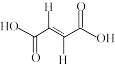 ’有关丁烯二酸的电离平衡常数如表(pKa=-lgKa):
’有关丁烯二酸的电离平衡常数如表(pKa=-lgKa):
顺丁烯二酸的Ka2小于反丁烯二酸的Ka2,原因为____ 。
(1)配离子[Cu(NH3)4]2+中存在配位键,NH3分子将孤电子对(N原子最外层未参与成键的电子对)单向提供给Cu2+。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是
(2)已知顺丁烯二酸的结构为
 ,反丁烯二酸的结构为
,反丁烯二酸的结构为 ’有关丁烯二酸的电离平衡常数如表(pKa=-lgKa):
’有关丁烯二酸的电离平衡常数如表(pKa=-lgKa):| pKa1 | pKa2 | |
| 顺丁烯二酸 | 1.32 | 6.23 |
| 反丁烯二酸 | 3.02 | 4.38 |
顺丁烯二酸的Ka2小于反丁烯二酸的Ka2,原因为
更新时间:2022-05-23 09:17:31
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】锂—磷酸氧铜电池正极的活性物质是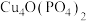 ,可通过下列反应制备:
,可通过下列反应制备: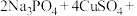
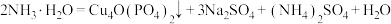 。
。
(1)写出基态 的电子排布式:
的电子排布式:_______________ 。
(2)P、S元素第一电离能大小关系为_______________ ,原因是_______________ 。
(3)氨基乙酸铜分子结构如图所示,碳原子的杂化方式为_______________ ,基态碳原子核外电子有_______________ 种运动状态。 ,生成配合物
,生成配合物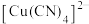 ,则
,则 该配合物含有
该配合物含有 键的数目为
键的数目为_______________ ( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(5)晶体铜的晶胞结构如图甲所示,原子之间相对位置关系的平面图如图乙所示,铜原子的配位数为_______________ ,铜的原子半径为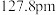 ,
, 表示阿伏加德罗常数的值,晶体铜的密度为
表示阿伏加德罗常数的值,晶体铜的密度为_______________  (列出计算式即可)。
(列出计算式即可)。
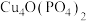 ,可通过下列反应制备:
,可通过下列反应制备: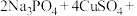
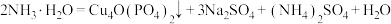 。
。(1)写出基态
 的电子排布式:
的电子排布式:(2)P、S元素第一电离能大小关系为
(3)氨基乙酸铜分子结构如图所示,碳原子的杂化方式为
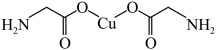
 ,生成配合物
,生成配合物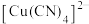 ,则
,则 该配合物含有
该配合物含有 键的数目为
键的数目为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(5)晶体铜的晶胞结构如图甲所示,原子之间相对位置关系的平面图如图乙所示,铜原子的配位数为
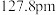 ,
, 表示阿伏加德罗常数的值,晶体铜的密度为
表示阿伏加德罗常数的值,晶体铜的密度为 (列出计算式即可)。
(列出计算式即可)。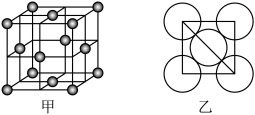
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】三明清流“天芳悦潭”温泉富含珍稀“锗”元素。其中锗石含有人体所需的硒、锌、镍、钴、锰、镁、钙等30多种对人体有益的微量元素。回答下列问题:
(1)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠: ;二锗酸钠:
;二锗酸钠: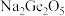 等),也能形成类似于烷烃的锗烷(
等),也能形成类似于烷烃的锗烷( )。
)。
① 中锗原子的杂化方式是
中锗原子的杂化方式是_______ 。
②推测1mol 中含有的σ键的数目是
中含有的σ键的数目是_______ (用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(2)利用离子液体 可电沉积还原金属Ge,其熔点只有7℃,其中
可电沉积还原金属Ge,其熔点只有7℃,其中 结构如图所示。
结构如图所示。

①该物质的晶体类型是_______ 。
② 中组成元素的电负性由小到大的顺序是
中组成元素的电负性由小到大的顺序是_______ 。
(3)独立的 分子中H−N−H的键角约为
分子中H−N−H的键角约为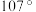 ,
, 中H−N−H的键角
中H−N−H的键角_______ 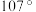 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
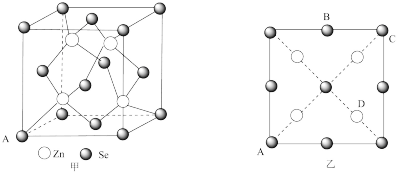
(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是_______ ;已知晶胞边长为apm,乙图为甲图的俯视图,A点坐标为(0,0,0),B点坐标为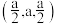 ,则D点坐标为
,则D点坐标为_______ ;若该晶胞密度为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值 为
为_______ (只列出计算式)。
(1)锗与碳同族,性质和结构有一定的相似性,锗元素能形成无机化合物(如锗酸钠:
 ;二锗酸钠:
;二锗酸钠: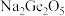 等),也能形成类似于烷烃的锗烷(
等),也能形成类似于烷烃的锗烷( )。
)。①
 中锗原子的杂化方式是
中锗原子的杂化方式是②推测1mol
 中含有的σ键的数目是
中含有的σ键的数目是 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(2)利用离子液体
 可电沉积还原金属Ge,其熔点只有7℃,其中
可电沉积还原金属Ge,其熔点只有7℃,其中 结构如图所示。
结构如图所示。
①该物质的晶体类型是
②
 中组成元素的电负性由小到大的顺序是
中组成元素的电负性由小到大的顺序是(3)独立的
 分子中H−N−H的键角约为
分子中H−N−H的键角约为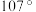 ,
, 中H−N−H的键角
中H−N−H的键角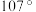 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图甲所示,该晶胞中硒原子的配位数是
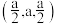 ,则D点坐标为
,则D点坐标为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值 为
为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】AgNO3是重要的化学试剂,常用于化学检验、医药和电子工业。回答下列问题:
(1)Ag与Cu为同族紧邻元素,二者基态原子的价电子排布相似,Ag在元素周期表中的位置为______ 。
(2)基态Ag+的价电子排布图为______ ; 的空间构型为
的空间构型为______ 。
(3)由AgNO3制备的[Ag(NH3)2]OH可用于检验醛基。[Ag(NH3)2]OH中向中心原子提供孤电子对的原子为______ ;若分子式为C3H6O的有机物经检验含醛基,则其分子中碳原子的杂化方式为______ 。
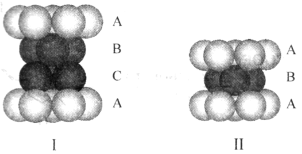
(4)银晶体为面心立方堆积,下图中可以表示银的堆积方式的为______ (填标号);银晶胞的边长为apm,则银晶胞的密度为______ g∙cm-3(用含a、NA的计算式表示)。
(1)Ag与Cu为同族紧邻元素,二者基态原子的价电子排布相似,Ag在元素周期表中的位置为
(2)基态Ag+的价电子排布图为
 的空间构型为
的空间构型为(3)由AgNO3制备的[Ag(NH3)2]OH可用于检验醛基。[Ag(NH3)2]OH中向中心原子提供孤电子对的原子为
(4)银晶体为面心立方堆积,下图中可以表示银的堆积方式的为

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】现有四种系列同族元素形成的物质,它们的沸点(℃,P=1.01×105Pa)如下表所示,
试根据上表回答下列问题
(1)a为____________ 色液体;b的分子式为_______________ 。
(2)写出②系列中物质主要化学性质的递变规律(任写一种)____________________ ;能够说明该递变规律的化学事实是_________________________
(任举一例,用离子方程式表示)。
(3)除极少数情况外,上述四种系列中物质的沸点与相对分子质量之间均存在一定的关系,该关系是___________________________________________________________________ 。
(4)上表中,______ 和______ 两种物质的沸点较同系列其它物质反常,反常的主要原因是___________________________________________________________________________ 。
| ① | He -268.8 | Ne -249.5 | Ar (x) | Kr -151.7 |
| ② | F2-187.0 | Cl2-33.6 | (a) 58.7 | I2184.0 |
| ③ | HF (y) | HCl -84.0 | HBr -67.0 | HI -35.3 |
| ④ | H2O (z) | H2S -60.2 | (b) -42.0 | H2Te -1.8 |
试根据上表回答下列问题
(1)a为
(2)写出②系列中物质主要化学性质的递变规律(任写一种)
(任举一例,用离子方程式表示)。
(3)除极少数情况外,上述四种系列中物质的沸点与相对分子质量之间均存在一定的关系,该关系是
(4)上表中,
您最近一年使用:0次
【推荐2】(1)比较 和
和 结合H+的能力强弱:
结合H+的能力强弱:
_____  (填“)”、“<”或“=”),用一个化学方程式说明
(填“)”、“<”或“=”),用一个化学方程式说明______________________________ 。
(2)CaC2是离子化合物,各原子均满足8电子稳定结构。写出CaC2的电子式__________ 。
(3)在常压下,甲醇的沸点(65℃)比甲醛的沸点(﹣19℃)高。主要原因是_______________ 。
 和
和 结合H+的能力强弱:
结合H+的能力强弱:
 (填“)”、“<”或“=”),用一个化学方程式说明
(填“)”、“<”或“=”),用一个化学方程式说明(2)CaC2是离子化合物,各原子均满足8电子稳定结构。写出CaC2的电子式
(3)在常压下,甲醇的沸点(65℃)比甲醛的沸点(﹣19℃)高。主要原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】填空。
(1)铁及其化合物在生活中有广泛应用。Fe3+基态核外电子排布式为_______ 。
(2)实验室用KSCN溶液检验Fe3+。类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是_______ 。
(3)某铁的化合物结构简式如图1所示。

①上述化合物中所含有的非金属元素的电负性由大到小的顺序为_______ (用元素符号表示)。
②上述化合物中氮原子的杂化方式为_______ ,_______ 。
(4)利用新制的Cu(OH)2检验醛基时,生成红色的Cu2O,其晶胞结构如图2所示。
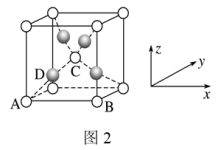
该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);C为( ,
, ,
, )。则D原子的坐标参数为
)。则D原子的坐标参数为_______ ,它代表_______ 原子。
(1)铁及其化合物在生活中有广泛应用。Fe3+基态核外电子排布式为
(2)实验室用KSCN溶液检验Fe3+。类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是
(3)某铁的化合物结构简式如图1所示。

①上述化合物中所含有的非金属元素的电负性由大到小的顺序为
②上述化合物中氮原子的杂化方式为
(4)利用新制的Cu(OH)2检验醛基时,生成红色的Cu2O,其晶胞结构如图2所示。

该晶胞原子坐标参数A为(0,0,0);B为(1,0,0);C为(
 ,
, ,
, )。则D原子的坐标参数为
)。则D原子的坐标参数为
您最近一年使用:0次



