为了减少碳排放,可在催化条件下将 和
和 转化为CO和
转化为CO和 ,其主要反应如下为
,其主要反应如下为 ,该反应历程及能量变化如图1,在发生上述反应的同时,还存在以下反应:
,该反应历程及能量变化如图1,在发生上述反应的同时,还存在以下反应:
积碳反应:
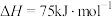
消碳反应:

积碳会影响催化剂的的活性。反应相同时间,测得积碳量与反应温度的关系如图2。

下列说法正确的是
 和
和 转化为CO和
转化为CO和 ,其主要反应如下为
,其主要反应如下为 ,该反应历程及能量变化如图1,在发生上述反应的同时,还存在以下反应:
,该反应历程及能量变化如图1,在发生上述反应的同时,还存在以下反应:积碳反应:

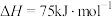
消碳反应:


积碳会影响催化剂的的活性。反应相同时间,测得积碳量与反应温度的关系如图2。

下列说法正确的是
A.消碳反应的 |
B.增大 与 与 的物质的量之比有助于减少积碳 的物质的量之比有助于减少积碳 |
| C.温度高于600℃,积碳反应的速率减慢,积碳量减少 |
D. 和 和 反应的快慢由反应物→过渡态Ⅰ的速率决定 反应的快慢由反应物→过渡态Ⅰ的速率决定 |
更新时间:2022-06-28 07:10:21
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】CH4-CO2催化重整反应为:CH4(g)+ CO2(g)=2CO(g)+2H2(g)。已知:①C(s)+2H2(g)=CH4(g) ΔH=-75 kJ·mol−1②C(s)+O2(g)=CO2(g) ΔH=-394 kJ·mol−1③C(s)+1/2O2(g)=CO(g) ΔH=-111 kJ·mol−1则该催化重整反应的ΔH等于
| A.-580 kJ·mol−1 | B.+247 kJ·mol−1 | C.+208 kJ·mol−1 | D.-430kJ·mol−1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知H+(aq) + OH—(aq) = H2O(l) △H1 = -57.3 kJ·mol—1 CH3COO-(aq) + H2O CH3COOH(aq) + OH-(aq) ΔH2 =aKJ/mol,下列说法正确的是:
CH3COOH(aq) + OH-(aq) ΔH2 =aKJ/mol,下列说法正确的是:
 CH3COOH(aq) + OH-(aq) ΔH2 =aKJ/mol,下列说法正确的是:
CH3COOH(aq) + OH-(aq) ΔH2 =aKJ/mol,下列说法正确的是:| A.a = 57.3 |
| B.a > 57.3 |
| C.0<a<57.3 |
| D.增大c(CH3COO-),a值增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】化学知识在生产和生活中有着重要的应用。下列说法中,错误的是
| A.浓硝酸具有强氧化性,可用铁罐贮运浓硝酸 |
| B.明矾常作为净水剂,双氧水通常可用于作杀菌消毒 |
| C.合成氨工业中通过升高温度可以增大平衡常数K,来提高氨的产率 |
| D.催化剂可以改变反应速率,对平衡移动没有影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某研究小组探究催化剂对CO、NO转化的影响。将含NO和CO的尾气以一定的流速通过两种不同的催化剂进行反应:2NO(g)+2CO(g)  N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
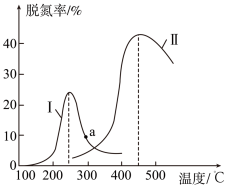
①两种催化剂均能降低活化能,但ΔH不变
②相同条件下,改变压强对脱氮率没有影响
③曲线Ⅱ中的催化剂适用于450 ℃左右脱氮
④曲线Ⅱ中催化剂脱氮率比曲线Ⅰ中的高
⑤ a 点是对应温度下的平衡脱氮率
⑥若低于200 ℃,图中曲线Ⅰ脱氮率随温度升高而变化不大的主要原因是催化剂的活性不高
 N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
N2(g)+2CO2(g),ΔH<0,相同时间内测量逸出气体中NO含量, 从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。以下说法正确的是( )
①两种催化剂均能降低活化能,但ΔH不变
②相同条件下,改变压强对脱氮率没有影响
③曲线Ⅱ中的催化剂适用于450 ℃左右脱氮
④曲线Ⅱ中催化剂脱氮率比曲线Ⅰ中的高
⑤ a 点是对应温度下的平衡脱氮率
⑥若低于200 ℃,图中曲线Ⅰ脱氮率随温度升高而变化不大的主要原因是催化剂的活性不高
| A.①③⑥ | B.①③④ | C.②③④ | D.①③⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】目前应用最广泛的烟气脱硝技术是NH3催化还原氮氧化物,用活化后的V2O5作催化剂的一种反应历程如图所示(图中的虚线表示某种分子间作用力。下列说法正确的是
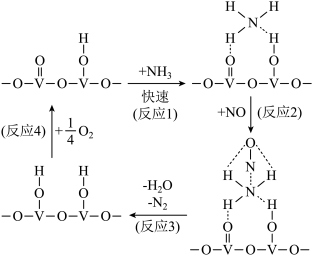

| A.反应1是该过程的决速步骤,活化能最低 |
| B.反应2中,NO通过σ键与中间体结合 |
| C.反应3中涉及非极性键的断裂与生成 |
| D.全过程中,每消耗1 molO2,同时生成6 molH2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
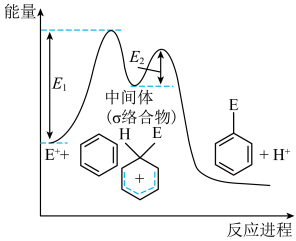
【推荐2】苯的亲电取代反应分两步进行,可表示为 ,苯的亲电取代反应进程和能量的关系如图,下列说法正确的是
,苯的亲电取代反应进程和能量的关系如图,下列说法正确的是
 ,苯的亲电取代反应进程和能量的关系如图,下列说法正确的是
,苯的亲电取代反应进程和能量的关系如图,下列说法正确的是
A.反应Ⅱ的活化能 | B.反应速率:Ⅰ>Ⅱ |
| C.平均能量:中间体>反应物 | D. 与 与 的差值为总反应的焓变 的差值为总反应的焓变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】为减少对环境造成的影响,发电厂试图采用以下方法将废气排放中的CO进行合理利用,以获得重要工业产品。Burns和Dainton研究发现Cl2与CO合成COCl2的反应机理如下:
①Cl2(g) 2Cl·(g) 快;
2Cl·(g) 快;
②CO(g)+Cl·(g) COCl·(g) 快;
COCl·(g) 快;
③COCl·(g)+Cl2(g) COCl2(g)+Cl·(g) 慢。
COCl2(g)+Cl·(g) 慢。
反应②的速率方程 c(CO)×c(Cl·),
c(CO)×c(Cl·), c(COCl·),
c(COCl·),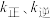 是速率常数。
是速率常数。
下列说法错误 的是
①Cl2(g)
 2Cl·(g) 快;
2Cl·(g) 快;②CO(g)+Cl·(g)
 COCl·(g) 快;
COCl·(g) 快;③COCl·(g)+Cl2(g)
 COCl2(g)+Cl·(g) 慢。
COCl2(g)+Cl·(g) 慢。反应②的速率方程
 c(CO)×c(Cl·),
c(CO)×c(Cl·), c(COCl·),
c(COCl·),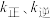 是速率常数。
是速率常数。下列说法
A.反应②的平衡常数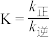 |
| B.反应①的活化能小于反应③的活化能 |
| C.要提高合成COCl2的速率,关键是提高反应③的速率 |
| D.使用合适的催化剂可以增大该反应体系中COCl2(g)的体积分数 |
您最近一年使用:0次

 和6.0mol
和6.0mol
 ,
,
 内,
内,


