回答下列问题:
(1) 时,
时, 的
的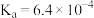 ,则此温度下
,则此温度下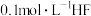 溶液的
溶液的 为
为_______  。
。
(2) 时,
时,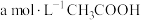 溶液的
溶液的 ,用含a和b的代数式表示
,用含a和b的代数式表示 的电离平衡常数
的电离平衡常数
_______ 。
(3)硒酸( )在水溶液中的电离如下:
)在水溶液中的电离如下: 。向
。向 溶液中滴加少量氨水,该反应的离子方程式为
溶液中滴加少量氨水,该反应的离子方程式为_______ 。
(4)已知 时,
时,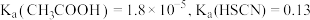 。现在该温度下将
。现在该温度下将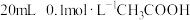 溶液和
溶液和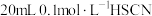 溶液分别与
溶液分别与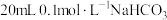 溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示,反应初始阶段,两种溶液产生
溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示,反应初始阶段,两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是_______ 。

(5)已知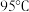 时的
时的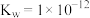 ,将
,将 的
的 溶液与
溶液与 的
的 溶液混合,若所得
溶液混合,若所得 ,则
,则 溶液与
溶液与 溶液的体积比为
溶液的体积比为_______ 。
(6)常温下,由水电离出的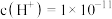 ,则该溶液的
,则该溶液的 为
为_______ 。
(1)
 时,
时, 的
的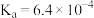 ,则此温度下
,则此温度下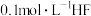 溶液的
溶液的 为
为 。
。(2)
 时,
时,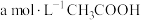 溶液的
溶液的 ,用含a和b的代数式表示
,用含a和b的代数式表示 的电离平衡常数
的电离平衡常数
(3)硒酸(
 )在水溶液中的电离如下:
)在水溶液中的电离如下: 。向
。向 溶液中滴加少量氨水,该反应的离子方程式为
溶液中滴加少量氨水,该反应的离子方程式为(4)已知
 时,
时,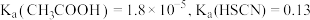 。现在该温度下将
。现在该温度下将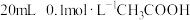 溶液和
溶液和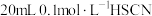 溶液分别与
溶液分别与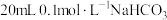 溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示,反应初始阶段,两种溶液产生
溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示,反应初始阶段,两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是
(5)已知
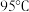 时的
时的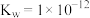 ,将
,将 的
的 溶液与
溶液与 的
的 溶液混合,若所得
溶液混合,若所得 ,则
,则 溶液与
溶液与 溶液的体积比为
溶液的体积比为(6)常温下,由水电离出的
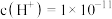 ,则该溶液的
,则该溶液的 为
为
更新时间:2022/06/27 09:46:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】已知水溶液中 和
和 的关系如图所示:
的关系如图所示:
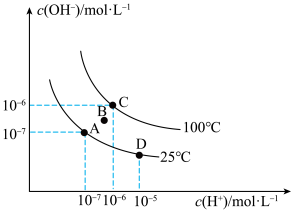
(1)图中B点水的离子积常数___________  (填>、=或<)。
(填>、=或<)。
(2)从A点到D点,可采取的措施是___________ 。
a.升温b.加入少量盐酸c.降温d.加入少量NaOH
(3)100℃时,pH=2的盐酸中水电离产生的H+浓度为___________  。
。
(4)25℃时,将pH=12的NaOH溶液与pH=3的 溶液混合,若所得混合溶液pH=7,则NaOH溶液与
溶液混合,若所得混合溶液pH=7,则NaOH溶液与 溶液的体积比为
溶液的体积比为___________ 。
 和
和 的关系如图所示:
的关系如图所示:
(1)图中B点水的离子积常数
 (填>、=或<)。
(填>、=或<)。(2)从A点到D点,可采取的措施是
a.升温b.加入少量盐酸c.降温d.加入少量NaOH
(3)100℃时,pH=2的盐酸中水电离产生的H+浓度为
 。
。(4)25℃时,将pH=12的NaOH溶液与pH=3的
 溶液混合,若所得混合溶液pH=7,则NaOH溶液与
溶液混合,若所得混合溶液pH=7,则NaOH溶液与 溶液的体积比为
溶液的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,用酚酞作指示剂,用0.10mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10mol·L-1的 CH3COOH溶液和HCN溶液所得滴定曲线如图。
(已知:CH3COOH、 HCN的电离平衡常数分别为1.75×10-5、6.4×10-10)
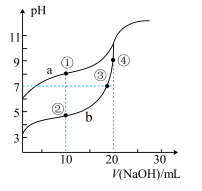
(1)图__ (a或b)是NaOH溶液滴定HCN溶液的pH变化的曲线,判断的理由是__ 。
(2)点③所示溶液中所含离子浓度的从大到小的顺序:__ 。
(3)点①和点② 所示溶液中:c(CH3COO-)-c(CN-)__ c(HCN)-c(CH3COOH)(填“>、<或=”)
(4)点②③④所示的溶液中水的电离程度由大到小的顺序是:__ 。
(已知:CH3COOH、 HCN的电离平衡常数分别为1.75×10-5、6.4×10-10)

(1)图
(2)点③所示溶液中所含离子浓度的从大到小的顺序:
(3)点①和点② 所示溶液中:c(CH3COO-)-c(CN-)
(4)点②③④所示的溶液中水的电离程度由大到小的顺序是:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】 常作食品加工中的食品添加剂,用于焙烤食品;
常作食品加工中的食品添加剂,用于焙烤食品; 在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1) 可作净水剂,其原理是
可作净水剂,其原理是_______ (用离子方程式说明)。
(2)配制 溶液时,通常需加入适量的
溶液时,通常需加入适量的_______ ,减小其水解程度。
(3)相同条件下, 溶液中的
溶液中的
_______ (填“等于”“大于”或“小于”) 溶液中的
溶液中的 。
。
(4)下列图像为0.1mol/L的几种电解质溶液的pH随温度变化的曲线。

其中符合 溶液的pH随温度变化的曲线是
溶液的pH随温度变化的曲线是_______ (填罗马数字), 溶液的pH随温度变化的原因是
溶液的pH随温度变化的原因是_______ 。
(5)室温时,向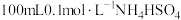 溶液中滴加
溶液中滴加 溶液,溶液pH与加入
溶液,溶液pH与加入 溶液体积的关系曲线如图所示。
溶液体积的关系曲线如图所示。

①试分析图中a、b、c、d四个点,水的电离程度最大的是_______ 点。
②在b点,溶液中各离子浓度由大到小的排列顺序是_______ 。
③由b到c发生反应的离子方程式为_______ 。
 常作食品加工中的食品添加剂,用于焙烤食品;
常作食品加工中的食品添加剂,用于焙烤食品; 在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
在分析试剂、医药、电子工业中用途广泛。请回答下列问题:(1)
 可作净水剂,其原理是
可作净水剂,其原理是(2)配制
 溶液时,通常需加入适量的
溶液时,通常需加入适量的(3)相同条件下,
 溶液中的
溶液中的
 溶液中的
溶液中的 。
。(4)下列图像为0.1mol/L的几种电解质溶液的pH随温度变化的曲线。

其中符合
 溶液的pH随温度变化的曲线是
溶液的pH随温度变化的曲线是 溶液的pH随温度变化的原因是
溶液的pH随温度变化的原因是(5)室温时,向
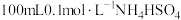 溶液中滴加
溶液中滴加 溶液,溶液pH与加入
溶液,溶液pH与加入 溶液体积的关系曲线如图所示。
溶液体积的关系曲线如图所示。
①试分析图中a、b、c、d四个点,水的电离程度最大的是
②在b点,溶液中各离子浓度由大到小的排列顺序是
③由b到c发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.计算下列溶液的pH值(25 ℃),(请写出计算过程)将20mL0.01 mol·L-1 KOH溶液与30mL0.005mol·L-1H2SO4溶液混合并加水至100ml.
(1)求KOH溶液的pH值_______________ ;
(2)求H2SO4溶液的pH值_______________ ;
(3)求混合液的pH值_______________ 。
II.将10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH(酸)与强碱的pH(碱)之间应满足的关系__________ 。
(1)求KOH溶液的pH值
(2)求H2SO4溶液的pH值
(3)求混合液的pH值
II.将10体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的pH(酸)与强碱的pH(碱)之间应满足的关系
您最近一年使用:0次
填空题
|
适中
(0.65)
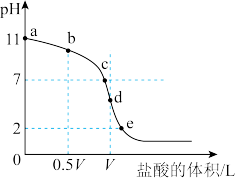
【推荐2】在25℃时,向浓度为0.1mol⋅L-1、体积为1.0L的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而降低的滴定曲线如图所示,d点两种溶液恰好完全反应。请根据图中信息回答下列问题:
I.
(1)在25℃时, 的电离常数K=
的电离常数K=___________ 。
(2)比较a、b、c、d四点时的溶液中,水电离程度由大到小的顺序是___________ 。
II.在某温度下的水溶液中,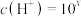 mol⋅L
mol⋅L ,
, mol⋅L-1。x与y的关系如图所示,回答下列问题:
mol⋅L-1。x与y的关系如图所示,回答下列问题:
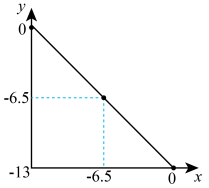
(3)水的离子积为___________ ;pH=7的溶液呈___________ 性(填“酸”、“中”、“碱”)
(4)若测得某溶液中,水电离出来的 mol∙L-1,且溶液为强酸溶液,则该溶液的pH=
mol∙L-1,且溶液为强酸溶液,则该溶液的pH=___________ 。

I.
(1)在25℃时,
 的电离常数K=
的电离常数K=(2)比较a、b、c、d四点时的溶液中,水电离程度由大到小的顺序是
II.在某温度下的水溶液中,
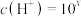 mol⋅L
mol⋅L ,
, mol⋅L-1。x与y的关系如图所示,回答下列问题:
mol⋅L-1。x与y的关系如图所示,回答下列问题:
(3)水的离子积为
(4)若测得某溶液中,水电离出来的
 mol∙L-1,且溶液为强酸溶液,则该溶液的pH=
mol∙L-1,且溶液为强酸溶液,则该溶液的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求填写下列相关内容:
(1)在常温下,将体积为VaL、pH为a的稀硫酸和体积为VbL、pH为b的烧碱溶液混合,所得混合溶液为中性.如果a+b=15,则Va:Vb=_________
某温度时,水的离子积常数Kw=1×10-13.在此温度下,将pH=a的硫酸溶液VaL与pH=b的NaOH溶液VbL混合,若所得混合液为中性,如果a+b=12,则Va:Vb=_________
(2)中和相同体积,相同pH的Ba(OH)2、NH3•H2O、NaOH三种稀溶液,所用相同浓度的盐酸的体积分别为V1、V2、V3,则三者按由大到小的顺序为_________ (用“V1、V2、V3”和“>、<、=”表示
(3)为抑制水解,实验室中配制FeCl3溶液时常加入___________ (填名称)。将FeCl3溶液和NaHCO3溶液混合,产生红褐色沉淀和无色气体,反应的离子方程式为__________________________________ 。
(4)25 ℃时,pH均为5的醋酸和硫酸铝两种溶液中,由水电离出的c(H+)之比为________________ 。
(1)在常温下,将体积为VaL、pH为a的稀硫酸和体积为VbL、pH为b的烧碱溶液混合,所得混合溶液为中性.如果a+b=15,则Va:Vb=
某温度时,水的离子积常数Kw=1×10-13.在此温度下,将pH=a的硫酸溶液VaL与pH=b的NaOH溶液VbL混合,若所得混合液为中性,如果a+b=12,则Va:Vb=
(2)中和相同体积,相同pH的Ba(OH)2、NH3•H2O、NaOH三种稀溶液,所用相同浓度的盐酸的体积分别为V1、V2、V3,则三者按由大到小的顺序为
(3)为抑制水解,实验室中配制FeCl3溶液时常加入
(4)25 ℃时,pH均为5的醋酸和硫酸铝两种溶液中,由水电离出的c(H+)之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】碳氢化合物是重要的能源物质。
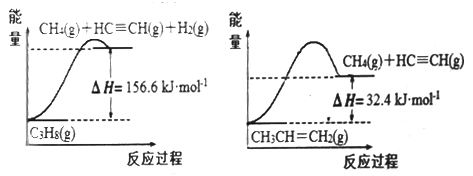
(1)丙烷脱氢可得丙烯。已知:有关化学反应的能量变化如下图所示。
则相同条件下,反应C3H8(g) CH3CH=CH2(g)+H2(g)的△H=
CH3CH=CH2(g)+H2(g)的△H=___ kJ·mol-1。
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池正极反应式为________________ 。
(3)常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3) = 1.5×10-5mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3 HCO3-+H+的平衡常数K1=
HCO3-+H+的平衡常数K1=__________ 。(结果保留2位有效数字)(已知10-5.60=2.5×10-6)
(4)用氨气制取尿素的反应为:2NH3(g)+CO2(g)==CO(NH2)2(l)+H2O(g)△H<0
某温度下,向容积为100L的密闭容器中通入4molNH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%。
①理论上生产尿素的条件是______ 。(填选项编号)
A.高温、高压 B.高温、低压 C.低温、低压 D.低温、高压
②下列描述能说明反应达到平衡状态的是_____________ 。
A.反应混合物中CO2和H2O的物质的量之比为1:2
B.混合气体的总质量不随时间的变化而变化
C.单位时间内消耗2a molNH3,同时生成a molH2O
D.保持温度和容积不变,混合气体的压强不随时间的变化而变化
③该温度下此反应平衡常数K的值为____________ 。
④图中的曲线I表示该反应在前25s内的反应进程中的NH3浓度变化.。在0~25s内该反应的平均反应速率v(CO2)=___________ 。
保持其它条件不变,只改变一种条件,图象变成II,则改变的条件可能是_______________ 。
(1)丙烷脱氢可得丙烯。已知:有关化学反应的能量变化如下图所示。
则相同条件下,反应C3H8(g)
 CH3CH=CH2(g)+H2(g)的△H=
CH3CH=CH2(g)+H2(g)的△H=(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐。电池正极反应式为
(3)常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3) = 1.5×10-5mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3
 HCO3-+H+的平衡常数K1=
HCO3-+H+的平衡常数K1=(4)用氨气制取尿素的反应为:2NH3(g)+CO2(g)==CO(NH2)2(l)+H2O(g)△H<0
某温度下,向容积为100L的密闭容器中通入4molNH3和2molCO2,该反应进行到40s时达到平衡,此时CO2的转化率为50%。
①理论上生产尿素的条件是
A.高温、高压 B.高温、低压 C.低温、低压 D.低温、高压
②下列描述能说明反应达到平衡状态的是
A.反应混合物中CO2和H2O的物质的量之比为1:2
B.混合气体的总质量不随时间的变化而变化
C.单位时间内消耗2a molNH3,同时生成a molH2O
D.保持温度和容积不变,混合气体的压强不随时间的变化而变化
③该温度下此反应平衡常数K的值为
④图中的曲线I表示该反应在前25s内的反应进程中的NH3浓度变化.。在0~25s内该反应的平均反应速率v(CO2)=
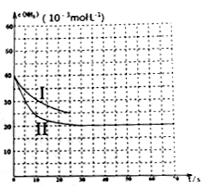
保持其它条件不变,只改变一种条件,图象变成II,则改变的条件可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】溶液中的化学反应大多是离子反应。根据要求回答下列问题:
(1)Na2CO3溶液显碱性的原因,用离子反应方程式表示_____________________________ ;CuSO4溶液呈酸性的原因,用离子反应方程式表示:___________________________ 。
(2)25 ℃时,pH为9的CH3COONa溶液中c(OH-)=________ 。
(3)25 ℃时,将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH )=c(Cl-),则溶液显
)=c(Cl-),则溶液显________ (填“酸”“碱”或“中”)性。用含a的代数式表示NH3·H2O的电离常数Kb=___________ 。
(1)Na2CO3溶液显碱性的原因,用离子反应方程式表示
(2)25 ℃时,pH为9的CH3COONa溶液中c(OH-)=
(3)25 ℃时,将a mol·L-1氨水与0.01 mol·L-1盐酸等体积混合,反应平衡时溶液中c(NH
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显
您最近一年使用:0次

 Cu2+(aq)+Ag2S(s)为例,推导沉淀转化的平衡常数K
Cu2+(aq)+Ag2S(s)为例,推导沉淀转化的平衡常数K

