科学、安全、有效和合理地开发自然资源,对生产、生活有重要价值。请回答下列问题:
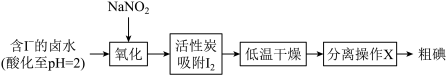
(1)活性炭吸附法是工业提取碘的方法之一,其流程如下:
II.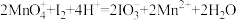
①氧化过程的离子方程式为_______ 。
②根据I2的特性,分离操作X应为_______ 、冷却结晶。
③酸性KMnO4是常用的强氧化剂,但该方法中却选择了价格较高的NaNO2,原因是_______ 。
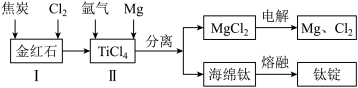
(2)以金红石(主要成分为TiO2)为原料,制取Ti的工艺流程如图所示:_______ 。
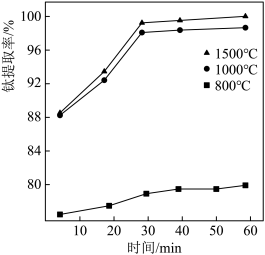
②II中钛的提取率在不同温度下随时间变化的曲线如图所示,则反应适宜的温度为_______ ℃。_______ 。
④海绵钛除杂时得到的MgCl2可以循环使用,在上述工艺流程中可循环使用的物质还有_______ (填化学式)。
(1)活性炭吸附法是工业提取碘的方法之一,其流程如下:
II.
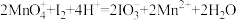
①氧化过程的离子方程式为
②根据I2的特性,分离操作X应为
③酸性KMnO4是常用的强氧化剂,但该方法中却选择了价格较高的NaNO2,原因是
(2)以金红石(主要成分为TiO2)为原料,制取Ti的工艺流程如图所示:
②II中钛的提取率在不同温度下随时间变化的曲线如图所示,则反应适宜的温度为
④海绵钛除杂时得到的MgCl2可以循环使用,在上述工艺流程中可循环使用的物质还有
21-22高一下·辽宁锦州·期末 查看更多[6]
辽宁省锦州市2021-2022学年高一下学期期末考试化学试卷辽宁省沈阳市新民市第一高级中学2021-2022学年高一下学期期末考试化学试题黑龙江省齐齐哈尔市八校联考2022-2023学年高一下学期期末考试化学试题安徽省六安第一中学2022-2023学年高一下学期期末考试化学试题(已下线)猜想03 气体的制取、无机实验探究、无机综合应用(考题猜想)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)名校期末好题汇编-化学与可持续发展(非选择题)
更新时间:2022-07-12 15:14:30
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】氯气是一种重要的化工原料,它的发现和研究经过了化学家们的不懈努力。
(1)舍勒发现氯气的方法是实验室制取氯气(如图)的主要方法之一。
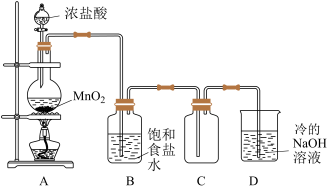
①盛装浓盐酸的仪器名称为_____ ;装置A中发生反应的化学方程式为___________ 。
②装置B中饱和食盐水的作用是___________ 。
③装置D中发生反应的离子方程式为___________ 。
(2)含氧化合物亚氯酸钠( )是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
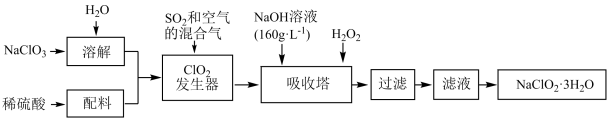
已知:纯 易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全。
易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全。
① 发生器中发生反应的离子方程式为
发生器中发生反应的离子方程式为_____ ,在发生器中鼓入空气的作用可能是_____ 。
②吸收塔中为防止 被还原成NaCl,可用还原性适中的
被还原成NaCl,可用还原性适中的 作还原剂,写出吸收塔中发生反应的化学方程式:
作还原剂,写出吸收塔中发生反应的化学方程式:_____ ;除 外还可以选择的还原剂是
外还可以选择的还原剂是_____ (填字母)。
A. B.
B. C.
C.
(1)舍勒发现氯气的方法是实验室制取氯气(如图)的主要方法之一。

①盛装浓盐酸的仪器名称为
②装置B中饱和食盐水的作用是
③装置D中发生反应的离子方程式为
(2)含氧化合物亚氯酸钠(
 )是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
已知:纯
 易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全。
易分解爆炸,一般用稀有气体或空气稀释到10%以下较安全。①
 发生器中发生反应的离子方程式为
发生器中发生反应的离子方程式为②吸收塔中为防止
 被还原成NaCl,可用还原性适中的
被还原成NaCl,可用还原性适中的 作还原剂,写出吸收塔中发生反应的化学方程式:
作还原剂,写出吸收塔中发生反应的化学方程式: 外还可以选择的还原剂是
外还可以选择的还原剂是A.
 B.
B. C.
C.
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】肼(N2H4)是一种可燃性液体,可用作火箭燃料。
(1)N2H4分子中氮原子均达到8电子稳定结构,写出N2H4的电子式___ ;一种与肼电子数相等的绿色氧化剂,当它与肼反应时生成两种无污染物质,该反应的化学方程式为___ 。
(2)以Cl2、NaOH和尿素[(NH2)2CO]为原料可制备水合肼(N2H4·H2O),其主要实验流程如图:
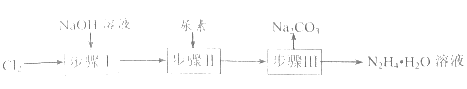
①步骤I制备NaClO溶液,写出该反应的离子方程式___ ;反应中放出大量的热,若温度超过40℃,Cl2会与NaOH溶液反应生成NaClO3。为防止NaClO3的生成,实验中可用冰水浴控制温度,还可采取的措施是___ 。
②步骤II合成N2H4·H2O,写出该反应的化学方程式___ 。
③步骤III分离得到N2H4·H2O溶液样品。为测定所得样品中N2H4·H2O的含量,采用以下实验步骤。
I.取5.00mL样品配制成250mL溶液,取该溶液10.00mL于锥形瓶内,加20mL蒸馏水、1mL1mol·L-1硫酸、NaHCO3约1g、15.00mL0.1000mol·L-1碘标准溶液,振荡。
II.向锥形瓶内加入适量___ 作指示剂,用0.05000mol·L-1的Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液12.00mL。
已知:N2H4·H2O+2I2+H2SO4+6NaHCO3=N2↑+6CO2↑+Na2SO4+4NaI+7H2O。
I2+2Na2S2O3=Na2S4O6+2NaI
计算试样中N2H4·H2O的物质的量浓度___ (写出计算过程)。
(1)N2H4分子中氮原子均达到8电子稳定结构,写出N2H4的电子式
(2)以Cl2、NaOH和尿素[(NH2)2CO]为原料可制备水合肼(N2H4·H2O),其主要实验流程如图:

①步骤I制备NaClO溶液,写出该反应的离子方程式
②步骤II合成N2H4·H2O,写出该反应的化学方程式
③步骤III分离得到N2H4·H2O溶液样品。为测定所得样品中N2H4·H2O的含量,采用以下实验步骤。
I.取5.00mL样品配制成250mL溶液,取该溶液10.00mL于锥形瓶内,加20mL蒸馏水、1mL1mol·L-1硫酸、NaHCO3约1g、15.00mL0.1000mol·L-1碘标准溶液,振荡。
II.向锥形瓶内加入适量
已知:N2H4·H2O+2I2+H2SO4+6NaHCO3=N2↑+6CO2↑+Na2SO4+4NaI+7H2O。
I2+2Na2S2O3=Na2S4O6+2NaI
计算试样中N2H4·H2O的物质的量浓度
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】铋为第五周期VA族元素,利用湿法治金从辉铋矿(含Bi2S3、Bi、Bi2O3等)提取金属铋的工艺流程如下图所示:
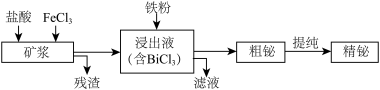
已知:BiCl3水解的离子方程式为:BiCl3+H2O BiOCl+2H++2Cl-。
BiOCl+2H++2Cl-。
(1)矿浆浸出时加入盐酸的作用是___________ 。
(2)浸出时,Bi溶于FeCl3溶液的化学方程式为___________ 。
(3)残渣中含有一种单质,该单质是___________ 。
(4)滤液的主要溶质是(化学式)___________ ,该物质可在工艺中转化为循环利用的原料,转化的反应方程式为___________ 。
(5)精辉铋矿中含有Ag2S,被氧化溶解后不会进入浸出液,银元素以___________ (填化学式)进入残渣中。
(6)粗铋提纯时,粗铋应放在___________ 极,阴极的电极反应式___________ 。

已知:BiCl3水解的离子方程式为:BiCl3+H2O
 BiOCl+2H++2Cl-。
BiOCl+2H++2Cl-。(1)矿浆浸出时加入盐酸的作用是
(2)浸出时,Bi溶于FeCl3溶液的化学方程式为
(3)残渣中含有一种单质,该单质是
(4)滤液的主要溶质是(化学式)
(5)精辉铋矿中含有Ag2S,被氧化溶解后不会进入浸出液,银元素以
(6)粗铋提纯时,粗铋应放在
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】氯化亚铜是一种重要的化工产品,广泛用于颜料、电镀和有机合成等方面。它不溶于H2SO4和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解且被氧化成绿色的碱式氯化铜Cu(OH)Cl]。以海绵铜(主要成分是Cu,还含少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺流程如下:
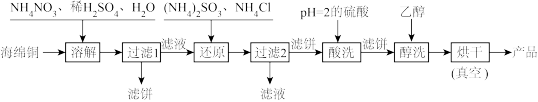
回答下列问题: .
(1)为了提高“溶解”速率,工业生产中宜采用的措施有_______________ (答两条即可)。.
(2)写出“溶解”过程中发生氧化还原反应的离子方程式:___________________ 。
(3)“过滤2”所得滤液经蒸发浓缩、冷却结晶过滤等操作获得一种化学肥料,它的主要成分是_________________ (填化学式)。
(4)工业生产中,用pH=2的硫酸洗涤“产品”,其目的是______________________ 。
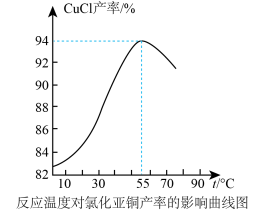
(5)氯化亚铜产率与温度的关系如图1所示。据图分析,流程化生产氯化亚铜的过程中,温度过低会影响CuCl产率的原因是_______________________ 。

回答下列问题: .
(1)为了提高“溶解”速率,工业生产中宜采用的措施有
(2)写出“溶解”过程中发生氧化还原反应的离子方程式:
(3)“过滤2”所得滤液经蒸发浓缩、冷却结晶过滤等操作获得一种化学肥料,它的主要成分是
(4)工业生产中,用pH=2的硫酸洗涤“产品”,其目的是
(5)氯化亚铜产率与温度的关系如图1所示。据图分析,流程化生产氯化亚铜的过程中,温度过低会影响CuCl产率的原因是


您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
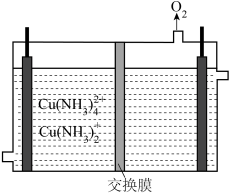
【推荐2】氯碱工业上利用电解精制饱和食盐水的方法制取氢气、氯气、烧碱和氯的含氧酸盐等一系列化工产品,图-1所示是离子交换膜法电解饱和食盐水的示意图。
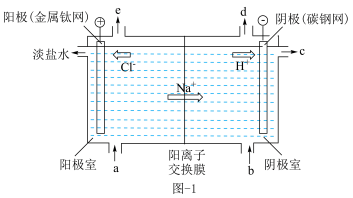
(1)图-1中b处加入的原料是___________ (填化学式)的稀溶液,e处出来的气体为___________ 。
(2)如果没有阳离子交换膜,则可以得到一种家用消毒液和氢气,写出装置中发生该反应的化学方程式___________ 。
(3)去除泥沙后的粗盐溶液中含有Mg2+、Ca2+和SO 等杂质离子,需要依次加入NaOH溶液、BaCl2溶液、Na2CO3溶液、HCl溶液等试剂来获取精制食盐水。
等杂质离子,需要依次加入NaOH溶液、BaCl2溶液、Na2CO3溶液、HCl溶液等试剂来获取精制食盐水。
①BaCl2溶液一定要在Na2CO3溶液之前添加,其理由用离子方程式表示为___________ 。
②加HCl溶液的作用为___________ 。
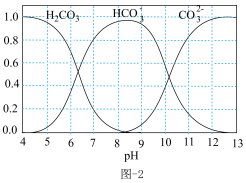
③已知碳酸溶液中含碳微粒的物质的量分数随pH变化如图-2所示,则最后一步用HCl溶液调节pH=7是否可行___________ (填“可行”或“不可行”),理由是___________ 。
(4)判断杂质离子是否除尽是粗盐精制的关键环节,当c(Mg2+)≤10-5mol·L-1时,可认为Mg2+被除尽。(Ksp[Mg(OH)2]=5.6×10-12)。常温下当加入NaOH使溶液pH=11时,c(Mg2+)=___________ mol·L−1,此时溶液中Mg2+___________ (填“已除尽”或“未除尽”)。

(1)图-1中b处加入的原料是
(2)如果没有阳离子交换膜,则可以得到一种家用消毒液和氢气,写出装置中发生该反应的化学方程式
(3)去除泥沙后的粗盐溶液中含有Mg2+、Ca2+和SO
 等杂质离子,需要依次加入NaOH溶液、BaCl2溶液、Na2CO3溶液、HCl溶液等试剂来获取精制食盐水。
等杂质离子,需要依次加入NaOH溶液、BaCl2溶液、Na2CO3溶液、HCl溶液等试剂来获取精制食盐水。①BaCl2溶液一定要在Na2CO3溶液之前添加,其理由用离子方程式表示为
②加HCl溶液的作用为
③已知碳酸溶液中含碳微粒的物质的量分数随pH变化如图-2所示,则最后一步用HCl溶液调节pH=7是否可行

(4)判断杂质离子是否除尽是粗盐精制的关键环节,当c(Mg2+)≤10-5mol·L-1时,可认为Mg2+被除尽。(Ksp[Mg(OH)2]=5.6×10-12)。常温下当加入NaOH使溶液pH=11时,c(Mg2+)=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】用含钴废料(主要成分为CoCO3,还含有少量NiCO3与铁屑)制备CoCl2•6H2O的工艺流程如图。

①已知除镍过程中溶液pH对钴的回收率及Ni2+含量的影响如图所示。

②一部分金属阳离子在实验条件下开始沉淀和完全沉淀的pH如表所示。
回答下列问题:
(1)酸浸后溶液中的阳离子为:Co2+,Ni2+和___
(2)除镍时,应调节溶液pH=___ ,此时Ni2+是否形成Ni(OH)2沉淀?___ (填“是”或“否”)。若pH过小,则产品纯度会___ (填“升高”、“降低”或“不变”)。
(3)酸溶时,当调节pH=8时,溶液中n(Fe3+):n(Co2+)=___ 。
已知Ksp[Co(OH)2]=2.0×10-16,Ksp[Fe(OH)3]=4.0×10-38。
(4)除铁时先向溶液中加入30%的H2O2,充分反应后再向溶液中加入CoCO3,调节溶液pH范围为___ ,使Fe3+完全转化为Fe(OH)3沉淀,最后过滤得到CoCl2溶液。

①已知除镍过程中溶液pH对钴的回收率及Ni2+含量的影响如图所示。

②一部分金属阳离子在实验条件下开始沉淀和完全沉淀的pH如表所示。
| 金属阳离子 | 开始沉淀pH | 完全沉淀pH |
| Fe3+ | 1.5 | 4.0 |
| Fe2+ | 7.5 | 9.7 |
| Co2+ | 6.6 | 9.4 |
| Ni2+ | 7.7 | 9.5 |
回答下列问题:
(1)酸浸后溶液中的阳离子为:Co2+,Ni2+和
(2)除镍时,应调节溶液pH=
(3)酸溶时,当调节pH=8时,溶液中n(Fe3+):n(Co2+)=
已知Ksp[Co(OH)2]=2.0×10-16,Ksp[Fe(OH)3]=4.0×10-38。
(4)除铁时先向溶液中加入30%的H2O2,充分反应后再向溶液中加入CoCO3,调节溶液pH范围为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】焦亚硫酸钠 ( Na2S2O5)是一种食品添加剂,实验室用如图所示装置制备Na2S2O5,实验步骤如下:
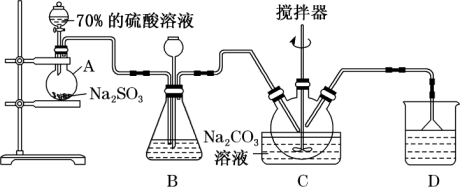
(1)原料气(SO2)的制备
①装置A中盛装药品之前需要进行的操作是______ ;装置B的作用之一是观察SO2的生成速率,其中的试剂最好选用______ (填字母)。
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和Na2CO3溶液
②B瓶中长颈漏斗的作用______ 。
③D 中盛放溶液的溶质的化学名称是______ 。
(2)焦亚硫酸钠(Na2S2O5) 的制备
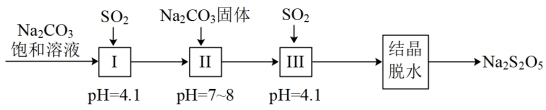
① Na2S2O5溶于水且与水能反应,所得溶液显酸性,其原因是______ ,步骤III中测定溶液的pH的方法是______ ;pH>4.1时,则产品中会有副产物,其化学式是______ 。
②结晶脱水生成产品的化学方程式为______ 。

(1)原料气(SO2)的制备
①装置A中盛装药品之前需要进行的操作是
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和Na2CO3溶液
②B瓶中长颈漏斗的作用
③D 中盛放溶液的溶质的化学名称是
(2)焦亚硫酸钠(Na2S2O5) 的制备

① Na2S2O5溶于水且与水能反应,所得溶液显酸性,其原因是
②结晶脱水生成产品的化学方程式为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】亚氯酸钠(NaClO2)是重要漂白剂。探究小组开展如下实验,回答下列问题:
实验Ⅰ:制取NaClO2晶体按图装置进行制取。
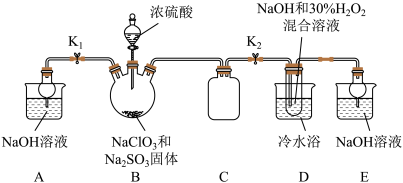
已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,38-60℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
(1)装置C的作用是___________________ 。
(2)B中产生ClO2的化学方程式_________________________ 。
(3)装置D中反应生成NaClO2的化学方程式为____________ 。反应后的溶液中阴离子除了ClO2-、ClO3-、Cl-、ClO-、OH—外还可能含有的一种阴离子是_______ ,检验该离子的方法是____________ 。
(4)请补充从装置D反应后的溶液中获得NaClO2晶体的操作步骤。
①减压,55℃蒸发结晶;②______________ ;③______________ ;④______________ ;得到成品。
(5)如果撤去D中的冷水浴,可能导致产品中混有的杂质是______________ 。
实验Ⅰ:制取NaClO2晶体按图装置进行制取。

已知:NaClO2饱和溶液在低于38℃时析出NaClO2•3H2O,38-60℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
(1)装置C的作用是
(2)B中产生ClO2的化学方程式
(3)装置D中反应生成NaClO2的化学方程式为
(4)请补充从装置D反应后的溶液中获得NaClO2晶体的操作步骤。
①减压,55℃蒸发结晶;②
(5)如果撤去D中的冷水浴,可能导致产品中混有的杂质是
您最近一年使用:0次
【推荐3】我国出口球状氯化镁融雪剂时,对产品色度(白度)要求很高,因此研究脱色及显色离子的去除有现实意义。以水氯镁石为原料生产符合白度要求的融雪剂的流程如下。
已知:①水氯镁石的主要成分是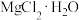 ,还含有少量有色有机物、可溶性
,还含有少量有色有机物、可溶性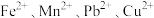 等杂质离子及少量不溶物。
等杂质离子及少量不溶物。
I.去除泥沙及脱除有机物颜色
水氯镁石
 饱和溶液
饱和溶液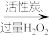 脱色后的
脱色后的 饱和溶液
饱和溶液
(1)操作1的名称是_______ 。
(2)活性炭的作用是_______ 。
(3)部分有机物可与 反应脱氢,在该反应中,
反应脱氢,在该反应中, 体现的性质是
体现的性质是_______ 。
(4)其它条件都不变的情况下,得到温度对脱色率的影响如图所示。 后,随温度升高,脱色率下降的原因是
后,随温度升高,脱色率下降的原因是_______ 。

II.去除显色离子
向脱色处理后的氯化镁溶液中加入氨水反应30分钟,再将溶液升温至 保持30分钟,恢复至室温,最后加入适量的
保持30分钟,恢复至室温,最后加入适量的 溶液反应一段时间,过滤得到氯化镁精制溶液。
溶液反应一段时间,过滤得到氯化镁精制溶液。
(5)过滤得到的滤渣中含有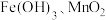 、
、_______ 。
①将横线补充完整_______ 。
②将生成 的离子方程式补充完整:
的离子方程式补充完整:_______ 、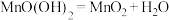
(6)将溶液升温至 的目的是
的目的是_______ 。
III.制备产品
氯化镁精制溶液
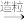 球状氯化镁融雪剂
球状氯化镁融雪剂
(7)操作2是_______ 。
已知:①水氯镁石的主要成分是
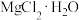 ,还含有少量有色有机物、可溶性
,还含有少量有色有机物、可溶性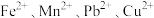 等杂质离子及少量不溶物。
等杂质离子及少量不溶物。| 物质 |  |  |
 | 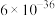 | 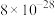 |
水氯镁石

 饱和溶液
饱和溶液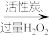 脱色后的
脱色后的 饱和溶液
饱和溶液(1)操作1的名称是
(2)活性炭的作用是
(3)部分有机物可与
 反应脱氢,在该反应中,
反应脱氢,在该反应中, 体现的性质是
体现的性质是(4)其它条件都不变的情况下,得到温度对脱色率的影响如图所示。
 后,随温度升高,脱色率下降的原因是
后,随温度升高,脱色率下降的原因是
II.去除显色离子
向脱色处理后的氯化镁溶液中加入氨水反应30分钟,再将溶液升温至
 保持30分钟,恢复至室温,最后加入适量的
保持30分钟,恢复至室温,最后加入适量的 溶液反应一段时间,过滤得到氯化镁精制溶液。
溶液反应一段时间,过滤得到氯化镁精制溶液。(5)过滤得到的滤渣中含有
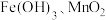 、
、①将横线补充完整
②将生成
 的离子方程式补充完整:
的离子方程式补充完整: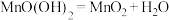
(6)将溶液升温至
 的目的是
的目的是III.制备产品
氯化镁精制溶液

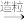 球状氯化镁融雪剂
球状氯化镁融雪剂(7)操作2是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下面的工艺流程生产单质碘:
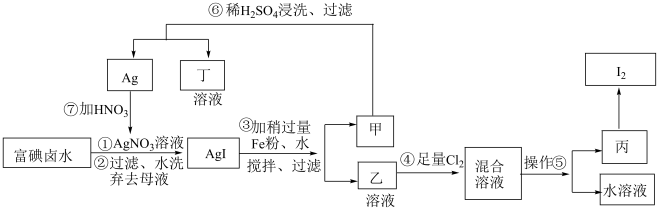
(1)步骤③加Fe粉的目的是____________________________________ 。
(2)写出步骤④中反应的离子方程式_________________________________ 。
(3)上述生产流程中,可以循环利用的副产物是___________ 。
(4)操作⑤的名称是_______________ ,选用的试剂是__________ 。

(1)步骤③加Fe粉的目的是
(2)写出步骤④中反应的离子方程式
(3)上述生产流程中,可以循环利用的副产物是
(4)操作⑤的名称是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】锗是一种重要的半导体材料,其有机化合物在治疗癌症方面有着独特的功效。下图为工业上利用湿法炼锌渣(主要含有GeO2、ZnO、FeO、Fe2O3、SiO2)制备高纯锗的工艺流程:
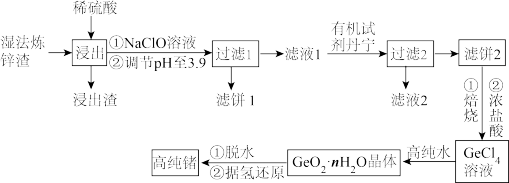
已知:①GeO2为两性化合物。
②常温下,部分金属阳离子转化为氢氧化物沉淀的pH见下表。
③有机试剂丹宁沉淀金属离子的沉淀率见下表。
(1)“浸出”时加热的目的是___________ ;浸出渣的主要成分是___________ (填化学式)。
(2)浸出后加入NaClO溶液的作用是___________ 。
(3)“滤液2”中主要含有的金属阳离子是___________ (填离子符号)。
(4)GeCl4与高纯水反应的化学方程式为___________ 。
(5)I2的一种制备方法如下图所示:
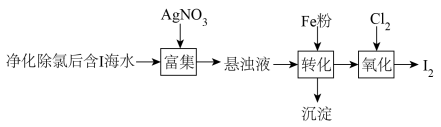
加入Fe粉进行转化反应的离子方程式为___________ ,生成的沉淀与硝酸反应,生成___________ 后可循环使用。

已知:①GeO2为两性化合物。
②常温下,部分金属阳离子转化为氢氧化物沉淀的pH见下表。
| 离子 | Fe2+ | Fe3+ | Zn2+ | Ge4+ |
| 开始沉淀pH | 7.5 | 2.2 | 6.2 | 8.2 |
| 完全沉淀pH | 9.0 | 3.2 | 8.2 | 11.2 |
| 离子 | Fe2+ | Fe3+ | Zn2+ | Ge4+ |
| 沉淀率(%) | 0 | 99 | 0 | 97~98.5 |
(2)浸出后加入NaClO溶液的作用是
(3)“滤液2”中主要含有的金属阳离子是
(4)GeCl4与高纯水反应的化学方程式为
(5)I2的一种制备方法如下图所示:

加入Fe粉进行转化反应的离子方程式为
您最近一年使用:0次
【推荐3】碘元素是人体必需的微量元素之一。某学习小组在实验室进行海带提碘的探究,实验过程如下:
Ⅰ.海带中碘元素的确定
(1)同学们称取一定量干海带,将海带先剪碎,然后用水浸泡、洗净、晾干,放入_______ (填仪器名称)中灼烧至海带完全成灰烬,然后继续进行下列流程。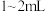 ,加入
,加入 稀硫酸、
稀硫酸、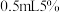 的
的 溶液,然后再加入
溶液,然后再加入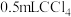 ,振荡后静置,若观察到
,振荡后静置,若观察到_______ (填实验现象),则证明海带中含有碘元素,上述过程中涉及的离子反应方程式为_______ 。
Ⅱ.海带提碘 中,可采取的操作是
中,可采取的操作是_______ 。
(4)从含碘的有机溶剂中提取碘和回收有机溶剂,还需经过蒸馏,指出图实验装置中存在的错误之处_______ 。
Ⅲ.人体碘的重要来源之一是食用加碘食盐(含 )。为测定加碘食盐中的碘含量,学习小组设计如下实验:
)。为测定加碘食盐中的碘含量,学习小组设计如下实验: 食盐样品,加适量蒸馏水使其完全溶解;
食盐样品,加适量蒸馏水使其完全溶解;
②用稀硫酸酸化所得溶液,加入足量 溶液,使
溶液,使 与
与 反应完全生成
反应完全生成 ;
;
③向②中混合液逐滴加入浓度为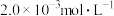 的
的 溶液,恰好反应完全时,消耗
溶液,恰好反应完全时,消耗 溶液
溶液 。(已知:
。(已知: )
)
(5)写出步骤②中发生反应的离子方程式_______ 。
(6)上述实验样品中碘元素的含量为_______ 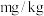 (用含w的代数式表示)。
(用含w的代数式表示)。
Ⅰ.海带中碘元素的确定
(1)同学们称取一定量干海带,将海带先剪碎,然后用水浸泡、洗净、晾干,放入

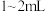 ,加入
,加入 稀硫酸、
稀硫酸、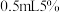 的
的 溶液,然后再加入
溶液,然后再加入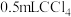 ,振荡后静置,若观察到
,振荡后静置,若观察到Ⅱ.海带提碘

 中,可采取的操作是
中,可采取的操作是(4)从含碘的有机溶剂中提取碘和回收有机溶剂,还需经过蒸馏,指出图实验装置中存在的错误之处
Ⅲ.人体碘的重要来源之一是食用加碘食盐(含
 )。为测定加碘食盐中的碘含量,学习小组设计如下实验:
)。为测定加碘食盐中的碘含量,学习小组设计如下实验: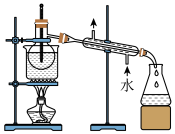
 食盐样品,加适量蒸馏水使其完全溶解;
食盐样品,加适量蒸馏水使其完全溶解;②用稀硫酸酸化所得溶液,加入足量
 溶液,使
溶液,使 与
与 反应完全生成
反应完全生成 ;
;③向②中混合液逐滴加入浓度为
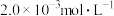 的
的 溶液,恰好反应完全时,消耗
溶液,恰好反应完全时,消耗 溶液
溶液 。(已知:
。(已知: )
)(5)写出步骤②中发生反应的离子方程式
(6)上述实验样品中碘元素的含量为
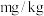 (用含w的代数式表示)。
(用含w的代数式表示)。
您最近一年使用:0次



