A、B、C、D、E为前四周期的五种元素,原子序数依次增大。基态A原子核外电子的L层电子数是K层的2倍;B原子基态时的2p轨道上未成对的电子数最多;C元素为最活泼的非金属元素;D元素核外有3个电子层,最外层电子数是核外电子总数的 ;E元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素与B元素位于同一主族,其某种氧化物有剧毒。
(1)画出基态B原子的轨道表示式_______ 。
(2)B的最简单气态氢化物的空间构型为_______ 。
(3)DC2的电子式为_______ 。
(4)第一电离能D_______ (填“>”、“<”或“=”)Al,原因是_______ 。
(5)B、C、E三种元素电负性由大到小的顺序为_______ (用元素符号表示)。
(6)相同条件下,A、B的最简单氢化物在水中溶解度较大的是_______ (填化学式),理由是_______ 。
 ;E元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素与B元素位于同一主族,其某种氧化物有剧毒。(1)画出基态B原子的轨道表示式
(2)B的最简单气态氢化物的空间构型为
(3)DC2的电子式为
(4)第一电离能D
(5)B、C、E三种元素电负性由大到小的顺序为
(6)相同条件下,A、B的最简单氢化物在水中溶解度较大的是
更新时间:2022-07-29 11:10:45
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生大量的白烟,D是日常生活中常见的盐(部分反应物和生成物及溶剂水已略去)。

请回答下列问题:
(1)甲元素在周期表中的位置_______ 。
(2)A的电子式为_______ ;B的电子式为_______ 。
(3)写出A溶液和甲反应生成丙的化学方程式_______ 。
(4)如何检验E溶液中阳离子?_______ 。
(5)B的实验室制法化学方程式_______ 。

请回答下列问题:
(1)甲元素在周期表中的位置
(2)A的电子式为
(3)写出A溶液和甲反应生成丙的化学方程式
(4)如何检验E溶液中阳离子?
(5)B的实验室制法化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期元素X、Y、Z、W的原子序数依次增大,Z的一种常见氧化物是形成酸雨的罪魁祸首。X、Y、W可组成化合物I,I和Ca(OH)2共热的关系图如图:
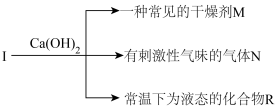
(1)W的元素符号为_______ ;Z原子的结构示意图为_______ 。
(2)I、N的电子式分别为_______ 、_______ 。
(3)I和Ca(OH)2共热的化学方程式为_______ 。
(4)I、M、N、R中离子化合物有_______ ;共价化合物有_______ 。

(1)W的元素符号为
(2)I、N的电子式分别为
(3)I和Ca(OH)2共热的化学方程式为
(4)I、M、N、R中离子化合物有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】氯化镁(MgCl2)可用作部分食品的添加剂、小麦粉处理剂、融雪剂等。某MgCO3样品中含有Fe2O3、FeO杂质,以该样品制取MgCl2溶液的流程如图:

已知: Fe3+在pH=6时可完全生成Fe (OH)3沉淀,Fe2+在pH=7.6时可完全生成Fe (OH) 2沉淀。
请回答下列问题:
(1)Fe2O3属于_____ (填“酸”或“碱”)性氧化物,写出一条基于其物理性质的用途________________ 。
(2)“酸溶”所得气体的电子式为__________________ 。
(3)加入氯水的作用是__________________ ,该反应的离子方程式为_____________________ 。
(4)滤渣的化学式为______________ 。
(5)请设计实验方案,检验过滤后所得氯化镁溶液中铁元素是否已被除尽:_________________ 。

已知: Fe3+在pH=6时可完全生成Fe (OH)3沉淀,Fe2+在pH=7.6时可完全生成Fe (OH) 2沉淀。
请回答下列问题:
(1)Fe2O3属于
(2)“酸溶”所得气体的电子式为
(3)加入氯水的作用是
(4)滤渣的化学式为
(5)请设计实验方案,检验过滤后所得氯化镁溶液中铁元素是否已被除尽:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E、F是原子序数依次增大的短周期主族元素。其相关信息如下表所示:
回答下列问题:
(1)F的原子结构示意图为_______ 。F和溴分别与氢形成的化合物.更稳定的是_______ (填化学式)。
(2)上述六种元素的原子中半径最大的是_______ (填元素符号)。
(3)E的最高价氧化物对应的水化物的化学式为_______ 。
(4)B的氢化物与B的最高价氧化物对应的水化物反应的离子方程式为_______ 。
| 元素 | 相关信息 |
| A | A的原子半径在短周期中最小 |
| B | A、B形成的最简单化合物X是一种气体,其水溶液呈碱性 |
| C | C的最外层电子数是内层电子数的3倍 |
| D | 常温下,D的单质在浓硫酸中会钝化 |
| E | E和C处于同一主族 |
(1)F的原子结构示意图为
(2)上述六种元素的原子中半径最大的是
(3)E的最高价氧化物对应的水化物的化学式为
(4)B的氢化物与B的最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】a、b、c、d、e、f是原子序数依次递增的短周期元素,周期表中b与c、c与d相邻;b与f的最外层电子数之比为2:3,c的最外层电子数比f的最外层电子数少1个;常见化合物e2d2与水反应生成d的单质;a与d两元素只能形成两种化合物,电子数分别为10和18个。
(1)b、c、d氢化物稳定性顺序为(用分子式表示)______ <______<______;
(2)由4个a原子、2个c、3个d原子组成化合物Z,则Z中的化学键类型为______ ;
(3)bc-离子的电子式为____________ ;
(4)一定量的e2d2与bd2反应后的固体物质,恰好与0.8 mol稀盐酸溶液完全反应,并收集到0.25 mol气体,则该固体物质的组成为_______ mol Na2O2、________ mol Na2CO3。
(1)b、c、d氢化物稳定性顺序为(用分子式表示)
(2)由4个a原子、2个c、3个d原子组成化合物Z,则Z中的化学键类型为
(3)bc-离子的电子式为
(4)一定量的e2d2与bd2反应后的固体物质,恰好与0.8 mol稀盐酸溶液完全反应,并收集到0.25 mol气体,则该固体物质的组成为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】前四周期元素A、B、C、D、E的原子序数依次增大,基态A原子核外电子占据3个轨道,基态B原子核外电子占据3个能级且每个能级上电子数相等,C的双原子单质分子中σ键和π键数目之比为1∶2,D的最高化合价和最低化合价代数和等于4;基态E原子核外有6个未成对电子。
(1)基态E原子的价电子排布式为_______ ;基态D原子核外电子占据的能量最高的能级符号为_______ 。
(2)A元素的各级电离能数据如表:
分析表中数据可知,相邻两级的电离能中,I3和I4之间差异最大,其主要原因是_______ 。
(3)A、B、C元素的最高价氧化物对应的水化物酸性依次增强,其原因是_______ 。
(4)氯元素与A、B、C元素组成的共价分子ACl3、BCl4、CCl3中,中心原子采用sp3杂化、空间结构为三角锥形的是_______ (填分子式)。
(5)(DC)4为热色性固体,且有色温效应.其颜色在低于-30℃时为淡黄色,室温下为橙黄色,高于100℃时为深红色。在淡黄色→橙黄色→深红色的转化中,破坏的作用力是_______ ;在常压下,(DC)4高于130℃分解为相应的单质,这一变化中破坏的作用力是_______ 。在B、C、D的简单气态氢化物中,属于非极性分子的是_______ (填分子式)。
(6)A、C形成立方晶体,晶体结构类似于金刚石,如图所示(白色球代表A原子,黑色球代表C原子).

该晶体的化学式为_______ 。
(1)基态E原子的价电子排布式为
(2)A元素的各级电离能数据如表:
| 符号 | I1 | I2 | I3 | I4 | I5 |
电离能/( ) ) | 800.6 | 2427 | 3660 | 25026 | 32827 |
分析表中数据可知,相邻两级的电离能中,I3和I4之间差异最大,其主要原因是
(3)A、B、C元素的最高价氧化物对应的水化物酸性依次增强,其原因是
(4)氯元素与A、B、C元素组成的共价分子ACl3、BCl4、CCl3中,中心原子采用sp3杂化、空间结构为三角锥形的是
(5)(DC)4为热色性固体,且有色温效应.其颜色在低于-30℃时为淡黄色,室温下为橙黄色,高于100℃时为深红色。在淡黄色→橙黄色→深红色的转化中,破坏的作用力是
(6)A、C形成立方晶体,晶体结构类似于金刚石,如图所示(白色球代表A原子,黑色球代表C原子).

该晶体的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:_____ 。
(2)o、p两种元素的部分电离能数据如下表所示:
比较两元素的 、
、 可知,气态
可知,气态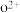 再失去一个电子比气态
再失去一个电子比气态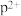 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是 ___________ 。
(3)表中所列的某主族元素的电离能情况如图所示,则该元素是上述元素中的____ (填元素符号)。


试回答下列问题:
(1)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:
(2)o、p两种元素的部分电离能数据如下表所示:
| 元素 | o | p | |
电离能/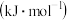 |  | 717 | 763 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
比较两元素的
 、
、 可知,气态
可知,气态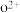 再失去一个电子比气态
再失去一个电子比气态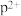 再失去一个电子难。对此,你的解释是
再失去一个电子难。对此,你的解释是 (3)表中所列的某主族元素的电离能情况如图所示,则该元素是上述元素中的

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】碳、氧、氮、镁、铬、铁、铜是几种重要的元素,请回答下列问题:
(1) 在第二周期的元素中,第一电离能介于B 与N之间的元素有_________ 种。
(2)查阅相关资料发现MgO的熔点比CuO的熔点高得多,其原因是____________________ 。
(3)Fe 与CO能形成一种重要的催化剂Fe(CO)5,该分子中σ键与π键个数比为______________ 。请写出一个与CO互为等电子体的离子:____________________ 。
(4)金属铬是一种银白色,极硬,耐腐蚀的金属,铬的化合物种类繁多,如:Cr2(SO4)3、K2Cr2O7以及配离子[Cr(H2O)3(NH3)3]3+。
①K2Cr2O7具有很强的氧化性,能直接将CH3CH2OH 氧化成CH3COOH,试写出基态铬原子的价层电子排布式:_______________ ;CH3COOH 分子中碳原子的杂化类型为_________________ ;乙醇和丙烷相对分子质量相近,但乙醇的熔、沸点比丙烷高很多,试解释其主要原因:____________________________________ 。
②该配离子[Cr(H2O)3(NH3)3]3+中,中心离子的配位数为_______ ,NH3的VSEPR模型为_______ 。
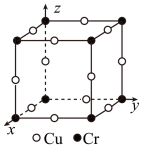
③图为Cu-Cr形成的一种合金的晶胞(假设晶体中原子之间彼此相切),单独属于该晶胞的Cu原子共有三个,其原子坐标可分别表示为:( ,0,0)、 (0,
,0,0)、 (0, ,0)、
,0)、_______ ;已知晶胞中Cr 和Cu原子间的最近距离为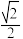 a pm,则该晶体的密度为
a pm,则该晶体的密度为_______ g·cm-3 (用含a的代数式表示,设N A为阿伏伽德罗常数的值)。
(1) 在第二周期的元素中,第一电离能介于B 与N之间的元素有
(2)查阅相关资料发现MgO的熔点比CuO的熔点高得多,其原因是
(3)Fe 与CO能形成一种重要的催化剂Fe(CO)5,该分子中σ键与π键个数比为
(4)金属铬是一种银白色,极硬,耐腐蚀的金属,铬的化合物种类繁多,如:Cr2(SO4)3、K2Cr2O7以及配离子[Cr(H2O)3(NH3)3]3+。
①K2Cr2O7具有很强的氧化性,能直接将CH3CH2OH 氧化成CH3COOH,试写出基态铬原子的价层电子排布式:
②该配离子[Cr(H2O)3(NH3)3]3+中,中心离子的配位数为
③图为Cu-Cr形成的一种合金的晶胞(假设晶体中原子之间彼此相切),单独属于该晶胞的Cu原子共有三个,其原子坐标可分别表示为:(
 ,0,0)、 (0,
,0,0)、 (0, ,0)、
,0)、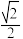 a pm,则该晶体的密度为
a pm,则该晶体的密度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】现有前四周期的A、B、C、D、E、F六种元素,原子序数依次增大。A元素基态原子的价电子排布式为nsnnpn+1;C元素为最活泼的非金属元素;D元素原子核外有三个电子层,其最外层电子数是核外电子总数的 ;E元素基态正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子。
;E元素基态正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子。
(1)A元素的第一电离能___________ (填“<”“>”或“=”)B元素的第一电离能, A、B、C三种元素的电负性由小到大的顺序为___________ (用元素符号表示)。
(2)基态D元素原子的原子结构示意图为___________ 。
(3)基态C元素原子的电子排布图为___________ ;E3+的离子价电子排布式为___________ 。
(4)F元素位于元素周期表的___________ 区,其基态原子的电子排布式为___________ 。
(5)金属性:D___________ (填“>”或“<”)Al。
 ;E元素基态正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子。
;E元素基态正三价离子的3d轨道为半充满状态;F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子。(1)A元素的第一电离能
(2)基态D元素原子的原子结构示意图为
(3)基态C元素原子的电子排布图为
(4)F元素位于元素周期表的
(5)金属性:D
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】碳元素在自然界中分布很广,是存在形式最复杂的元素。实验室可用邻二氮菲( )与Fe2+形成的红色配合物(如下图)测定铁的含量。
)与Fe2+形成的红色配合物(如下图)测定铁的含量。
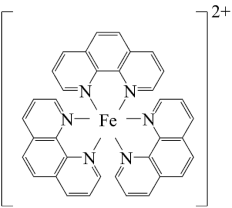
回答下列问题:
(1)基态Fe原子核外电子的空间运动状态有__________ 种。
(2)红色配合物中H、C、N、Fe四种元素的电负性从大到小的顺序为__________ 。
(3)邻二氮菲分子中C、N两种元素原子的杂化方式分别为__________ 、__________ 。
(4)红色配离子的中心原子的配位数为__________ 。
(5)红色配离子中不存在的作用力有__________ 。
A. σ键 B.π键 C.离子键 D.氢键 E.配位键
(6)临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是__________ 。
(7)三甲胺[N(CH3)3]和乙二胺(H2N-CH2-CH2-NH2)均属于胺,但三甲胺比乙二胺的沸点低得多,原因是__________ 。
(8)汽车安全气囊产生气体的功臣是叠氮化钠(NaN3),N 的空间构型为
的空间构型为__________ 。
(9)钨和碳能形成耐高温、耐磨材料碳化钨,其晶体结构如下图所示,六棱柱的底边长为apm,高为bpm,设阿伏加德罗常数的值为NA,则碳化钨晶体的密度是__________ g·cm-3(列出计算表达式)。

 )与Fe2+形成的红色配合物(如下图)测定铁的含量。
)与Fe2+形成的红色配合物(如下图)测定铁的含量。
回答下列问题:
(1)基态Fe原子核外电子的空间运动状态有
(2)红色配合物中H、C、N、Fe四种元素的电负性从大到小的顺序为
(3)邻二氮菲分子中C、N两种元素原子的杂化方式分别为
(4)红色配离子的中心原子的配位数为
(5)红色配离子中不存在的作用力有
A. σ键 B.π键 C.离子键 D.氢键 E.配位键
(6)临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是
(7)三甲胺[N(CH3)3]和乙二胺(H2N-CH2-CH2-NH2)均属于胺,但三甲胺比乙二胺的沸点低得多,原因是
(8)汽车安全气囊产生气体的功臣是叠氮化钠(NaN3),N
 的空间构型为
的空间构型为(9)钨和碳能形成耐高温、耐磨材料碳化钨,其晶体结构如下图所示,六棱柱的底边长为apm,高为bpm,设阿伏加德罗常数的值为NA,则碳化钨晶体的密度是

您最近一年使用:0次
【推荐2】氮的化合物在工业生产中有重要用途,请回答下列问题:
(1)[Ni(N2H4)2](N3)2是一种富氮含能材料。写出一种与N 互为等电子体的分子:
互为等电子体的分子:_______ (填化学式);实验数据表明键角:NH3>PH3>AsH3,分析原因是_______ 。
(2)氮与碳还能形成一种离子液体的正离子 ,为使该正离子以单个形式存在以获得良好的溶解性能,与N原子相连的-C2H5,不能被H原子替换,原因是
,为使该正离子以单个形式存在以获得良好的溶解性能,与N原子相连的-C2H5,不能被H原子替换,原因是_______ 。
(3)配合物顺铂[Pt(NH3)2Cl2]是临床使用的第一代铂类抗癌药物。顺铂的抗癌机理:在铜转运蛋白的作用下,顺铂进入人体细胞发生水解,生成的Pt(NH3)2(OH)Cl破坏DNA的结构,阻止癌细胞增殖。如:
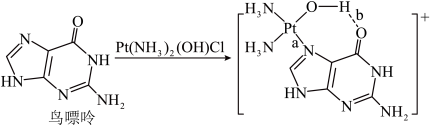
①基态Cu原子价层电子的轨道表示式为_______ ,鸟嘌呤中氮原子的杂化方式为______ 。构成鸟嘌呤的元素电负性由大到小的顺序_______ 。
②在Pt(NH3)2Cl2中,配体与铂(Ⅱ)的结合能力:Cl-_______ NH3(填“>”或“<”)。
③顺铂和反铂互为同分异构体,两者的结构和性质如表。
请从分子结构角度解释顺铂在水中的溶解度大于反铂的原因是________ 。
④顺铂的发现与铂电极的使用有关。铂晶胞为正方体,边长为a nm,结构如图。铂晶体的摩尔体积Vm=_______ m3/mol(阿伏加德罗常数为NA)。(已知:单位物质的量的物质所具有的体积叫做摩尔体积)

(1)[Ni(N2H4)2](N3)2是一种富氮含能材料。写出一种与N
 互为等电子体的分子:
互为等电子体的分子:(2)氮与碳还能形成一种离子液体的正离子
 ,为使该正离子以单个形式存在以获得良好的溶解性能,与N原子相连的-C2H5,不能被H原子替换,原因是
,为使该正离子以单个形式存在以获得良好的溶解性能,与N原子相连的-C2H5,不能被H原子替换,原因是(3)配合物顺铂[Pt(NH3)2Cl2]是临床使用的第一代铂类抗癌药物。顺铂的抗癌机理:在铜转运蛋白的作用下,顺铂进入人体细胞发生水解,生成的Pt(NH3)2(OH)Cl破坏DNA的结构,阻止癌细胞增殖。如:

①基态Cu原子价层电子的轨道表示式为
②在Pt(NH3)2Cl2中,配体与铂(Ⅱ)的结合能力:Cl-
③顺铂和反铂互为同分异构体,两者的结构和性质如表。
| 顺铂 | 反铂 | |
| 结构 |  | 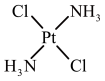 |
| 25℃时溶解度/g | 0.2577 | 0.0366 |
④顺铂的发现与铂电极的使用有关。铂晶胞为正方体,边长为a nm,结构如图。铂晶体的摩尔体积Vm=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】钴是生产耐热合金、硬质合金、防腐合金、磁性合金和各种钴盐的重要原料。在奥运场馆中美丽的透光气囊材料由含氟的化合物制成。请回答下列问题:
(1)过渡元素Co基态原子的价电子排布图(轨道表示式)为___________ ;第四电离能 ,其原因是
,其原因是___________ 。
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学疗法中的光敏剂、催化剂等方面得到了广泛的应用。其结构如图所示,中心离子为钴离子。
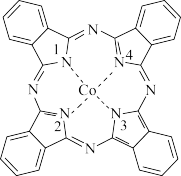
①酞菁钴中三种非金属原子的电负性由大到小的顺序为___________ (用相应的元素符号作答)。
②与钴离子通过配位键结合的氮原子数有___________ 个。
③酞菁钴中氮原子的杂化类型为___________ 。
(3) 分子与
分子与 结合成配合物
结合成配合物 ,与游离的氨分子相比,其键角
,与游离的氨分子相比,其键角
___________ (填“较大”“较小”或“相同”),解释原因:___________ 。
(4)萤石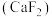 是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是
是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是___________ ;X离子的配位数是___________ ,若该立方晶胞参数为 ,正负离子的核间距最小为
,正负离子的核间距最小为___________ pm。

(1)过渡元素Co基态原子的价电子排布图(轨道表示式)为
 ,其原因是
,其原因是(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学疗法中的光敏剂、催化剂等方面得到了广泛的应用。其结构如图所示,中心离子为钴离子。

①酞菁钴中三种非金属原子的电负性由大到小的顺序为
②与钴离子通过配位键结合的氮原子数有
③酞菁钴中氮原子的杂化类型为
(3)
 分子与
分子与 结合成配合物
结合成配合物 ,与游离的氨分子相比,其键角
,与游离的氨分子相比,其键角
(4)萤石
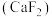 是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是
是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是 ,正负离子的核间距最小为
,正负离子的核间距最小为
您最近一年使用:0次



