恒温下,将amolN2与amolH2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g) 2NH3(g)。
2NH3(g)。
(1)若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,计算a的值_____ 。
(2)反应达平衡时,其中NH3的含量(体积分数为25%。计算平衡时NH3的物质的量为_____ 。
(3)原混合气体与平衡混和气体的压强比____ 。
 2NH3(g)。
2NH3(g)。(1)若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,计算a的值
(2)反应达平衡时,其中NH3的含量(体积分数为25%。计算平衡时NH3的物质的量为
(3)原混合气体与平衡混和气体的压强比
更新时间:2022-08-27 07:39:55
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】实验室里通常用MnO2与浓盐酸反应制取氯气,其反应的化学方程式为:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O ,把8.7gMnO2放入浓盐酸中完全反应,计算:
MnCl2+Cl2↑+2H2O ,把8.7gMnO2放入浓盐酸中完全反应,计算:
(1)8.7gMnO2的物质的量___________ ;
(2)参加反应的HCl的物质的量__________ ;
(3)生成Cl2的体积________________ (标准状况)。
 MnCl2+Cl2↑+2H2O ,把8.7gMnO2放入浓盐酸中完全反应,计算:
MnCl2+Cl2↑+2H2O ,把8.7gMnO2放入浓盐酸中完全反应,计算:(1)8.7gMnO2的物质的量
(2)参加反应的HCl的物质的量
(3)生成Cl2的体积
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】Zn与不同浓度的H2SO4反应,其还原产物不同,
(1)将13g锌粉投入足量的18.4mol/L的浓硫酸中,充分反应后,所得SO2气体其标况下体积为多少升?_____
(2)若将一定量的锌投入100mL14.5mol/L的浓硫酸中,反应后锌完全溶解,将反应后溶液稀释至1L,测得溶液中c(SO42﹣)=1.05mol/L、[H+]=0.1mol/L.反应产生SO2体积(标准状况下)V(SO2)=_____ L,V(H2)=_____ L。
(3)将(1)中产生的气体缓缓通入100MLamol/L NaOH溶液中,SO2、NaOH都完全消耗,则a的取值范围为_____ 。
(1)将13g锌粉投入足量的18.4mol/L的浓硫酸中,充分反应后,所得SO2气体其标况下体积为多少升?
(2)若将一定量的锌投入100mL14.5mol/L的浓硫酸中,反应后锌完全溶解,将反应后溶液稀释至1L,测得溶液中c(SO42﹣)=1.05mol/L、[H+]=0.1mol/L.反应产生SO2体积(标准状况下)V(SO2)=
(3)将(1)中产生的气体缓缓通入100MLamol/L NaOH溶液中,SO2、NaOH都完全消耗,则a的取值范围为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】在一定条件下,将2 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。
xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。
(1)x=_______ ,2min内A的平均反应速率v(A)=_______ 。
(2)B的转化率为_______ ,该温度下反应的平衡常数的值为_______ (结果保留三位有效数字)。
(3)其他条件不变,若再向容器中加入0.2 mol B和0.2 mol C,此时v(正)_______ v(逆)(填“>”“=”或“<”)。
 xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。
xC(g)+2D(g)。2 min末该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。(1)x=
(2)B的转化率为
(3)其他条件不变,若再向容器中加入0.2 mol B和0.2 mol C,此时v(正)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】在恒温的2L密闭容器中进行反应,气体X、Y,Z的物质的量随时间的变化曲线如图所示,反应在t时刻达到平衡。

(1)该反应的化学方程式是___ 。
(2)反应起始至t时刻,Y的平均反应速率是___ 。
(3)关于该反应的说法正确的是___ 。
a. 到达t时刻该反应已停止
b. 在t时刻正反应速率等于逆反应速率
c. 混合气体的密度不再改变说明该反应达到平衡
d. 达到化学平衡时,3v正(X)=2v逆(Y)
(4)tmin后,体系内的压强与反应前的压强之比为:___ 。

(1)该反应的化学方程式是
(2)反应起始至t时刻,Y的平均反应速率是
(3)关于该反应的说法正确的是
a. 到达t时刻该反应已停止
b. 在t时刻正反应速率等于逆反应速率
c. 混合气体的密度不再改变说明该反应达到平衡
d. 达到化学平衡时,3v正(X)=2v逆(Y)
(4)tmin后,体系内的压强与反应前的压强之比为:
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】生产实践和科学研究中的大量事实说明,为了使化学反应更好地服务于人类,需要从化学反应的快慢和进行的程度这两个角度进一步认识它们。在一定温度下,向1.0L密闭容器中加入0.60molX(g),发生反应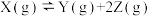 。测得反应物X的浓度与反应时间的数据如下表:
。测得反应物X的浓度与反应时间的数据如下表:
(1)写出两种 提高该化学反应速率的措施_______ 。
(2)2min时Y的物质的量为_______ mol。
(3)分析该反成中反应物的浓度与时间的规律,得出的结论是_______ 。
由此规律推出尺应在6min时反应物的浓度a为_______  。
。
(4)某一时刻反应达到平衡,若此时 ,则Z的物质的量浓度为
,则Z的物质的量浓度为_______ 。
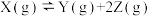 。测得反应物X的浓度与反应时间的数据如下表:
。测得反应物X的浓度与反应时间的数据如下表:| 反应时间t/min | 0 | 1 | 2 | 3 | 4 | 6 | 8 |
 | 0.60 | 0.42 | 0.30 | 0.21 | 0.15 | a | 0.0375 |
(1)写出
(2)2min时Y的物质的量为
(3)分析该反成中反应物的浓度与时间的规律,得出的结论是
由此规律推出尺应在6min时反应物的浓度a为
 。
。(4)某一时刻反应达到平衡,若此时
 ,则Z的物质的量浓度为
,则Z的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1 mol NH3通入3 L的密闭容器中进行反应(此时容器内总压为200 kPa),各物质的分压随时间的变化曲线如图所示。

(1)若保持容器容积不变,t1时反应达到平衡,用H2的浓度变化表示0~t1时间内的反应速率v(H2)=___________ mol·L-1·min-1(用含t1的代数式表示)
(2)在该温度下,反应的标准平衡常数K⊖=___________ [已知:分压=总压×该组分物质的量分数,对于反应dD(g)+eE(g)  gG(g)+hH(g) K⊖=
gG(g)+hH(g) K⊖= ,其中p⊖=100 kPa,pG、pH、pD、pE为各组分的平衡分压]
,其中p⊖=100 kPa,pG、pH、pD、pE为各组分的平衡分压]

(1)若保持容器容积不变,t1时反应达到平衡,用H2的浓度变化表示0~t1时间内的反应速率v(H2)=
(2)在该温度下,反应的标准平衡常数K⊖=
 gG(g)+hH(g) K⊖=
gG(g)+hH(g) K⊖= ,其中p⊖=100 kPa,pG、pH、pD、pE为各组分的平衡分压]
,其中p⊖=100 kPa,pG、pH、pD、pE为各组分的平衡分压]
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】在一定温度下,在某4L恒容容器内发生气体M和气体N的转化反应。它们的物质的量随时间变化的曲线如图所示。

(1)该反应的化学方程式为_________ (需要标注M、N的物质状态,且系数化成最简整数)。
(2)比较t2时刻,正、逆反应速率大小:v(正)_________ v(逆)(填“>”“=”或“<”)。
(3)若t2=2min,反应开始至t2时刻,M的平均化学反应速率v(M)_________ mol·L-1·min-1。
(4)该反应的化学平衡常数K=_________ 。
(5)若维持其他条件不变,在t3时升高温度,M的浓度降低,则该反应△H_________ 0(填“>”“=”或“<”)。

(1)该反应的化学方程式为
(2)比较t2时刻,正、逆反应速率大小:v(正)
(3)若t2=2min,反应开始至t2时刻,M的平均化学反应速率v(M)
(4)该反应的化学平衡常数K=
(5)若维持其他条件不变,在t3时升高温度,M的浓度降低,则该反应△H
您最近一年使用:0次

 C(g)+xD(g),5s达到平衡。达到平衡时,生成了1molC,测定D的浓度为1mol/L。
C(g)+xD(g),5s达到平衡。达到平衡时,生成了1molC,测定D的浓度为1mol/L。

