在一定的温度下,对于pH值相同的氨水和氢氧化钠稀溶液,下列说法正确的是
| A.中和等体积的这两种溶液,消耗在氢氧化钠稀溶液的盐酸比较多 |
| B.在同等程度稀释时,pH下降程度相同 |
| C.氨水中氨的物质的量浓度等于氢氧化钠溶液中氢氧化钠的物质的量浓度 |
| D.氨水中铵根离子的物质的量的浓度等于氢氧化钠溶液中钠离子的物质的量的浓度 |
更新时间:2022-08-16 15:36:18
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】室温时,盐酸和硫酸的混合溶液20 mL,向混合物中逐滴加入0.05 mol/L Ba(OH)2溶液,生成的BaSO4和pH的变化如图所示(不考虑溶液混合时体积的变化)。下列说法不正确的是
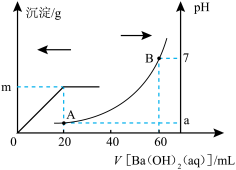

| A.原混合液中盐酸物质的量浓度为0.2 mol/L |
| B.逐滴加入Ba(OH)2溶液,当体积为40 mL,此时发生的离子方程式:OH-+H+=H2O |
| C.生成沉淀的最大质量m=2.33g |
| D.现将上述20 mL酸混合溶液与60 mL Ba(OH)2溶液直接混合,发生的离子方程式:Ba2++6OH-+SO42-+6H+=BaSO4↓+6H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】现有常温下4种溶液:①盐酸;②醋酸溶液;③氢氧化钠溶液;④氨水。已知①和②的pH为a,③和④的pH为b,且 b
b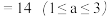 。则下列观点错误的是
。则下列观点错误的是
 b
b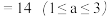 。则下列观点错误的是
。则下列观点错误的是A.若 时,则溶液④中水电离出的 时,则溶液④中水电离出的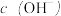 等于 等于 |
| B.若将①和③分别加水稀释100倍,则稀释后两溶液的pH之和仍为14 |
| C.若将等体积的②和③分别与足量铝粉反应,生成的氢气后者多 |
D.若将①和④等体积混合,则混合后的溶液中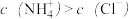 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某温度下,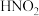 和
和 的电离常数分别为
的电离常数分别为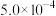 和
和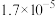 。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是

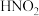 和
和 的电离常数分别为
的电离常数分别为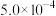 和
和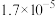 。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
A.曲线II代表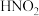 溶液 溶液 |
B.a点溶液中, |
C.从c点到d点,溶液中 增大 (其中 增大 (其中 、 、 分别代表相应的酸和酸根离子) 分别代表相应的酸和酸根离子) |
D.相同体积a点的两溶液分别与 恰好中和后,溶液中 恰好中和后,溶液中 相同 相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,① 的
的 溶液、②
溶液、② 的
的 溶液、③
溶液、③ 的氨水、④
的氨水、④ 的
的 溶液,相同条件下,有关上述溶液的比较中错误的是
溶液,相同条件下,有关上述溶液的比较中错误的是
 的
的 溶液、②
溶液、② 的
的 溶液、③
溶液、③ 的氨水、④
的氨水、④ 的
的 溶液,相同条件下,有关上述溶液的比较中错误的是
溶液,相同条件下,有关上述溶液的比较中错误的是A.水电离的 :①=④>②=③ :①=④>②=③ |
B.将②③溶液等体积混合后 |
| C.②④溶液混合后呈中性,则两溶液的体积关系是②:④=1:10 |
D.将①溶液和②溶液分别稀释10倍、100倍后,所得两溶液的 相等 相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 是一种常用的食品防腐剂。已知
是一种常用的食品防腐剂。已知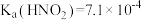 。下列叙述正确的是
。下列叙述正确的是
 是一种常用的食品防腐剂。已知
是一种常用的食品防腐剂。已知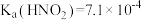 。下列叙述正确的是
。下列叙述正确的是A. 溶液的pH随温度升高而增大 溶液的pH随温度升高而增大 |
B.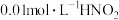 溶液的 溶液的 |
C.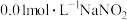 溶液中 溶液中 |
D.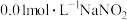 溶液中 溶液中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在二氧化碳的水溶液中存在着如下平衡: CO2(g) CO2(aq)CO2(aq)+H2O
CO2(aq)CO2(aq)+H2O H2CO3(aq) H2CO3(aq)
H2CO3(aq) H2CO3(aq) H+(aq)+HCO3-(aq)HCO3-(aq)
H+(aq)+HCO3-(aq)HCO3-(aq)  H+(aq)+CO32-(aq)
H+(aq)+CO32-(aq)
下列有关说法正确的是( )
 CO2(aq)CO2(aq)+H2O
CO2(aq)CO2(aq)+H2O H2CO3(aq) H2CO3(aq)
H2CO3(aq) H2CO3(aq) H+(aq)+HCO3-(aq)HCO3-(aq)
H+(aq)+HCO3-(aq)HCO3-(aq)  H+(aq)+CO32-(aq)
H+(aq)+CO32-(aq) 下列有关说法正确的是( )
| A.水中溶解的二氧化碳的浓度,夏天时比冬天时高 |
| B.如果海水略呈碱性,海水中二氧化碳的浓度比纯水高 |
| C.气压升高,水中c(HCO3-)增大 |
| D.常温下,二氧化碳的水溶液中,由水电离出的c(H+)与c(OH-)的乘积等于1×l0-14 |
您最近一年使用:0次

 L-1盐酸滴入20.00mL 1.000mol
L-1盐酸滴入20.00mL 1.000mol


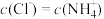
 电离吸热
电离吸热

