按要求填写下列问题:
(1)某些共价化合物(如 、
、 、
、 等)在液态时会发生微弱的电离,如
等)在液态时会发生微弱的电离,如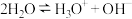 ,则液态
,则液态 的电离方程式为
的电离方程式为_______ 。
(2)已知水溶液中 和
和 的关系如图所示,试回答下列问题:
的关系如图所示,试回答下列问题:

图中五点对应的 的关系是
的关系是_______ 。若从A点到D点,可采用的措施是_______ (填序号)。
a.升温 b.加入少量的盐酸 c.加入少量的NaOH
(3)25℃时, 的HA溶液中
的HA溶液中 。请回答下列问题:
。请回答下列问题:
①HA是_______ (填“强电解质”或“弱电解质”)。
②在加水稀释HA溶液的过程中,随着水量的增加而增大的是_______ (填序号)。
A.c(HA) B. C.
C. 与
与 的乘积 D.
的乘积 D.
(4)现有浓度均为 的下列溶液:①硫酸、②醋酸、③氢氧化钠,三种溶液中由水电离出的
的下列溶液:①硫酸、②醋酸、③氢氧化钠,三种溶液中由水电离出的 浓度由大到小的顺序是
浓度由大到小的顺序是_______ (用序号表示)。
(1)某些共价化合物(如
 、
、 、
、 等)在液态时会发生微弱的电离,如
等)在液态时会发生微弱的电离,如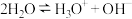 ,则液态
,则液态 的电离方程式为
的电离方程式为(2)已知水溶液中
 和
和 的关系如图所示,试回答下列问题:
的关系如图所示,试回答下列问题:
图中五点对应的
 的关系是
的关系是a.升温 b.加入少量的盐酸 c.加入少量的NaOH
(3)25℃时,
 的HA溶液中
的HA溶液中 。请回答下列问题:
。请回答下列问题:①HA是
②在加水稀释HA溶液的过程中,随着水量的增加而增大的是
A.c(HA) B.
 C.
C. 与
与 的乘积 D.
的乘积 D.
(4)现有浓度均为
 的下列溶液:①硫酸、②醋酸、③氢氧化钠,三种溶液中由水电离出的
的下列溶液:①硫酸、②醋酸、③氢氧化钠,三种溶液中由水电离出的 浓度由大到小的顺序是
浓度由大到小的顺序是
更新时间:2022-09-19 09:42:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】已知水在25℃和95℃时,其电离平衡曲线如右图所示:
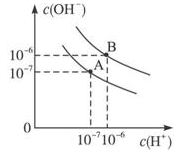
(1)则25℃时水的电离平衡曲线应为__________ (填“A”或“B”);
(2)25℃时,将 =11的NaOH溶液与
=11的NaOH溶液与 =4的
=4的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 =9,则NaOH溶液与
=9,则NaOH溶液与 溶液的体积比为
溶液的体积比为____________ ;
(3)95℃时,若100体积 1=
1= 的某强酸溶液与1体积
的某强酸溶液与1体积 2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的
2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的 1与强碱的
1与强碱的 2之间应满足的关系是
2之间应满足的关系是_______ 。

(1)则25℃时水的电离平衡曲线应为
(2)25℃时,将
 =11的NaOH溶液与
=11的NaOH溶液与 =4的
=4的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 =9,则NaOH溶液与
=9,则NaOH溶液与 溶液的体积比为
溶液的体积比为(3)95℃时,若100体积
 1=
1= 的某强酸溶液与1体积
的某强酸溶液与1体积 2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的
2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的 1与强碱的
1与强碱的 2之间应满足的关系是
2之间应满足的关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列化合物①NaCl、②NaOH、③HCl、④NH4Cl、⑤CH3COONa、⑥CH3COOH、⑦NH3·H2O、⑧H2O,回答问题:
(1)NH4Cl溶液显________ 性,用离子方程式表示________________________ 。
(2)pH=10的CH3COONa溶液中,水电离出来的c(OH-)为________ mol/l,在pH=3的CH3COOH溶液中水电离出来的c(H+)为________ mol/l。
(3)已知水中存在如下平衡:H2O+H2O H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,选择的方法是
H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,选择的方法是________ 。
A.向水中加入NaHSO4固体B.向水中加入Na2CO3固体
C.加热至100℃D.向水中加入(NH4)2SO4固体
(4)若等pH、等体积的②(NaOH)和⑦(氨水)分别加水稀释m倍、n倍,稀释后pH相等,则m________ (填“>”“<”或“=”)n。
(5)等物质的量浓度的NH4Cl、CH3COONH4、NH3·H2O溶液中 浓度由大到小的顺序
浓度由大到小的顺序_____________ 。
(1)NH4Cl溶液显
(2)pH=10的CH3COONa溶液中,水电离出来的c(OH-)为
(3)已知水中存在如下平衡:H2O+H2O
 H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,选择的方法是
H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,选择的方法是A.向水中加入NaHSO4固体B.向水中加入Na2CO3固体
C.加热至100℃D.向水中加入(NH4)2SO4固体
(4)若等pH、等体积的②(NaOH)和⑦(氨水)分别加水稀释m倍、n倍,稀释后pH相等,则m
(5)等物质的量浓度的NH4Cl、CH3COONH4、NH3·H2O溶液中
 浓度由大到小的顺序
浓度由大到小的顺序
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是不同温度下水的离子积常数:
试回答以下问题:
(1)若25℃<T1<T2,则a___________ 1×10-14(填“>”、“<”或“=”),做此判断的理由是___________ 。
(2)25℃时,某Na2SO4溶液中c(SO )=5×10-4mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=
)=5×10-4mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=___________ 。
(3)若T2温度下,向水中滴入稀盐酸,测得溶液中c(H+)=1.0×10-3mol/L,则溶液中c(OH-)=___________ mol/L。
| 温度/℃ | 25 | T1 | T2 |
| 水的离子积常数 | 1×10-14 | a | 1×10-12 |
(1)若25℃<T1<T2,则a
(2)25℃时,某Na2SO4溶液中c(SO
 )=5×10-4mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=
)=5×10-4mol/L,取该溶液1 mL加水稀释至10 mL,则稀释后溶液中c(Na+)∶c(OH-)=(3)若T2温度下,向水中滴入稀盐酸,测得溶液中c(H+)=1.0×10-3mol/L,则溶液中c(OH-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.处于下列状态的物质中:A.固态氯化钠 B.干冰 C.液氨 D.铜 E.硫酸钡晶体 F.甲烷 G.五氧化二磷 H.稀硫酸 I.熔融的硝酸钾 J.石墨 K.酒精 L.胆矾溶液 M.氢氧化铜 N.熟石灰 O.盐酸。
(1)上述物质中属于强电解质且能导电的是_______ (填字母,下同)。
(2)上述物质中属于电解质的是_______ 。
(3)上述物质中属于非电解质的是_______ 。
II.有A、B、C、D四种可溶性盐,它们的阳离子分别是 、
、 、
、 、
、 中的某一种,阴离子分别是
中的某一种,阴离子分别是 、
、 、
、 、
、 中的一种(离子在物质中不重复出现)。
中的一种(离子在物质中不重复出现)。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。请回答下列问题:
(4)A的化学式为_______ ,B的化学式为_______ 。
(5)写出D与足量 溶液反应的离子方程式
溶液反应的离子方程式_______ 。
(6)写出A溶液中阴离子的检验方法_______ 。
(1)上述物质中属于强电解质且能导电的是
(2)上述物质中属于电解质的是
(3)上述物质中属于非电解质的是
II.有A、B、C、D四种可溶性盐,它们的阳离子分别是
 、
、 、
、 、
、 中的某一种,阴离子分别是
中的某一种,阴离子分别是 、
、 、
、 、
、 中的一种(离子在物质中不重复出现)。
中的一种(离子在物质中不重复出现)。①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。请回答下列问题:
(4)A的化学式为
(5)写出D与足量
 溶液反应的离子方程式
溶液反应的离子方程式(6)写出A溶液中阴离子的检验方法
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I、如图表示元素周期表中部分元素的某种性质(X值)随原子序数变化的关系示意图。

(1)短周期中原子核外p能级上电子总数与s能级上电子总数相等的元素是_______ (填元素符号)。
(2)预测S元素与 元素x值的大小关系为
元素x值的大小关系为_______ ,x值最小的元素在元素周期表中的位置是_______ (放射性元素除外)。
(3)下列关于元素性质的说法正确的是_______ (填标号)。
a.X值可反映元素最高正化合价的变化规律
b.X值可反映元素在化合物中吸引电子的能力
c.X值的大小可用来判断元素金属性和非金属性的强弱
II、今有① 、②HCl、③
、②HCl、③ 三种溶液,根据要求回答下列问题:
三种溶液,根据要求回答下列问题:
(4)pH相同的三种酸溶液各lmL,加水稀释相同倍数后,溶液中水电离出来的 的关系为
的关系为_______ 。(用序号填空,下同)
(5)当它们pH相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为_______ 。
(6)中和等体积相同浓度的烧碱溶液,需同浓度的三种溶液的体积分别为 、
、 、
、 ,则
,则 、
、 、
、 的关系为
的关系为_______ (用等式表示)。
III.平衡思想是化学研究的一个重要观念,在水溶液中存在多种平衡体系。
(7)实验室在保存FeCl3溶液时,常在溶液中加少量的_______ ,以抑制其水解;把 溶液蒸干并灼烧,最后得到的固体主要产物是
溶液蒸干并灼烧,最后得到的固体主要产物是_______ 。
(8)在日常生活中经常用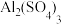 和
和 混合溶液作灭火剂,请用离子方程式表示其灭火原理:
混合溶液作灭火剂,请用离子方程式表示其灭火原理:_______ 。

(1)短周期中原子核外p能级上电子总数与s能级上电子总数相等的元素是
(2)预测S元素与
 元素x值的大小关系为
元素x值的大小关系为(3)下列关于元素性质的说法正确的是
a.X值可反映元素最高正化合价的变化规律
b.X值可反映元素在化合物中吸引电子的能力
c.X值的大小可用来判断元素金属性和非金属性的强弱
II、今有①
 、②HCl、③
、②HCl、③ 三种溶液,根据要求回答下列问题:
三种溶液,根据要求回答下列问题:(4)pH相同的三种酸溶液各lmL,加水稀释相同倍数后,溶液中水电离出来的
 的关系为
的关系为(5)当它们pH相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为
(6)中和等体积相同浓度的烧碱溶液,需同浓度的三种溶液的体积分别为
 、
、 、
、 ,则
,则 、
、 、
、 的关系为
的关系为III.平衡思想是化学研究的一个重要观念,在水溶液中存在多种平衡体系。
(7)实验室在保存FeCl3溶液时,常在溶液中加少量的
 溶液蒸干并灼烧,最后得到的固体主要产物是
溶液蒸干并灼烧,最后得到的固体主要产物是(8)在日常生活中经常用
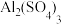 和
和 混合溶液作灭火剂,请用离子方程式表示其灭火原理:
混合溶液作灭火剂,请用离子方程式表示其灭火原理:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.现有下列物质:①HNO3②冰醋酸③氨水④Al(OH)3⑤NaHCO3(s)⑥Cu⑦氯水⑧CaCO3⑨H2CO3⑩盐酸
(1)上述物质中属于强电解质的有_____ (填序号,下同),属于弱电解质的有_____ 。
(2)下列溶液中,c(H+)由大到小排列顺序是_____ 。
①0.1mol/LHCl溶液②0.1mol/LH2SO4溶液③0.1mol/LNaOH溶液④0.1mol/LCH3COOH溶液
Ⅱ.已知室温时,0.1mol/L某一元酸HA在水中电离度为0.02%,回答下列问题:
(1)该溶液中c(H+)=_____ 。
(2)HA的电离平衡常数K=_____ 。
(1)上述物质中属于强电解质的有
(2)下列溶液中,c(H+)由大到小排列顺序是
①0.1mol/LHCl溶液②0.1mol/LH2SO4溶液③0.1mol/LNaOH溶液④0.1mol/LCH3COOH溶液
Ⅱ.已知室温时,0.1mol/L某一元酸HA在水中电离度为0.02%,回答下列问题:
(1)该溶液中c(H+)=
(2)HA的电离平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有常温下的五份溶液:
①0.01 mol·L−1 CH3COOH溶液;②0.01 mol·L−1 HCl溶液;
③pH=12的氨水; ④pH=12的NaOH溶液;
⑤0.01 mol·L−1 HCl溶液与pH=12的NaOH溶液等体积混合所得溶液。
(1)其中水的电离程度最大的是__ (填序号,下同),水的电离程度相同的是___ 。
(2)若将②③混合后所得溶液的pH=7,则消耗溶液的体积:②________ ③(填”>”“<”或”=“)。
(3)将五份溶液同等稀释10倍后,溶液的pH:①________ ②,③________ ④(填“>”“< ”或“=”)。
(4)将①④混合,若有c(CH3COO−)>c(H+),则混合溶液可能呈________ (填序号)。
A.酸性 B.碱性 C.中性
①0.01 mol·L−1 CH3COOH溶液;②0.01 mol·L−1 HCl溶液;
③pH=12的氨水; ④pH=12的NaOH溶液;
⑤0.01 mol·L−1 HCl溶液与pH=12的NaOH溶液等体积混合所得溶液。
(1)其中水的电离程度最大的是
(2)若将②③混合后所得溶液的pH=7,则消耗溶液的体积:②
(3)将五份溶液同等稀释10倍后,溶液的pH:①
(4)将①④混合,若有c(CH3COO−)>c(H+),则混合溶液可能呈
A.酸性 B.碱性 C.中性
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在一定温度下,醋酸溶液中存在电力平衡。
(1)一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图所示。

①a、b、c三点的c(H+)由小到大的顺序为___ (填字母)
②a、b、c三点中,醋酸的电离程度最大的是___ 。
③完全中和时消耗NaOH的物质的量:a___ b。(填“>”、“<”或“=”)
④测得0.1mol/L醋酸溶液中c(H+)=0.004mol/L,则该温度下醋酸的电力平衡常数数值为___ 。
(2)25℃时,部分物质的电离平衡常数如下表所示:
①CH3COOH、H2CO3、HCN的酸性由强到弱的顺序为___
②焦炉煤气中一般含有H2S和HCN气体,有的工厂在真空条件下,使用K2CO3溶液吸收煤气中的H2S和HCN气体,实现脱硫脱氰。请根据上述数据,从理论上推测同为0.1mol/L的K2CO3溶液和HCN溶液混合后,最可能发生反应的离子方程式:___ 。
(1)一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图所示。

①a、b、c三点的c(H+)由小到大的顺序为
②a、b、c三点中,醋酸的电离程度最大的是
③完全中和时消耗NaOH的物质的量:a
④测得0.1mol/L醋酸溶液中c(H+)=0.004mol/L,则该温度下醋酸的电力平衡常数数值为
(2)25℃时,部分物质的电离平衡常数如下表所示:
 | 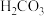 | 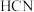 |
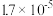 | 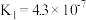 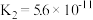 |  |
①CH3COOH、H2CO3、HCN的酸性由强到弱的顺序为
②焦炉煤气中一般含有H2S和HCN气体,有的工厂在真空条件下,使用K2CO3溶液吸收煤气中的H2S和HCN气体,实现脱硫脱氰。请根据上述数据,从理论上推测同为0.1mol/L的K2CO3溶液和HCN溶液混合后,最可能发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钠是其常见的盐[已知:25℃,Ka(CH3COOH)=1.69×10-5]。请回答下列问题:
(1)下列对于醋酸溶液和醋酸钠溶液的说法正确的是_______ (填字母,下同)。
A.加水稀释,醋酸的电离程度增大,醋酸钠的水解程度减小
B.升高温度,可以促进醋酸的电离,抑制醋酸钠的水解
C.醋酸和醋酸钠混合液中,醋酸抑制醋酸钠的水解,醋酸钠抑制醋酸的电离
(2)物质的量浓度均为0.1 mol·L-1的CH3COOH和CH3COONa溶液等体积混合(混合前后体积变化忽略不计),混合液中的下列关系式正确的是_______ 。
A.c(CH3COOH)+c(H+)=c(CH3COO-)+c(OH-)
B.c(H+)+c(Na+)=c(CH3COO-)+c(OH-)
C.c(CH3COO-)+c(CH3COOH)=0.1 mol·L-1
(3)常温时,pH=3的醋酸溶液和pH=11的NaOH溶液等体积混合后,溶液中c(Na+)_______ (填“>”“<”或“=”)c(CH3COO-),该溶液中电荷守恒表达式为_______ 。
(4)常温时,将m mol·L-1醋酸溶液和n mol·L-1 NaOH溶液等体积混合后,所得溶液的pH=7,则m与n的大小关系是m_______ (填“>”“<”或“=”,下同)n,醋酸溶液中c(H+)_______ NaOH溶液中c(OH-)。
(1)下列对于醋酸溶液和醋酸钠溶液的说法正确的是
A.加水稀释,醋酸的电离程度增大,醋酸钠的水解程度减小
B.升高温度,可以促进醋酸的电离,抑制醋酸钠的水解
C.醋酸和醋酸钠混合液中,醋酸抑制醋酸钠的水解,醋酸钠抑制醋酸的电离
(2)物质的量浓度均为0.1 mol·L-1的CH3COOH和CH3COONa溶液等体积混合(混合前后体积变化忽略不计),混合液中的下列关系式正确的是
A.c(CH3COOH)+c(H+)=c(CH3COO-)+c(OH-)
B.c(H+)+c(Na+)=c(CH3COO-)+c(OH-)
C.c(CH3COO-)+c(CH3COOH)=0.1 mol·L-1
(3)常温时,pH=3的醋酸溶液和pH=11的NaOH溶液等体积混合后,溶液中c(Na+)
(4)常温时,将m mol·L-1醋酸溶液和n mol·L-1 NaOH溶液等体积混合后,所得溶液的pH=7,则m与n的大小关系是m
您最近一年使用:0次



