按要求回答下列问题:
(1)研究发现,在CO2低压合成甲醇反应CO2+3H2=CH3OH+H2O中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Co基态原子核外电子排布为___________ ;元素Mn与O中,第一电离能较大的是___________ ,基态原子核外未成对电子数较多的是___________ 。
(2)我国科学家成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl。
①氮原子的价层电子排布图为___________ 。
②元素的基态的气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1),第二周期部分元素的E1变化趋势如图所示。
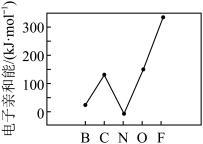
其中除氮元素外,其他元素的E1自左而右依次增大的原因是___________ ,氮元素E1呈现异常的原因是___________ 。
(1)研究发现,在CO2低压合成甲醇反应CO2+3H2=CH3OH+H2O中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。Co基态原子核外电子排布为
(2)我国科学家成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl。
①氮原子的价层电子排布图为
②元素的基态的气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1),第二周期部分元素的E1变化趋势如图所示。

其中除氮元素外,其他元素的E1自左而右依次增大的原因是
19-20高二·湖北咸宁·期末 查看更多[10]
湖北省咸宁市嘉鱼县第一中学2019-2020学年高二下学期期末考试化学试题(已下线)考点33 原子结构与性质-备战2022年高考化学一轮复习考点帮(全国通用)广东省东莞市新世纪英才学校2021-2022学年高二上学期第一次教学质量检测化学试题(已下线)第1章 章末综合测评B-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修1)(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)第一章 本章达标检测2河北省石家庄市第23中学2022-2023学年高二上学期第一次月考化学试题常州市武进区礼嘉中学2021-2022学年高二下学期第二次阶段测试化学试题湖南省衡阳县第四中学 2022-2023学年高二下学期开学摸底考试(平行班)化学试题(已下线)第一章 原子结构与性质(B卷)
更新时间:2022-10-20 14:16:38
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】太阳能电池的发展已经进入了第三代。第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGS(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池。亚铜离子(Cu+)基态时的价电子排布式表示为________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,表中所列字母分别代表一种元素。试回答下列问题:
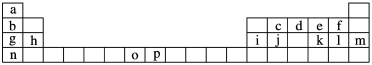
(1)①依据元素周期表的分区,元素c属于___________ 区。
②基态e离子的核外电子排布式是___________ 。
③基态g原子核外能量不同的电子有___________ 种。
④元素1的基态原子的核外电子共占据___________ 个原子轨道。
(2)将c、d、e、f四种元素按电负性由小到大的顺序排列___________ (用元素符号表示)。
(3)元素a和c可以构成多种化合物,苯就是其中的一种。以下有关苯分子中化学键的描述正确的是___________
(4)下列有关分子的空间结构,描述正确的是___________
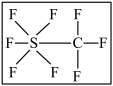
(5)据报道,大气中存在一种潜在的温室气体 (结构如图),虽然其数量有限,但它是已知气体中吸热最高的。关于
(结构如图),虽然其数量有限,但它是已知气体中吸热最高的。关于 的说法正确的是___________
的说法正确的是___________
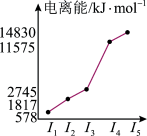
(6)表中所列的某主族元素的电离能情况如图所示,则该元素是___________ (填元素符号)。
(7)判断下列关于相关元素及元素组成的化合物的说法是否正确。(A—正确;B—错误)。
①玻璃纤维是合成纤维的一种,属于高分子材料。___________
②二氧化硫具有氧化性,可用于漂白纸浆。___________
③CaO能与 反应,可作工业废气的脱硫剂。
反应,可作工业废气的脱硫剂。___________
④制 时,用水或NaOH溶液吸收尾气。
时,用水或NaOH溶液吸收尾气。___________
(8)o、p两元素的部分电离能数据列于下表:
比较两元素的 、
、 可知,气态
可知,气态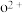 再失去一个电子比气态
再失去一个电子比气态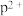 再失去一个电子难,其原因是
再失去一个电子难,其原因是___________

(1)①依据元素周期表的分区,元素c属于
②基态e离子的核外电子排布式是
③基态g原子核外能量不同的电子有
④元素1的基态原子的核外电子共占据
(2)将c、d、e、f四种元素按电负性由小到大的顺序排列
(3)元素a和c可以构成多种化合物,苯就是其中的一种。以下有关苯分子中化学键的描述正确的是___________
A.每个碳原子的一个 杂化轨道参与形成大π键 杂化轨道参与形成大π键 |
| B.每个碳原子的未参加杂化的2p轨道形成大π键 |
C.碳原子的3个 杂化轨道与其他碳原子形成2个σ键和1个π键 杂化轨道与其他碳原子形成2个σ键和1个π键 |
| D.碳原子的未参加杂化的2p轨道与其他碳原子的2p轨道成键 |
(4)下列有关分子的空间结构,描述正确的是___________
A. 分子中N原子处在3个H原子所组成的三角形的中心 分子中N原子处在3个H原子所组成的三角形的中心 |
B. 分子中C原子处在4个Cl原子所组成的四面体的中心 分子中C原子处在4个Cl原子所组成的四面体的中心 |
C. 分子中O原子处在2个H原子所连成的直线的中央 分子中O原子处在2个H原子所连成的直线的中央 |
D. 分子中P原子处在3个Cl原子所组成的三角形的中心 分子中P原子处在3个Cl原子所组成的三角形的中心 |
(5)据报道,大气中存在一种潜在的温室气体
 (结构如图),虽然其数量有限,但它是已知气体中吸热最高的。关于
(结构如图),虽然其数量有限,但它是已知气体中吸热最高的。关于 的说法正确的是___________
的说法正确的是___________
| A.分子中有σ键也有π键 |
B. 是s-pσ键 是s-pσ键 |
| C.分子中不是所有原子都满足8电子稳定结构 |
D.0.1mol 分子中电子数为8mol 分子中电子数为8mol |
(6)表中所列的某主族元素的电离能情况如图所示,则该元素是

(7)判断下列关于相关元素及元素组成的化合物的说法是否正确。(A—正确;B—错误)。
①玻璃纤维是合成纤维的一种,属于高分子材料。
②二氧化硫具有氧化性,可用于漂白纸浆。
③CaO能与
 反应,可作工业废气的脱硫剂。
反应,可作工业废气的脱硫剂。④制
 时,用水或NaOH溶液吸收尾气。
时,用水或NaOH溶液吸收尾气。(8)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p |
 | 717 | 759 |
 | 1509 | 1561 |
 | 3248 | 2957 |
 、
、 可知,气态
可知,气态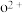 再失去一个电子比气态
再失去一个电子比气态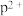 再失去一个电子难,其原因是
再失去一个电子难,其原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】生物质能是一种洁净、可再生能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Cu2+的核外电子排布式:_______ 。
(2)根据等电子原理,写出CO分子的结构式:_______ ,SCN-的一种等电子体分子的化学式:_______
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醛分子中碳原子轨道的杂化类型为_______ ;
②甲醛分子的立体构型是_______ ;
③1 mol甲醛分子中σ键的数目为_______ 。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Cu2+的核外电子排布式:
(2)根据等电子原理,写出CO分子的结构式:
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醛分子中碳原子轨道的杂化类型为
②甲醛分子的立体构型是
③1 mol甲醛分子中σ键的数目为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)基态Mn原子核外有___________ 种运动状态不同的电子。
(2)基态镁原子核外M层电子的自旋状态___________ (填“相同”或“相反”)。
(3)基态Ge原子有___________ 个未成对电子。
(4)镍元素基态原子的电子排布式为___________ 。
(5)氮原子价层电子的轨道表达式(电子排布图)为___________ 。
(6)基态 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为___________ 。
(7)基态K原子中,核外电子占据的最高能层的符号是___________ 。
(8)Se的基态原子中电子占据的原子轨道总数为___________ 。
(1)基态Mn原子核外有
(2)基态镁原子核外M层电子的自旋状态
(3)基态Ge原子有
(4)镍元素基态原子的电子排布式为
(5)氮原子价层电子的轨道表达式(电子排布图)为
(6)基态
 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为(7)基态K原子中,核外电子占据的最高能层的符号是
(8)Se的基态原子中电子占据的原子轨道总数为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】氧原子价电子层上的电子可以进行重排以便提供一个空轨道与氮原子形成配位键,该氧原子重排后的价电子排布图为_______ ,电子重排后的氧原子能量有所升高,原因是不符合_______ (填“泡利原理”或“洪特规则”)。
您最近一年使用:0次
【推荐3】I.雄黄( )、雌黄(
)、雌黄( )均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:
)均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:
(1)基态硫原子核外电子的运动轨道数有_______ 种;有___________ 种能量不同的电子;
(2)基态砷原子的价层电子的轨道表示式为___________ 。
(3)S和As比较,电负性较大的是___________
(4)As元素的第一电离能___________ Se元素的第一电离能(填“大于”“小于”或“等于”),原因是_______________________________ 。
II.目前已发现,在元素周期表中某些元素与右下方的主族元素的有些性质相似,这种相似性被称为对角线规则。据此回答下列问题:
(5)铍的最高价氧化物对应水化物的化学式是________ ,属于两性化合物,证明这一结论的有关离子方程式为__________________________ 、________________ 。
(6)若已知反应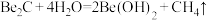 ,则
,则 与足量强碱溶液反应的离子方程式为
与足量强碱溶液反应的离子方程式为______________________ 。
(7)科学家证实, 属于共价化合物,请设计一个简单实验证明,方法是
属于共价化合物,请设计一个简单实验证明,方法是________________ 。用电子式表示 的形成过程:
的形成过程:__________
 )、雌黄(
)、雌黄( )均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:
)均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:(1)基态硫原子核外电子的运动轨道数有
(2)基态砷原子的价层电子的轨道表示式为
(3)S和As比较,电负性较大的是
(4)As元素的第一电离能
II.目前已发现,在元素周期表中某些元素与右下方的主族元素的有些性质相似,这种相似性被称为对角线规则。据此回答下列问题:
(5)铍的最高价氧化物对应水化物的化学式是
(6)若已知反应
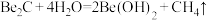 ,则
,则 与足量强碱溶液反应的离子方程式为
与足量强碱溶液反应的离子方程式为(7)科学家证实,
 属于共价化合物,请设计一个简单实验证明,方法是
属于共价化合物,请设计一个简单实验证明,方法是 的形成过程:
的形成过程:
您最近一年使用:0次
【推荐1】完成下列问题:
(1)N、O、Mg、Al、S、Fe是常见的六种元素,按要求回答下列问题:
①Fe位于元素周期表第_______ 周期第_______ 族。
②基态N原子核外电子排布式为_______ ;基态O原子核外有_______ 种运动状态的电子。
③基态S原子核外电子占据的最高能级的电子云轮廓图为_______ 形。
④Mg、Al两种元素中第一电离能较大的是_______ (填元素符号),原因为_______ 。
(2)几种元素的电负性数据如下表:
①AlBr3的熔点_______ AlF3的熔点(填“大于”、“小于”或“等于”),原因是_______ 。
②根据同一主族元素电负性递变规律,预测碘元素的电负性数值范围为_______ 。
(1)N、O、Mg、Al、S、Fe是常见的六种元素,按要求回答下列问题:
①Fe位于元素周期表第
②基态N原子核外电子排布式为
③基态S原子核外电子占据的最高能级的电子云轮廓图为
④Mg、Al两种元素中第一电离能较大的是
(2)几种元素的电负性数据如下表:
| O | F | Al | Br | …… |
| 3.5 | 4.0 | 1.5 | 2.8 | …… |
②根据同一主族元素电负性递变规律,预测碘元素的电负性数值范围为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】第三代半导体中,碳化硅(SiC)和氮化镓(GaN)是核心半导体。它们具有更宽的禁带宽度、更高的导热率、更高的抗辐射能力、更大的电子饱和漂移速率等特性。
(1)基态Ga原子的价电子排布式为____ 。
(2)晶体硅、碳化硅、金刚石三种晶体的熔点由高到低的顺序为____ 。
(3)氮化镓不存在于自然界中,只能通过人工合成来制备,反应为GaCl3+NH3 GaN+3HCl。
GaN+3HCl。
①GaCl3的熔点为77.9℃,其晶体类型为____ ,它在高温时会形成双聚分子(GaCl3)2,该双聚分子的结构式为____ 。GaF3的熔点为1000℃,则将GaF3熔化时,被破坏的作用力是____ 。
②上述反应涉及的元素中,电负性最小的是____ (填元素符号,下同),第一电离能最大的是____ 。
(1)基态Ga原子的价电子排布式为
(2)晶体硅、碳化硅、金刚石三种晶体的熔点由高到低的顺序为
(3)氮化镓不存在于自然界中,只能通过人工合成来制备,反应为GaCl3+NH3
 GaN+3HCl。
GaN+3HCl。①GaCl3的熔点为77.9℃,其晶体类型为
②上述反应涉及的元素中,电负性最小的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】铜元素的化合物种类很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)CuSO4和Cu(NO3)2是自然界中重要的铜盐。
① CuSO4和Cu(NO3)2中阳离子的基态外围电子排布式为_______________ 。
② S、O、N三种元素的第一电离能由大到小为_____________ 。
③ CuSO4的熔点为560℃,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因是________ 。
(2)硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如图所示。请回答下列问题:

① 配合物A中N原子的轨道杂化类型为__________ 。
② 1 mol配合物A含有σ键的数目为_____________ 。
(3)CuFeS2的晶胞如图1所示,CuFeS2的晶胞中每个Cu原子与__ 个S原子相连

(1)CuSO4和Cu(NO3)2是自然界中重要的铜盐。
① CuSO4和Cu(NO3)2中阳离子的基态外围电子排布式为
② S、O、N三种元素的第一电离能由大到小为
③ CuSO4的熔点为560℃,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因是
(2)硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如图所示。请回答下列问题:

① 配合物A中N原子的轨道杂化类型为
② 1 mol配合物A含有σ键的数目为
(3)CuFeS2的晶胞如图1所示,CuFeS2的晶胞中每个Cu原子与

您最近一年使用:0次



