16. 工业上采用高浓度含砷废水制取As
2O
3。工艺流程如下:
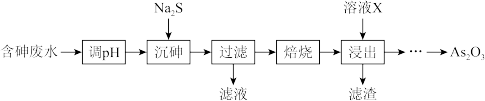
已知含砷废水中砷元素以+3价的形式存在。不同pH时,三价砷的物种分布如下图所示:
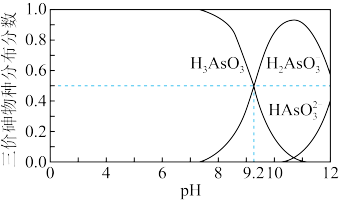
(1)H
3AsO
3第一步电离方程式H
3AsO
3
H
2AsO

+H
+的电离常数为K
a1,则pK
a1=
_______(pK
a1=-lgK
a1),“调pH”时,控制溶液的pH=6,“沉砷”时会生成As
2S
3沉淀。写出“沉砷”时反应的离子方程式:
_______。
(2)“沉砷”时会发生副反应:As
2S
3(s)+3S
2-(aq)

2AsS

(aq),从而降低砷元素的沉淀率。为减少副反应的发生,采取的方法是加入Na
2S的同时加入少量FeSO
4,生成的As
2S
3沉淀中会混有FeS。加入少量FeSO
4能抑制副反应的原因是
_______。
(3)“焙烧”含少量FeS的As
2S
3可以得到As
2O
3和Fe
2O
3的混合物。As
2O
3是一种酸性氧化物,选择合适的溶液X,将砷元素可以从混合物中浸出。写出“浸出”反应的离子方程式:
_______。
(4)保持反应温度和溶液X的浓度不变,为提高砷元素浸出的速率,可以采取的方法有
_______(填两条)。
(5)利用反应AsO

+2I
-+2H
+=AsO

+I
2+H
2O 可测定As(Ⅴ)的含量。取50 mL含As(Ⅴ)样品,加入硫酸使溶液呈酸性,加入过量的KI。用0.1250mol·L
-1的Na
2S
2O
3溶液滴定析出的碘,用去24.00 mL。试计算试样中As(Ⅴ)的含量(以g·L
-1表示)
_______。(已知:2Na
2S
2O
3+I
2=Na
2S
4O
6+2NaI)