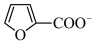
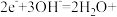下列判断正确的是


| A.图1可表示电解NaCl溶液过程中,产生氢气体积(标准状况)与转移电子物质的量的关系曲线 |
| B.图2可表示常温下0.1mol/L盐酸滴加到40mL 0.1mol/L NaOH溶液的滴定曲线 |
C.高温下能自发进行的反应CO2(g)+H2(g) CO(g)+H2O(g)的能量变化如图3所示,则该反应的ΔS>0 CO(g)+H2O(g)的能量变化如图3所示,则该反应的ΔS>0 |
D.图4可表示反应N2(g)+3H2(g) 2NH3(g),在t1时刻扩大容器体积时,v逆随时间的变化曲线 2NH3(g),在t1时刻扩大容器体积时,v逆随时间的变化曲线 |
更新时间:2022-10-27 09:26:05
|
相似题推荐
【推荐1】SO3通常通过SO2的氧化反应制得。某实验探究小组在实验室中模拟在不同条件下制备SO3的反应,在3个初始温度均为T℃的密闭容器中发生反应:2SO2(g)+O2(g)  2SO3(g) ΔH<0,实验数据如下。下列说法正确的是
2SO3(g) ΔH<0,实验数据如下。下列说法正确的是
 2SO3(g) ΔH<0,实验数据如下。下列说法正确的是
2SO3(g) ΔH<0,实验数据如下。下列说法正确的是| 容器编号 | 容器类型 | 初始体积 | 起始物质的量/mol | 平衡时SO3物质的量/mol | ||
| SO2 | O2 | SO3 | ||||
| Ⅰ | 恒温恒容 | 1.0L | 2 | 1 | 0 | 1.6 |
| Ⅱ | 绝热恒容 | 1.0L | 2 | 1 | 0 | a |
| Ⅲ | 恒温恒压, | 0.5L | 0 | 0 | 1 | b |
| A.a<1.6 |
| B.b>0.8 |
| C.平衡时v正(SO2)的大小关系:v(I)<v(II) |
| D.若起始时向容器I中充入1.0 mol SO2(g)、0.20 mol O2(g)和4.0 mol SO3(g),则反应将向正反应方向进行 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】我国学者结合实验与计算机模拟结果,研究了均相NO-CO的反应历程,该反应经历了I、II、III三个过渡态。图中显示的是反应路径中每一阶段内各驻点的能量相对于此阶段内反应物能量的能量之差。下列说法正确的是
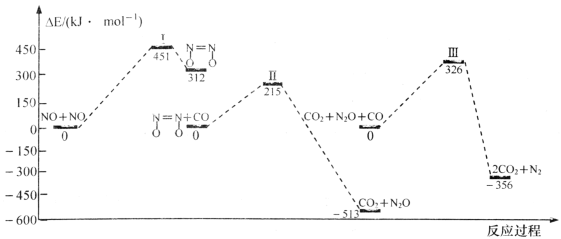

A.N2O比 更容易与CO发生反应 更容易与CO发生反应 |
| B.整个反应分为三个基元反应阶段,其中第一个反应阶段活化能最大 |
| C.2NO(g)+2CO(g)⇌N2(g)+2CO2(g) ∆H<0 |
| D.其他条件不变,增大压强或使用催化剂均可以增大反应速率,提高反应物的转化率 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】下面是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图象,其中图象和实验结论表达均正确的是
 |  |
| 图①mA(g)+nB(g)⇌pC(g) | 图②2X(g)⇌Y(g) |
 | 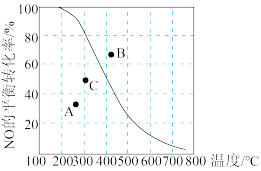 |
| 图③CO(g)+2H2(g)⇌CH3OH(g) ∆H<0 | 图④2NO(g)+O2(g)⇌2NO2(g) |
| A.图①若m+n=p,则a曲线一定使用了催化剂 |
B.图②是在一定条件下,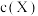 随时间t的变化,正反应 随时间t的变化,正反应 ,M点正反应速率<N点逆反应速率 ,M点正反应速率<N点逆反应速率 |
C.图③是在恒温恒容的密闭容器中,按不同投料比充入CO(g)和 (g)进行反应,若平衡时CO(g)和 (g)进行反应,若平衡时CO(g)和 (g)的转化率相等,则 (g)的转化率相等,则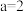 |
| D.图④中曲线表示一定压强下NO平衡转化率随温度的变化,A、B、C三点表示不同温度、压强下NO的平衡转化率,压强最小的是A点,化学平衡常数最小的是B点 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】下列有关化学反应的方向及判据的说法不正确的是
A.反应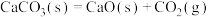 能否自发进行,主要由 能否自发进行,主要由 决定 决定 |
| B.焓变或熵变均可以单独作为反应自发性的判据 |
C. 、 、 的反应在任何温度下部能自发进行 的反应在任何温度下部能自发进行 |
| D.冰在室温下自动融化成水,是因为体系混乱度降低 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】以白云石(CaCO3·MgCO3)为原料冶炼金属镁的反应工艺涉及以下两个反应:
①CaCO3·MgCO3 MgO·CaO+2CO2↑;②2(MgO·CaO)+Si
MgO·CaO+2CO2↑;②2(MgO·CaO)+Si 2CaO·SiO2+2Mg↑
2CaO·SiO2+2Mg↑
对①②两个反应的说法正确的是
①CaCO3·MgCO3
 MgO·CaO+2CO2↑;②2(MgO·CaO)+Si
MgO·CaO+2CO2↑;②2(MgO·CaO)+Si 2CaO·SiO2+2Mg↑
2CaO·SiO2+2Mg↑对①②两个反应的说法正确的是
| A.在敞口容器中有利于反应①的进行 |
| B.反应①能进行,说明该反应△H<0 |
| C.在真空条件下有利于反应②的进行 |
| D.反应②能进行,说明Si的还原性比Mg强 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】科学家采用电渗析法提纯乳清(富含NaCl的蛋白质),有价值的蛋白质回收率达到98%,工作原理如图所示:

下列说法错误的是

下列说法错误的是
| A.膜1为阴离子交换膜,膜2为阳离子交换膜 |
| B.膜1、膜2孔径不大于半透膜孔径 |
| C.a极的电极反应式为2H2O+2e−=2OH−+H2↑ |
| D.每转移2mol电子,理论上乳清质量减少58.5g |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】电Fenton法是用于水体中有机污染物降解的高级氧化技术,反应原理如图所示。电解产生的H2O2与Fe2+发生反应生成的羟基自由基(•OH)能氧化降解有机污染物。下列说法错误的是


| A.电源的A极为正极 |
| B.与电源B极相连的电极反应式为:H2O-e-=H++•OH |
| C.H2O2与Fe2+发生的反应方程式为:H2O2+Fe2+=Fe(OH)2++•OH |
| D.每消耗2.24LO2(标准状况),整个电解池中理论上可产生的•OH为0.2mol |
您最近一年使用:0次

 变成
变成

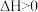 、
、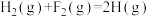
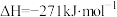

 的装置,装置如图所示.下列有关说法不正确的是
的装置,装置如图所示.下列有关说法不正确的是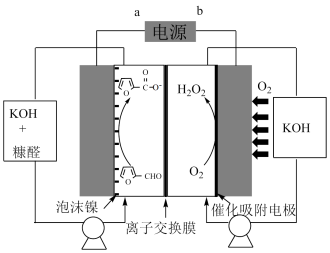
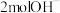 时,参加反应的
时,参加反应的 在标准状况下的体积为
在标准状况下的体积为
 -
-