请回答与HCl的制法和性质探究的相关问题。
(1)实验室用食盐晶体与浓硫酸在微热条件下反应制取氯化氢气体,反应的化学方程式为:_______ 。
(2)氯化氢气体的发生装置应该选择下图A、B、C中的_______ (填装置的编号)。实验室常用装置D来收集氯化氢,则收集氯化氢时,气体从_______ 管(填“a”或“b”)进入。用水吸收多余的氯化氢气体时,不能选择的装置①~⑤中的_______ (填装置的编号)。

(3)某同学欲证明盐酸与氯化氢气体性质不同,他向X、Y、Z三支洁净试管里各放一片干燥的蓝色石蕊试纸,然后向试管X中加入盐酸,试纸显_______ 色;往试管Y中通入干燥的氯化氢气体,试纸显_______ 色,这时他认为由此还不能得出满意的结论,于是向试管Z中加入化学式为_______ 的物质。
(4)写出工业合成氯化氢的化学方程式:_______ 。
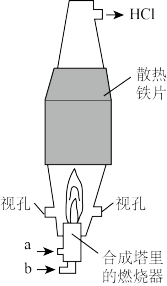
(5)如图所示,为防止污染空气,在刚开始合成时,应先从_______ (填“a”或“b”)口通入_______ (填电子式)气体,并使该气体过量。
(1)实验室用食盐晶体与浓硫酸在微热条件下反应制取氯化氢气体,反应的化学方程式为:
(2)氯化氢气体的发生装置应该选择下图A、B、C中的

(3)某同学欲证明盐酸与氯化氢气体性质不同,他向X、Y、Z三支洁净试管里各放一片干燥的蓝色石蕊试纸,然后向试管X中加入盐酸,试纸显
(4)写出工业合成氯化氢的化学方程式:
(5)如图所示,为防止污染空气,在刚开始合成时,应先从

更新时间:2022-10-31 17:03:44
|
相似题推荐
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐1】(1)指出如图实验装置中的错误之处(加热装置中烧杯底部已垫有石棉网)
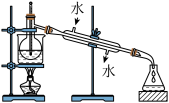
①___ ;②___ 。
(2)图是某学生的过滤操作示意图,其操作不规范的是___ 。
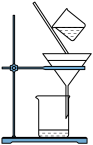
a.漏斗下口尖端未紧靠烧杯壁 b.玻璃棒有引流 作用
c.将滤纸湿润,使其紧贴漏斗壁 d.滤纸边缘低于漏斗口边缘
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度

①
(2)图是某学生的过滤操作示意图,其操作不规范的是

a.漏斗下口尖端未紧靠烧杯壁 b.玻璃棒有引流 作用
c.将滤纸湿润,使其紧贴漏斗壁 d.滤纸边缘低于漏斗口边缘
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐2】用下列仪器的编号回答问题
①容量瓶 ②蒸馏烧瓶 ③分液漏斗 ④量筒 ⑤烧杯
(1)加热时必须垫石棉网的有_______ ,
(2)使用时必须检查是否漏水的有_______ 。
①容量瓶 ②蒸馏烧瓶 ③分液漏斗 ④量筒 ⑤烧杯
(1)加热时必须垫石棉网的有
(2)使用时必须检查是否漏水的有
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
解题方法
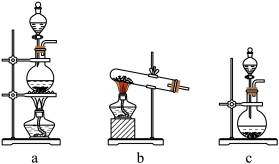
【推荐1】某小组同学用如图所示装置制取氨气并验证氨气的性质。请回答:
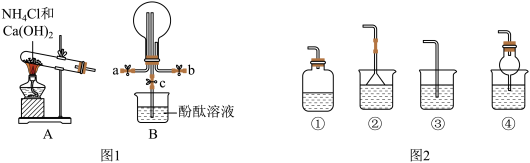
(1)实验室制取氨气的化学方程式是______ 。欲制取4.48L(标准状况) ,至少需称取
,至少需称取 的质量
的质量______ g。
(2)用图1装置B收集氨气时,应选择氨气的进气口是______ (选填“a”或“b”)。
(3)打开图1装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是______ ,______ 。
(4)把蘸有浓盐酸的玻璃棒靠近集满氨气的试管口,观察到的实验现象是______ 。
(5)下列不能用于干燥氨气的是______(填标号,下同)。
(6)为防止环境污染,图2装置(盛放的液体均为水)可用于吸收多余氨气的是______ (填序号)。
(7)生石灰与水反应生成 并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用如图的气体发生装置是
并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用如图的气体发生装置是______ 。

(1)实验室制取氨气的化学方程式是
 ,至少需称取
,至少需称取 的质量
的质量(2)用图1装置B收集氨气时,应选择氨气的进气口是
(3)打开图1装置B中的止水夹c,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是
(4)把蘸有浓盐酸的玻璃棒靠近集满氨气的试管口,观察到的实验现象是
(5)下列不能用于干燥氨气的是______(填标号,下同)。
| A.浓硫酸 | B.氢氧化钠 | C.五氧化二磷 | D.碱石灰 |
(7)生石灰与水反应生成
 并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用如图的气体发生装置是
并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用如图的气体发生装置是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
解题方法
【推荐2】如图所示的仪器和装置,请回答有关问题:
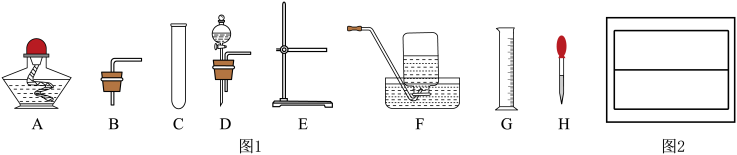
(1)若用高锰酸钾制取氧气,该反应的化学方程式是_____ ,其气体发生装置可选择上图中_____ (填标号)组合;
(2)实验室也可以用过氧化氢溶液来制取氧气,现要配制 溶质质量分数为
溶质质量分数为 的过氧化氢溶液,需要
的过氧化氢溶液,需要 的过氧化氢溶液
的过氧化氢溶液_____  ,若用
,若用 来量取
来量取 的过氧化氢溶液时,仰视读数,则配得的溶液中溶质质量分数
的过氧化氢溶液时,仰视读数,则配得的溶液中溶质质量分数_____ (填“偏大”或“偏小”);
(3)将配制好的溶液装入试剂瓶中,贴好标签。请在如图2所示的标签内填入试剂瓶所要贴的标签内容_____ 。

(1)若用高锰酸钾制取氧气,该反应的化学方程式是
(2)实验室也可以用过氧化氢溶液来制取氧气,现要配制
 溶质质量分数为
溶质质量分数为 的过氧化氢溶液,需要
的过氧化氢溶液,需要 的过氧化氢溶液
的过氧化氢溶液 ,若用
,若用 来量取
来量取 的过氧化氢溶液时,仰视读数,则配得的溶液中溶质质量分数
的过氧化氢溶液时,仰视读数,则配得的溶液中溶质质量分数(3)将配制好的溶液装入试剂瓶中,贴好标签。请在如图2所示的标签内填入试剂瓶所要贴的标签内容
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐3】请选择适当的化学试剂和实验用品,用下图所示的装置进行实验,验证过氧化钠可在呼吸面具和潜水艇中做供氧剂。

(1)A装置中分别加入大理石和稀盐酸,其中仪器a的名称是_______ 。
(2)B装置中加入饱和NaHCO3溶液的目的是_______ 。
(3)写出C中发生反应的化学方程式_______ 。
(4)为了保证F中收集到较纯的气体,装置D中应加入的下列试剂中的_______ (填序号)。
①浓硫酸 ②NaOH溶液
(5)F中得到的气体是_______ (填化学式)。

(1)A装置中分别加入大理石和稀盐酸,其中仪器a的名称是
(2)B装置中加入饱和NaHCO3溶液的目的是
(3)写出C中发生反应的化学方程式
(4)为了保证F中收集到较纯的气体,装置D中应加入的下列试剂中的
①浓硫酸 ②NaOH溶液
(5)F中得到的气体是
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
【推荐1】“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为Na2CO3)吸收烟气中的 SO2,得到亚硫酸钠(Na2SO3)粗品。其流程如下:
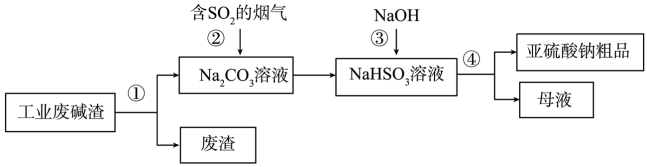
(1)为加快工业废碱渣中 Na2CO3的溶解,可采取的措施是_____ (写出一种即可)。
(2)上述流程中,加入NaOH 后,发生反应的化学方程式为_____ 。
(3)亚硫酸钠粗品中含有少量Na2SO4,原因是_____ 。
(4)设计实验证明亚硫酸钠粗品含有少量 Na2SO4的方案是:在一支试管中,加入少量 亚硫酸钠粗品,用适量蒸馏水溶解,_____ ,出现白色沉淀,则证明含有 Na2SO4。

(1)为加快工业废碱渣中 Na2CO3的溶解,可采取的措施是
(2)上述流程中,加入NaOH 后,发生反应的化学方程式为
(3)亚硫酸钠粗品中含有少量Na2SO4,原因是
(4)设计实验证明亚硫酸钠粗品含有少量 Na2SO4的方案是:在一支试管中,加入少量 亚硫酸钠粗品,用适量蒸馏水溶解,
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
解题方法
【推荐2】肼(N2H4)是氮和氢形成的一种化合物,易溶于水。工业上利用尿素法生产肼,同时得到副产品十水合碳酸钠,其工艺流程如图:
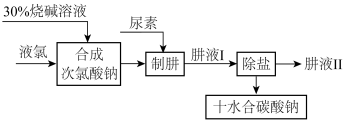
制肼过程的反应为:CO(NH2)2(尿素)+NaClO+2NaOH=N2H4+Na2CO3+NaCl+H2O
(1)实验室若配制30%烧碱溶液,所需的玻璃仪器除玻璃棒外,还有______ (填标号)。
A.漏斗 B.烧杯 C.烧瓶 D.量筒
(2)已知:Cl2+H2O=HCl+HClO,请推测C12与NaOH溶液发生反应的化学方程式:____ 。从后续反应过程来看,若要使原料不浪费,合成次氯酸钠时投入的液氯与烧碱的质量之比为71:_________ 。
(3)实验室中,欲从母液中分离出十水合碳酸钠晶体。可采用的操作依次为________ 。(填标号)
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
(4)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等。请写出肼除氧时发生反应的化学方程式:______________ 。

制肼过程的反应为:CO(NH2)2(尿素)+NaClO+2NaOH=N2H4+Na2CO3+NaCl+H2O
(1)实验室若配制30%烧碱溶液,所需的玻璃仪器除玻璃棒外,还有
A.漏斗 B.烧杯 C.烧瓶 D.量筒
(2)已知:Cl2+H2O=HCl+HClO,请推测C12与NaOH溶液发生反应的化学方程式:
(3)实验室中,欲从母液中分离出十水合碳酸钠晶体。可采用的操作依次为
A.蒸馏 B.蒸发 C.灼烧 D.过滤 E.冷却结晶
(4)肼具有很好的还原性,且氧化产物无污染,故可用于除去锅炉等设备供水中的溶解氧等。请写出肼除氧时发生反应的化学方程式:
您最近一年使用:0次




