已知水的电离平衡曲线如图所示:
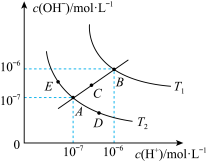
试回答下列问题:
(1)图中
_______  (用“>”、“<”、“=”回答)
(用“>”、“<”、“=”回答)
(2)图中五点的 间的关系是
间的关系是_______ 。
(3)若从A点到E点,可采用的措施是_______ 。
a.升温 b.加入少量的盐酸 c.加入少量的NaOH溶液
(4)点E对应的温度下,将 的NaOH溶液与
的NaOH溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则NaOH溶液与
,则NaOH溶液与 溶液的体积比为
溶液的体积比为_______ 。
(5)点B对应的温度下,若100体积 的某强酸溶液与1体积
的某强酸溶液与1体积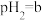 的某强碱溶液混合后溶液呈中性,则混合前,该强酸的
的某强碱溶液混合后溶液呈中性,则混合前,该强酸的 与强碱的
与强碱的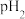 之间应满足的关系是
之间应满足的关系是_______ 。
(6)写出用pH试纸测溶液pH的操作_______ 。

试回答下列问题:
(1)图中

 (用“>”、“<”、“=”回答)
(用“>”、“<”、“=”回答)(2)图中五点的
 间的关系是
间的关系是(3)若从A点到E点,可采用的措施是
a.升温 b.加入少量的盐酸 c.加入少量的NaOH溶液
(4)点E对应的温度下,将
 的NaOH溶液与
的NaOH溶液与 的
的 溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的 ,则NaOH溶液与
,则NaOH溶液与 溶液的体积比为
溶液的体积比为(5)点B对应的温度下,若100体积
 的某强酸溶液与1体积
的某强酸溶液与1体积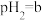 的某强碱溶液混合后溶液呈中性,则混合前,该强酸的
的某强碱溶液混合后溶液呈中性,则混合前,该强酸的 与强碱的
与强碱的 之间应满足的关系是
之间应满足的关系是(6)写出用pH试纸测溶液pH的操作
更新时间:2022-11-10 10:13:51
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】完成下列个小题
(1)写出下列物质的电离式:
①NaHCO3:_____________________
②NH3·H2O :_____________________
(2)已知H+(aq)+OH-(aq)=H2O(l) ΔH=−57.3 kJ∙mol−1,用 Ba(OH)2配成稀溶液与足量稀硝酸反应,请写出它们反应的中和热的热化学方程式为_____________________
(3)25℃时,pH=2的溶液中c(OH-)=__________ 该溶液中c水(H+)=___________ ;取该溶液1mL将其稀释为1000mL,则稀释后的pH=_________ 。
(4)已知120℃,Kw=1×10−11 ;在该温度下,取pH=3的H2SO4溶液与pH=8的NaOH溶液等体积混合,则混合液的pH____ 7(填“>”、“=”、“ < ”)
(5)已知:C(s)+H2O(g) = CO(g)+H2(g) ΔH=a kJ∙mol−1
2C(s)+O2(g)=2CO(g) ΔH=-220 kJ∙mol−1
H −H、O=O和O −H键的键能分别为436 kJ∙mol−1、496 kJ∙mol−1和462 kJ∙mol−1,则a的值为_____
(1)写出下列物质的电离式:
①NaHCO3:
②NH3·H2O :
(2)已知H+(aq)+OH-(aq)=H2O(l) ΔH=−57.3 kJ∙mol−1,用 Ba(OH)2配成稀溶液与足量稀硝酸反应,请写出它们反应的中和热的热化学方程式为
(3)25℃时,pH=2的溶液中c(OH-)=
(4)已知120℃,Kw=1×10−11 ;在该温度下,取pH=3的H2SO4溶液与pH=8的NaOH溶液等体积混合,则混合液的pH
(5)已知:C(s)+H2O(g) = CO(g)+H2(g) ΔH=a kJ∙mol−1
2C(s)+O2(g)=2CO(g) ΔH=-220 kJ∙mol−1
H −H、O=O和O −H键的键能分别为436 kJ∙mol−1、496 kJ∙mol−1和462 kJ∙mol−1,则a的值为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】某科研小组为研究电化学原理,设计如图所示装置。回答下列问题:
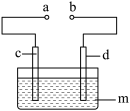
(1)若a和b不相连,c是铜片,d是锌片,m是稀硫酸,则锌片上的现象是_______ ,常温下,pH=3的稀硫酸溶液中,水电离出的c(H+)浓度为______ mol/L。
(2)若a和b用导线相连:
①c是石墨电极,d是铜片,m是硝酸银溶液,则原电池正极的电极反应式为_______ 。
②c、d均是Pt电极,m是NaOH稀溶液,分别向两极通入CH4和O2,通入CH4一极的电极反应式是_______ 。
(3)若a和b分别连接直流电源的两极:
①c,d是石墨电极,m是NaCl溶液,向溶液中滴加几滴酚酞溶液。实验开始后c极周围溶液首先出现红色,则b连接直流电源的_______ (填“正极”或“负极”),通电时总反应的离子方程式是_______ ,检验d极气体产物可以选用的试纸是_______ (填字母)。
A.干燥的红色石蕊试纸 B.干燥的蓝色石蕊试纸
C.湿润的淀粉-KI试纸 D.干燥的淀粉-KI试纸
②c,d分别是石墨电极和铜电极,m是NaOH浓溶液,通过反应: 可制得纳米级Cu2O。阳极的电极反应式是
可制得纳米级Cu2O。阳极的电极反应式是_______ 。

(1)若a和b不相连,c是铜片,d是锌片,m是稀硫酸,则锌片上的现象是
(2)若a和b用导线相连:
①c是石墨电极,d是铜片,m是硝酸银溶液,则原电池正极的电极反应式为
②c、d均是Pt电极,m是NaOH稀溶液,分别向两极通入CH4和O2,通入CH4一极的电极反应式是
(3)若a和b分别连接直流电源的两极:
①c,d是石墨电极,m是NaCl溶液,向溶液中滴加几滴酚酞溶液。实验开始后c极周围溶液首先出现红色,则b连接直流电源的
A.干燥的红色石蕊试纸 B.干燥的蓝色石蕊试纸
C.湿润的淀粉-KI试纸 D.干燥的淀粉-KI试纸
②c,d分别是石墨电极和铜电极,m是NaOH浓溶液,通过反应:
 可制得纳米级Cu2O。阳极的电极反应式是
可制得纳米级Cu2O。阳极的电极反应式是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐3】已知水在25℃和95℃时的电离平衡曲线如图所示:

(1)25℃时水的电离平衡曲线应为_______ (填“A”或“B”)。
(2)温度95℃时,0.1mol·L-1NaOH溶液pH为_______ 。
(3)25℃时,等体积的pH=12的NaOH溶液和氨水分别与0.1mol•L-1的盐酸发生中和反应,恰好完全反应时消耗盐酸的体积_______ (填“前者多”“后者多”或“一样多”)。
(4)软锰矿的主要成分为MnO2,还含有Fe2O3、MgO、Al2O3、CaO、SiO2等杂质,工业上用软锰矿制取MnSO4·H2O的流程如图:

①“浸出”过程中MnO2与SO2转化为Mn2+的离子方程式为_______ 。
②第1步除杂中调pH至5~6使溶液中的Fe3+、Al3+形成Fe(OH)3、Al(OH)3,所加的试剂,可选择_______ (填字母)。
a.CaO b.MgO c.Al2O3 d.氨水
③“第2步除杂”主要是将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF2除去Ca2+的离子方程式_______ 。

(1)25℃时水的电离平衡曲线应为
(2)温度95℃时,0.1mol·L-1NaOH溶液pH为
(3)25℃时,等体积的pH=12的NaOH溶液和氨水分别与0.1mol•L-1的盐酸发生中和反应,恰好完全反应时消耗盐酸的体积
(4)软锰矿的主要成分为MnO2,还含有Fe2O3、MgO、Al2O3、CaO、SiO2等杂质,工业上用软锰矿制取MnSO4·H2O的流程如图:

①“浸出”过程中MnO2与SO2转化为Mn2+的离子方程式为
②第1步除杂中调pH至5~6使溶液中的Fe3+、Al3+形成Fe(OH)3、Al(OH)3,所加的试剂,可选择
a.CaO b.MgO c.Al2O3 d.氨水
③“第2步除杂”主要是将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF2除去Ca2+的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】如图是用0.1000mol•L-1的盐酸滴定某未知浓度的NaOH溶液的示意图和某次滴定前、后盛放盐酸的滴定管中液面的位置。

请回答下列问题:
(1)仪器A的名称是____ 。
(2)依据记录规则,图中所示消耗盐酸的体积为____ mL。
(3)某实验小组同学的2次实验的实验数据如表所示。根据表中数据计算出的待测NaOH溶液的平均浓度是_____ mol•L-1(保留四位有效数字)。
(4)以下操作会导致测定结果偏高的是_____ (填选项字母)。
(5)滴定时,眼睛注视_____ ,若选择甲基橙作指示剂,当加入最后半滴盐酸后:_____ ,即可确定达到滴定终点。
(6)25℃时,用0.1000mol•L-1盐酸滴定0.1000mol•L-1NaOH溶液,中和后,溶液体积为50mL。若滴定时终点判断有误差:①多加了1滴盐酸;②少加了1滴盐酸(设1滴为0.05mL,中和后总体积仍按50mL计算)。则①和②中pH相差____ (填正整数)。

请回答下列问题:
(1)仪器A的名称是
(2)依据记录规则,图中所示消耗盐酸的体积为
(3)某实验小组同学的2次实验的实验数据如表所示。根据表中数据计算出的待测NaOH溶液的平均浓度是
| 实验编号 | 待测NaOH溶液的体积/mL | 滴定前盐酸的体积读数/mL | 滴定后盐酸的体积读数/mL |
| 1 | 20.00 | 1.20 | 23.22 |
| 2 | 20.00 | 1.50 | 23.48 |
| A.蒸馏水洗涤后未用盐酸标准溶液润洗滴定管 |
| B.装待测液前,锥形瓶中有少量蒸馏水 |
| C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失 |
| D.观察读数时,滴定前仰视,滴定后俯视 |
(6)25℃时,用0.1000mol•L-1盐酸滴定0.1000mol•L-1NaOH溶液,中和后,溶液体积为50mL。若滴定时终点判断有误差:①多加了1滴盐酸;②少加了1滴盐酸(设1滴为0.05mL,中和后总体积仍按50mL计算)。则①和②中pH相差
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐2】I.向等物质的量浓度的 、NaOH混合溶液中滴加稀盐酸至过量。其中
、NaOH混合溶液中滴加稀盐酸至过量。其中 、
、 、
、 的分布分数(平衡时某微粒的浓度占含硫微粒浓度之和的分数)与滴加盐酸体积的关系如图所示(假设滴加过程中无
的分布分数(平衡时某微粒的浓度占含硫微粒浓度之和的分数)与滴加盐酸体积的关系如图所示(假设滴加过程中无 气体逸出)。
气体逸出)。

(1)滴加盐酸至过量的过程中,下列正确的是________ (填字母)。
A.曲线B表示的微粒为
B.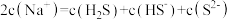
C.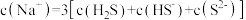
D.
(2)已知NaHS溶液呈碱性,当滴加盐酸至M点时,溶液中离子浓度由大到小的顺序是________ 。
Ⅱ.物质A~E都是由下表中离子形成,其中A与D反应得到E.常温下各物质溶液从1mL稀释到1000mL,pH的变化如图甲所示。请回答:

(3)写出B、D的化学式:B________ 、D________ 。
(4)另取浓度为 的B溶液25mL,常温下向其中逐滴滴加
的B溶液25mL,常温下向其中逐滴滴加 的D溶液,滴定过程中溶液pH的变化曲线如图乙所示。
的D溶液,滴定过程中溶液pH的变化曲线如图乙所示。
①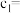
________ 。
②G点溶液中呈中性,则加入D溶液的体积V(D)________ 12.5mL(填“>”“<”“=”)。
③常温下B、C溶液的pH分别是x、y,且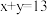 ,将B、C溶液恰好完全反应时所消耗B、C溶液的体积比
,将B、C溶液恰好完全反应时所消耗B、C溶液的体积比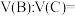
________ 。
 、NaOH混合溶液中滴加稀盐酸至过量。其中
、NaOH混合溶液中滴加稀盐酸至过量。其中 、
、 、
、 的分布分数(平衡时某微粒的浓度占含硫微粒浓度之和的分数)与滴加盐酸体积的关系如图所示(假设滴加过程中无
的分布分数(平衡时某微粒的浓度占含硫微粒浓度之和的分数)与滴加盐酸体积的关系如图所示(假设滴加过程中无 气体逸出)。
气体逸出)。
(1)滴加盐酸至过量的过程中,下列正确的是
A.曲线B表示的微粒为

B.
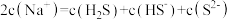
C.
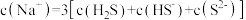
D.

(2)已知NaHS溶液呈碱性,当滴加盐酸至M点时,溶液中离子浓度由大到小的顺序是
Ⅱ.物质A~E都是由下表中离子形成,其中A与D反应得到E.常温下各物质溶液从1mL稀释到1000mL,pH的变化如图甲所示。请回答:
| 阳离子 |  、 、 、 、 |
| 阴离子 |  、 、 、 、 |

(3)写出B、D的化学式:B
(4)另取浓度为
 的B溶液25mL,常温下向其中逐滴滴加
的B溶液25mL,常温下向其中逐滴滴加 的D溶液,滴定过程中溶液pH的变化曲线如图乙所示。
的D溶液,滴定过程中溶液pH的变化曲线如图乙所示。①
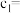
②G点溶液中呈中性,则加入D溶液的体积V(D)
③常温下B、C溶液的pH分别是x、y,且
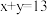 ,将B、C溶液恰好完全反应时所消耗B、C溶液的体积比
,将B、C溶液恰好完全反应时所消耗B、C溶液的体积比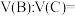
您最近一年使用:0次



