黄铁矿烧渣(主要成分为Fe2O3、FeO、及少量FeS、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用黄铁矿烧渣为原料制备高档颜料—铁红(Fe2O3)(主要成分为Fe2O3不考虑其他杂质),并以铁红为原料制备硫酸亚铁晶体(FeSO4·7H2O)的工艺:
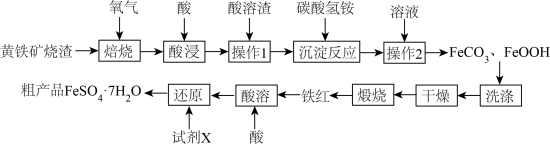
(1)焙烧的过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是_______ (任答两点)。

(2)“酸浸”时温度比较高,最适合的酸是_______ ,“酸溶渣”的成分是_______ 。
(3)“沉淀反应”中,生成FeCO3的离子方程式是_______ 。
(4)检验FeCO3是否洗涤干净的操作方法_______ 。
(5)从过滤后的滤液中得到产品,应进行的操作是_______ 、_______ 、过滤、洗涤、干燥。
(6)FeSO4·7H2O在医学上常用作补血剂。某课外小组通过以下实验方法测定某补血剂中亚铁离子的含量:
步骤I:取20片补血剂样品除去糖衣、研磨、溶解、过滤,将滤液配成250mL溶液。
步骤Ⅱ:取上述溶液25mL于锥形瓶中,加入少量稀硫酸酸化后,逐渐滴加0.0200 mol/L的KMnO4溶液,至恰好完全反应,记录消耗的KMnO4溶液的体积(假定药品中其他成分不与KMnO4反应,且 )。
)。
步骤Ⅲ:重复“步骤II”2-3次,平均消耗KMnO4溶液10.00mL。
①步骤I中配制溶液时需要的玻璃仪器除烧杯、量筒,玻璃棒外,还需要_______ 、_______ 。
②该补血剂中亚铁离子的含量为_______ mg/片。

(1)焙烧的过程中采用如图所示的“多层逆流焙烧”,“多层逆流焙烧”的优点是

(2)“酸浸”时温度比较高,最适合的酸是
(3)“沉淀反应”中,生成FeCO3的离子方程式是
(4)检验FeCO3是否洗涤干净的操作方法
(5)从过滤后的滤液中得到产品,应进行的操作是
(6)FeSO4·7H2O在医学上常用作补血剂。某课外小组通过以下实验方法测定某补血剂中亚铁离子的含量:
步骤I:取20片补血剂样品除去糖衣、研磨、溶解、过滤,将滤液配成250mL溶液。
步骤Ⅱ:取上述溶液25mL于锥形瓶中,加入少量稀硫酸酸化后,逐渐滴加0.0200 mol/L的KMnO4溶液,至恰好完全反应,记录消耗的KMnO4溶液的体积(假定药品中其他成分不与KMnO4反应,且
 )。
)。步骤Ⅲ:重复“步骤II”2-3次,平均消耗KMnO4溶液10.00mL。
①步骤I中配制溶液时需要的玻璃仪器除烧杯、量筒,玻璃棒外,还需要
②该补血剂中亚铁离子的含量为
更新时间:2022-11-13 10:24:51
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】以硫酸渣(含Fe2O3、SiO2等)为原料制备铁黄(FeOOH)的一种工艺流程如图:
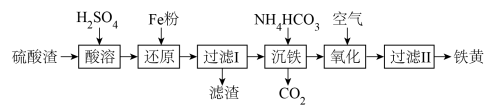
(1)“酸溶”中加快溶解的方法为_______ (任意写出一种)。
(2)“还原”过程中的离子方程式为_______ 。
(3)写出“滤渣”中主要成分的化学式:_______ 。
(4)①“沉铁”过程中生成Fe(OH)2的化学方程式为_______ 。
②若用CaCO3“沉铁”,则生成FeCO3沉淀。当反应完成时,溶液中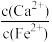 =
=_______ 。[已知Ksp(CaCO3)=2.8×10-9,Ksp(FeCO3)=2×10-11]
(5)“氧化”时,用NaNO2浓溶液代替空气氧化Fe(OH)2浆液,能缩短氧化时间,但缺点是_______ 。

(1)“酸溶”中加快溶解的方法为
(2)“还原”过程中的离子方程式为
(3)写出“滤渣”中主要成分的化学式:
(4)①“沉铁”过程中生成Fe(OH)2的化学方程式为
②若用CaCO3“沉铁”,则生成FeCO3沉淀。当反应完成时,溶液中
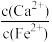 =
=(5)“氧化”时,用NaNO2浓溶液代替空气氧化Fe(OH)2浆液,能缩短氧化时间,但缺点是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】某碳素钢锅炉内水垢的主要成分是碳酸钙、硫酸钙、氢氧化镁、铁锈、二氧化硅等。水垢会形成安全隐患,需及时清洗除去。清洗流程如下:
Ⅰ.加入NaOH和Na2CO3混合液,加热,浸泡数小时;
Ⅱ.放出洗涤废液,清水冲洗锅炉,加入稀盐酸和少量NaF溶液,浸泡;
Ⅲ.向洗液中加入Na2SO3溶液;
Ⅳ.清洗达标,用NaNO2溶液钝化锅炉。
(1)用NaOH溶解二氧化硅的化学方程式是__________________________________ 。
(2)已知:20℃时溶解度/g
根据数据,结合化学平衡原理解释清洗CaSO4的过程________________________ 。
(3)在步骤Ⅱ中:
① 被除掉的水垢除铁锈外,还有_______________________________________ 。
② 清洗过程中,溶解的铁锈会加速锅炉腐蚀,用离子方程式解释其原因________ 。
(4)步骤Ⅲ中,加入Na2SO3的目的是_______________________ 。
(5)步骤Ⅳ中,钝化后的锅炉表面会覆盖一层致密的Fe2O3保护膜。
① 完成并配平其反应的离子方程式:______

②下面检测钝化效果的方法合理的是______ 。
a.在炉面上滴加浓H2SO4,观察溶液出现棕黄色的时间
b.在炉面上滴加酸性CuSO4溶液,观察蓝色消失的时间
c.在炉面上滴加酸性K3[Fe(CN)6]溶液,观察出现蓝色沉淀的时间
d.在炉面上滴加浓HNO3,观察出现红棕色气体的时间
Ⅰ.加入NaOH和Na2CO3混合液,加热,浸泡数小时;
Ⅱ.放出洗涤废液,清水冲洗锅炉,加入稀盐酸和少量NaF溶液,浸泡;
Ⅲ.向洗液中加入Na2SO3溶液;
Ⅳ.清洗达标,用NaNO2溶液钝化锅炉。
(1)用NaOH溶解二氧化硅的化学方程式是
(2)已知:20℃时溶解度/g
| CaCO3 | CaSO4 | Mg(OH)2 | MgCO3 |
| 1.4×10-3 | 2.55×10-2 | 9×10-4 | 1.1×10-2 |
(3)在步骤Ⅱ中:
① 被除掉的水垢除铁锈外,还有
② 清洗过程中,溶解的铁锈会加速锅炉腐蚀,用离子方程式解释其原因
(4)步骤Ⅲ中,加入Na2SO3的目的是
(5)步骤Ⅳ中,钝化后的锅炉表面会覆盖一层致密的Fe2O3保护膜。
① 完成并配平其反应的离子方程式:

②下面检测钝化效果的方法合理的是
a.在炉面上滴加浓H2SO4,观察溶液出现棕黄色的时间
b.在炉面上滴加酸性CuSO4溶液,观察蓝色消失的时间
c.在炉面上滴加酸性K3[Fe(CN)6]溶液,观察出现蓝色沉淀的时间
d.在炉面上滴加浓HNO3,观察出现红棕色气体的时间
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】锗是一种稀散金属,在光纤通信、航空航天等领域有广泛应用,模拟从氧化锌烟灰(成分有ZnO、ZnO·GeO2、FeO·GeO2、Fe2O3·GeO2、PbO等)中提取锗元素的流程图如下:
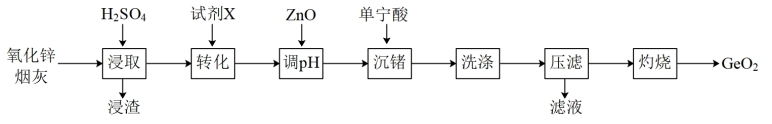
已知:①浸取后溶液pH为2,Ge以GeO2+的形式存在;
②单宁酸为复杂有机酸,易与Fe3+络合沉淀。
(1)浸取时ZnO·GeO2发生反应的化学方程式是_______ ,浸渣的主要成分是_______ 。
(2)试剂X的作用是_______ 。
(3)下图为沉锗时溶液pH对锗沉淀率的影响,则适宜的pH应为_______(填标号)。

(4)沉锗时有一段沉锗和二段沉锗两种工艺,单宁酸用量与锗沉淀率关系如表所示,工业常用二段沉锗工艺且单宁酸总用量为25倍,其原因是_______ 。
(5)可从滤液中回收的金属元素主要有_______ 。
(6)若用C2H2O表示单宁酸,压滤后的含锗沉淀表示为GeO(C2H2O)2SO4,其在空气中灼烧会得到SO2、H2O、CO2三种气体,该反应方程式为_______ 。

已知:①浸取后溶液pH为2,Ge以GeO2+的形式存在;
②单宁酸为复杂有机酸,易与Fe3+络合沉淀。
(1)浸取时ZnO·GeO2发生反应的化学方程式是
(2)试剂X的作用是
(3)下图为沉锗时溶液pH对锗沉淀率的影响,则适宜的pH应为_______(填标号)。

| A.1.0 | B.2.0 | C.2.5 | D.3.0 |
| 一段沉锗单宁酸总用量/倍 | 10 | 15 | 20 | 25 | 30 |
| 锗沉淀率/% | 88.5 | 89.5 | 90.5 | 91.5 | 93.5 |
| 二段沉锗单宁酸总用量/倍 | 10 | 15 | 20 | 25 | 30 |
| 锗沉淀率/% | 92 | 93.5 | 94.5 | 97 | 97.5 |
(6)若用C2H2O表示单宁酸,压滤后的含锗沉淀表示为GeO(C2H2O)2SO4,其在空气中灼烧会得到SO2、H2O、CO2三种气体,该反应方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】硼镁泥是一种工业废料,主要成分是MgO(占40%),还有CaO、MnO、Fe2O3、、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4•7H2O的流程如图:
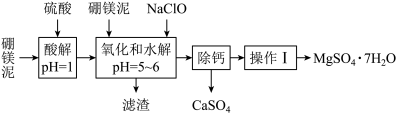
根据题意回答下列问题:
(1)实验中需用1.0mol•L-1的硫酸240mL,若用18.4mol•L-1的浓硫酸来配制,所需的仪器除了烧杯、量筒、玻璃棒,还需的玻璃仪器是_____ 。
(2)加入的NaClO可与Mn2+反应:Mn2++ClO—+H2O=MnO2↓+2H++Cl—,还有一种阳离子也会被NaClO氧化,该反应的离子方程式为_____ 。
(3)滤渣的主要成分中除含有Fe(OH)3、Al(OH)3外,还有_____ 。
(4)在“除钙”前,需检验滤液中Fe3+是否被除尽,简述检验方法:_____ 。
(5)已知MgSO4、CaSO4的溶解度如表:
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据表中数据,简要说明操作步骤:_____ 。“操作1”是将滤液继续_____ 、过滤、洗涤,便得到了MgSO4•7H2O。
(6)实验中提供的硼镁泥共10g,得到的MgSO4•7H2O为17.22g,则MgSO4•7H2O的产率为_____ 。

根据题意回答下列问题:
(1)实验中需用1.0mol•L-1的硫酸240mL,若用18.4mol•L-1的浓硫酸来配制,所需的仪器除了烧杯、量筒、玻璃棒,还需的玻璃仪器是
(2)加入的NaClO可与Mn2+反应:Mn2++ClO—+H2O=MnO2↓+2H++Cl—,还有一种阳离子也会被NaClO氧化,该反应的离子方程式为
(3)滤渣的主要成分中除含有Fe(OH)3、Al(OH)3外,还有
(4)在“除钙”前,需检验滤液中Fe3+是否被除尽,简述检验方法:
(5)已知MgSO4、CaSO4的溶解度如表:
| 温度/℃ | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(6)实验中提供的硼镁泥共10g,得到的MgSO4•7H2O为17.22g,则MgSO4•7H2O的产率为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】经多年勘测,2018年11月23日省自然资源厅发布消息称在皖江地区发现特大铜矿床,具有重大实际意义。以黄铜矿(主要成分为CuFeS2,含有少量PbS、Al2O3、SiO2)为原料制取胆矾的流程如图:


已知:常温下Ksp[Fe(OH)3]=8.0×10-38,Ksp[Al(OH)3]=3.0×10-33,Ksp[Cu(OH)2]=3.0×10-20。
(1)CuFeS2中硫元素的化合价为___________ ,硫元素在周期表中的位置是___________ 。写出上述流程中生成亚硫酸铵的离子方程式:___________ 。
(2)最适合的试剂A是___________ (写化学式)溶液,固体2的成分为PbSO4和___________ 。当试剂A的浓度为6mol·L-1时,“浸出”实验中,铜的浸出率结果如图所示。所采用的最佳实验条件(温度、时间)为___________ 。
(3)最适合的试剂B是___________ (填序号),最适合的试剂C是___________ (填序号),固体3的成分为___________ 。
a.Cl2 b.CuO c.酸性高锰酸钾溶液 d.NaOH e.H2O2溶液 f.K2CO3
(4)操作1如在实验室中进行,用到的玻璃仪器有烧杯、玻璃棒和___________ ,操作2的步骤为___________ ,___________ ,过滤、洗涤。
(5)根据已知图象信息,请计算:当Fe3+完全沉淀时,溶液中Al3+理论最大浓度为___________ 。
(提示:当离子浓度≤1×10-5mol·L时,认为该离子沉淀完全)


已知:常温下Ksp[Fe(OH)3]=8.0×10-38,Ksp[Al(OH)3]=3.0×10-33,Ksp[Cu(OH)2]=3.0×10-20。
(1)CuFeS2中硫元素的化合价为
(2)最适合的试剂A是
(3)最适合的试剂B是
a.Cl2 b.CuO c.酸性高锰酸钾溶液 d.NaOH e.H2O2溶液 f.K2CO3
(4)操作1如在实验室中进行,用到的玻璃仪器有烧杯、玻璃棒和
(5)根据已知图象信息,请计算:当Fe3+完全沉淀时,溶液中Al3+理论最大浓度为
(提示:当离子浓度≤1×10-5mol·L时,认为该离子沉淀完全)
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】铁是人体不可缺少的微量元素,硫酸亚铁晶体(FeSO4·7H2O)在医疗上常用作补血剂。某课外活动小组为测定该补血剂中铁元素的含量,设计如下实验。

(1)实验时用18.4 mol·L-1的浓硫酸配制100mL1.0 mol·L-1的硫酸溶液,所需浓硫酸的体积为______ mL(保留一位小数)。
(2)步骤①过滤后的滤液中加入氯水后发生反应的离子方程式为__________________________ 。
(3)向滤液中直接加入过量氨水时,生成的白色沉淀迅速变为灰绿色,最后变为红褐色,沉淀颜色变化的原因用化学方程式表示为_______________________ 。
(4)该补血剂中铁元素的质量分数为____________ ,若步骤③加入氨水的量不足,则实验结果_____ (填“偏大”、“偏小”、“无影响”)
(5)科学研究表明服用含硫酸亚铁的补血剂时,同时服用维生素C有利于铁元素的吸收。则维生素C在其过程中的作用是_________________ 。

(1)实验时用18.4 mol·L-1的浓硫酸配制100mL1.0 mol·L-1的硫酸溶液,所需浓硫酸的体积为
(2)步骤①过滤后的滤液中加入氯水后发生反应的离子方程式为
(3)向滤液中直接加入过量氨水时,生成的白色沉淀迅速变为灰绿色,最后变为红褐色,沉淀颜色变化的原因用化学方程式表示为
(4)该补血剂中铁元素的质量分数为
(5)科学研究表明服用含硫酸亚铁的补血剂时,同时服用维生素C有利于铁元素的吸收。则维生素C在其过程中的作用是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】可乐中的食品添加剂有白砂糖、二氧化碳、焦糖色、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为H3PO4,沸点高,难挥发)有一定关系。
(1)室温下,测得0.1 mol/L H3PO4溶液的pH= 1.5,用电离方程式解释原因:_______ 。
(2)羟基磷酸钙[Ca5(PO4)3OH]是牙齿表面起保护作用的一层坚硬物质, 在唾液中存在如下平衡:Ca5(PO4)3OH(s)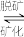 5Ca2+(aq) +3
5Ca2+(aq) +3 (aq) + OH-(aq),长期过量饮用可乐会破坏这层坚硬物质,造成龋齿。结合平衡移动原理解释原因:
(aq) + OH-(aq),长期过量饮用可乐会破坏这层坚硬物质,造成龋齿。结合平衡移动原理解释原因:_______ 。
(3)用含氟牙膏刷牙,氟离子会与牙釉质[主要成分为Ca5(PO4)3OH]发生反应: Ca5(PO4)3OH(s)+F-(aq) Ca5(PO4)3F(s)+OH-(aq),该反应的平衡常数K=_____(已知Ksp[Ca5(PO4)3OH]=7×l0-37,Ksp[Ca5(PO4)3F]=2.8×l0-61)。
Ca5(PO4)3F(s)+OH-(aq),该反应的平衡常数K=_____(已知Ksp[Ca5(PO4)3OH]=7×l0-37,Ksp[Ca5(PO4)3F]=2.8×l0-61)。
(4)向磷酸溶液中滴加NaOH溶液,含磷各微粒在溶液中的物质的量分数与pH的关系如图。
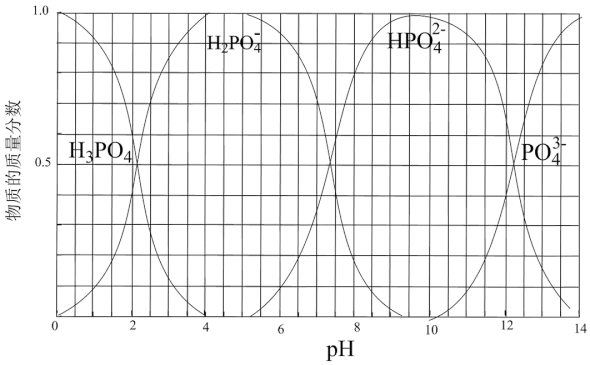
①向磷酸溶液中滴加NaOH溶液至pH = 10时发生的主要反应的离子方程式是_______ 。
②下列关于0.1 mol/L Na2HPO4溶液的说法正确的是_______ (填序号)。
a.Na2HPO4溶液显碱性,原因是 的水解程度大于其电离程度
的水解程度大于其电离程度
b.c(Na+) + c(H+) = c( )+ 2c(
)+ 2c( ) + 3c(
) + 3c( )+ c(OH- )
)+ c(OH- )
c.c(Na+) = c( ) + c(
) + c( ) +c(
) +c( ) + c(H3PO4)
) + c(H3PO4)
(5)小组同学在实验室测定某可乐中磷酸的含量(不考虑白砂糖、咖啡因的影响)。
i.将一瓶可乐注入圆底烧瓶,加入活性炭,吸附色素。
ii.将可乐回流加热10 min,冷却至室温,过滤。
iii.取50.00 mL滤液,用百里香酚酞作指示剂,用0.100 mol/L NaOH溶液滴定至终点时生成Na2HPO4,消耗NaOH溶液5.00 mL。
①加热的目的是_______ 。
②该可乐样品中磷酸的含量为_______ g/L。
(1)室温下,测得0.1 mol/L H3PO4溶液的pH= 1.5,用电离方程式解释原因:
(2)羟基磷酸钙[Ca5(PO4)3OH]是牙齿表面起保护作用的一层坚硬物质, 在唾液中存在如下平衡:Ca5(PO4)3OH(s)
 5Ca2+(aq) +3
5Ca2+(aq) +3 (aq) + OH-(aq),长期过量饮用可乐会破坏这层坚硬物质,造成龋齿。结合平衡移动原理解释原因:
(aq) + OH-(aq),长期过量饮用可乐会破坏这层坚硬物质,造成龋齿。结合平衡移动原理解释原因:(3)用含氟牙膏刷牙,氟离子会与牙釉质[主要成分为Ca5(PO4)3OH]发生反应: Ca5(PO4)3OH(s)+F-(aq)
 Ca5(PO4)3F(s)+OH-(aq),该反应的平衡常数K=_____(已知Ksp[Ca5(PO4)3OH]=7×l0-37,Ksp[Ca5(PO4)3F]=2.8×l0-61)。
Ca5(PO4)3F(s)+OH-(aq),该反应的平衡常数K=_____(已知Ksp[Ca5(PO4)3OH]=7×l0-37,Ksp[Ca5(PO4)3F]=2.8×l0-61)。(4)向磷酸溶液中滴加NaOH溶液,含磷各微粒在溶液中的物质的量分数与pH的关系如图。

①向磷酸溶液中滴加NaOH溶液至pH = 10时发生的主要反应的离子方程式是
②下列关于0.1 mol/L Na2HPO4溶液的说法正确的是
a.Na2HPO4溶液显碱性,原因是
 的水解程度大于其电离程度
的水解程度大于其电离程度b.c(Na+) + c(H+) = c(
 )+ 2c(
)+ 2c( ) + 3c(
) + 3c( )+ c(OH- )
)+ c(OH- )c.c(Na+) = c(
 ) + c(
) + c( ) +c(
) +c( ) + c(H3PO4)
) + c(H3PO4)(5)小组同学在实验室测定某可乐中磷酸的含量(不考虑白砂糖、咖啡因的影响)。
i.将一瓶可乐注入圆底烧瓶,加入活性炭,吸附色素。
ii.将可乐回流加热10 min,冷却至室温,过滤。
iii.取50.00 mL滤液,用百里香酚酞作指示剂,用0.100 mol/L NaOH溶液滴定至终点时生成Na2HPO4,消耗NaOH溶液5.00 mL。
①加热的目的是
②该可乐样品中磷酸的含量为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】 在化工领域有着极其广泛的应用,某兴趣小组以钛铁矿(主要成分为
在化工领域有着极其广泛的应用,某兴趣小组以钛铁矿(主要成分为 ,含少量FeO和二氧化硅,其他杂质忽略)为原料制备
,含少量FeO和二氧化硅,其他杂质忽略)为原料制备 和
和 ,流程如下:
,流程如下:

已知:①
②硫酸氧钛( )溶解度在中性或弱碱性溶液中较小,酸性条件下大大升高。
)溶解度在中性或弱碱性溶液中较小,酸性条件下大大升高。
(1)试剂A的成分___________
(2)操作Ⅱ___________ 、洗涤、干燥
(3) 加水煮沸发生的反应方程式
加水煮沸发生的反应方程式___________
(4)下列说法正确的是___________
(5)为了测定 产品的纯度,可采用氧化还原滴定法。其原理:在一定条件下,将
产品的纯度,可采用氧化还原滴定法。其原理:在一定条件下,将 溶解并还原为
溶解并还原为 ,再用硫酸酸化的
,再用硫酸酸化的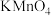 标准溶液滴定
标准溶液滴定 至全部生成
至全部生成 。
。
①从下列选项中选出合理正确的操作并按序排列:___________
a.向棕色的酸式滴定管中注入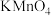 标准溶液至“0”刻度以上
标准溶液至“0”刻度以上
b.量取25.00mL待测溶液于锥形瓶
c.滴定至溶液呈微红色,30s内不褪色,记录读数
d.用洗耳球吹出润洗液
e.重复滴定,记录数据,并处理。
f.排气泡后调节液面至零刻度或零刻度以下,记录数据
g.称取mg ,溶解并还原为
,溶解并还原为 ,配成100mL待测溶液
,配成100mL待测溶液
h.往锥形瓶中滴入几滴指示剂
②三次平行实验测得的数据如下表:
已知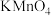 标准溶液的浓度为0.01250
标准溶液的浓度为0.01250 ,则实验测得
,则实验测得 产品的纯度为
产品的纯度为___________
③若滴定管滴定前有气泡,滴定后气泡消失,则测定结果将___ (填“偏高”、“偏低”或“无影响”)。
 在化工领域有着极其广泛的应用,某兴趣小组以钛铁矿(主要成分为
在化工领域有着极其广泛的应用,某兴趣小组以钛铁矿(主要成分为 ,含少量FeO和二氧化硅,其他杂质忽略)为原料制备
,含少量FeO和二氧化硅,其他杂质忽略)为原料制备 和
和 ,流程如下:
,流程如下:
已知:①

②硫酸氧钛(
 )溶解度在中性或弱碱性溶液中较小,酸性条件下大大升高。
)溶解度在中性或弱碱性溶液中较小,酸性条件下大大升高。(1)试剂A的成分
(2)操作Ⅱ
(3)
 加水煮沸发生的反应方程式
加水煮沸发生的反应方程式(4)下列说法正确的是___________
| A.用酸浸取钛矿石,矿石越粉碎浸取率越高 |
B.滤渣的成分只有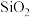 |
C.洗涤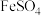 晶体表面的杂质时,应用浓硫酸,防止 晶体表面的杂质时,应用浓硫酸,防止 析出 析出 |
| D.灼烧过程中用到硅酸盐仪器有瓷坩埚、泥三角、酒精灯、玻璃棒 |
(5)为了测定
 产品的纯度,可采用氧化还原滴定法。其原理:在一定条件下,将
产品的纯度,可采用氧化还原滴定法。其原理:在一定条件下,将 溶解并还原为
溶解并还原为 ,再用硫酸酸化的
,再用硫酸酸化的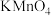 标准溶液滴定
标准溶液滴定 至全部生成
至全部生成 。
。①从下列选项中选出合理正确的操作并按序排列:
a.向棕色的酸式滴定管中注入
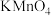 标准溶液至“0”刻度以上
标准溶液至“0”刻度以上b.量取25.00mL待测溶液于锥形瓶
c.滴定至溶液呈微红色,30s内不褪色,记录读数

d.用洗耳球吹出润洗液
e.重复滴定,记录数据,并处理。
f.排气泡后调节液面至零刻度或零刻度以下,记录数据

g.称取mg
 ,溶解并还原为
,溶解并还原为 ,配成100mL待测溶液
,配成100mL待测溶液h.往锥形瓶中滴入几滴指示剂
②三次平行实验测得的数据如下表:
| 实验序号 |  |  |
| 1 | 0.50 | 20.48 |
| 2 | 1.10 | 21.54 |
| 3 | 1.50 | 21.52 |
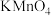 标准溶液的浓度为0.01250
标准溶液的浓度为0.01250 ,则实验测得
,则实验测得 产品的纯度为
产品的纯度为③若滴定管滴定前有气泡,滴定后气泡消失,则测定结果将
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】钴配合物 溶于热水,稍溶于冷水,微溶于盐酸,难溶于乙醇,可通过以下步骤制备,具体步骤如下:
溶于热水,稍溶于冷水,微溶于盐酸,难溶于乙醇,可通过以下步骤制备,具体步骤如下:

①称取 ,用5mL水溶解。
,用5mL水溶解。
②分批加入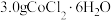 后,将溶液温度降至10℃以下,将混合物转入如图所示装置,加入1g活性炭、7mL浓氨水,搅拌下逐滴加入10mL6%的双氧水。
后,将溶液温度降至10℃以下,将混合物转入如图所示装置,加入1g活性炭、7mL浓氨水,搅拌下逐滴加入10mL6%的双氧水。
③加热至55~60℃反应20min。冷却,过滤。
④将滤得的固体转入含有少量盐酸的25mL沸水中,趁热过滤。
⑤滤液转入烧杯,加入4mL浓盐酸,冷却、过滤、洗涤、干燥得到橙黄色晶体。
回答下列问题:
(1)盛双氧水的仪器名称是______ ;三颈烧瓶选用规格是______ (填写字母)。
A.50mL B.100mL C.250mL D.500mL
(2)步骤②中,将温度降至10℃以下可避免______ ;步骤④中,趁热过滤得到滤渣的主要成分是______ 。
(3)步骤④、⑤中,提纯滤得固体的方法是______ ,步骤⑤中加入浓盐酸的目的是______ 。
(4)洗涤橙黄色晶体,下列方法中最合适的是______(填写字母)。
(5)产品分析:假设 是产品中唯一可与氢氧化钠反应生成氨气的物质,可采用如下方法测定产品
是产品中唯一可与氢氧化钠反应生成氨气的物质,可采用如下方法测定产品 纯度。从下列选项中选择最佳操作并排序填入中
纯度。从下列选项中选择最佳操作并排序填入中_______ 。
准确称取产品xg→ → → → →计算。
a.将样品加入三颈烧瓶中,再加入足量NaOH溶液并加热,蒸出氨气
b.用HCl标准溶液滴定
c.用NaOH标准溶液滴定
d.用已知体积且过量的HCl标准溶液吸收氨气
e.用已知体积且过量的醋酸溶液吸收氨气
f.滴加酚酞指示剂(变色的pH范围8.2~10.0)
g.滴加石蕊指示剂(变色的pH范围4.5~8.3)
h.滴加甲基红指示剂(变色的pH范围4.4~6.2)
 溶于热水,稍溶于冷水,微溶于盐酸,难溶于乙醇,可通过以下步骤制备,具体步骤如下:
溶于热水,稍溶于冷水,微溶于盐酸,难溶于乙醇,可通过以下步骤制备,具体步骤如下:
①称取
 ,用5mL水溶解。
,用5mL水溶解。②分批加入
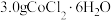 后,将溶液温度降至10℃以下,将混合物转入如图所示装置,加入1g活性炭、7mL浓氨水,搅拌下逐滴加入10mL6%的双氧水。
后,将溶液温度降至10℃以下,将混合物转入如图所示装置,加入1g活性炭、7mL浓氨水,搅拌下逐滴加入10mL6%的双氧水。③加热至55~60℃反应20min。冷却,过滤。
④将滤得的固体转入含有少量盐酸的25mL沸水中,趁热过滤。
⑤滤液转入烧杯,加入4mL浓盐酸,冷却、过滤、洗涤、干燥得到橙黄色晶体。
回答下列问题:
(1)盛双氧水的仪器名称是
A.50mL B.100mL C.250mL D.500mL
(2)步骤②中,将温度降至10℃以下可避免
(3)步骤④、⑤中,提纯滤得固体的方法是
(4)洗涤橙黄色晶体,下列方法中最合适的是______(填写字母)。
| A.先用盐酸洗,后用乙醇洗 | B.先用盐酸洗,后用冷水洗 |
| C.先用冷水洗,后用乙醇洗 | D.先用乙醇洗,后用冷水洗 |
(5)产品分析:假设
 是产品中唯一可与氢氧化钠反应生成氨气的物质,可采用如下方法测定产品
是产品中唯一可与氢氧化钠反应生成氨气的物质,可采用如下方法测定产品 纯度。从下列选项中选择最佳操作并排序填入中
纯度。从下列选项中选择最佳操作并排序填入中准确称取产品xg→ → → → →计算。
a.将样品加入三颈烧瓶中,再加入足量NaOH溶液并加热,蒸出氨气
b.用HCl标准溶液滴定
c.用NaOH标准溶液滴定
d.用已知体积且过量的HCl标准溶液吸收氨气
e.用已知体积且过量的醋酸溶液吸收氨气
f.滴加酚酞指示剂(变色的pH范围8.2~10.0)
g.滴加石蕊指示剂(变色的pH范围4.5~8.3)
h.滴加甲基红指示剂(变色的pH范围4.4~6.2)
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】从砷化镓废料(主要成分为GaAs、含Fe2O3、SiO2和CaCO3等杂质)中回收镓和砷的工艺流程如图所示:

已知: Ga(OH)3是两性氢氧化物,其酸式电离和碱式电离的方程式如下:

25℃时,Ga(OH)3的溶度积Ksp[ Ga(OH)3 ]=1.6×10-34,Kb(NH3·H2O) ≈2.0×10-5
回答下列问题:
(1)“浆化”过程将砷化镓废料转变为悬浊液,目的是________________________ 。
(2)“碱浸1”过程,砷化镓转化为NaGaO2和Na3AsO4,该反应的离子方程式:_____________ 。
(3)滤渣1的成份主要是___________________
(4)“电解”是指用传统的方法将Ga(OH)3溶解到NaOH溶液中,电解得到金属镓。电解时,GaO 在阴极放电的电极反应式:
在阴极放电的电极反应式:________________________ 。
(5)向“调pH”后得到的滤液中加入足量NaOH溶液,使pH大于12,经__________ 、_____ 、过滤、洗涤、低温干燥后得到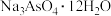 。
。
(6)为探究Ga(OH)3在氨水中能否溶解,计算反应Ga(OH)3+NH3·H2O [Ga(OH)4]+NH
[Ga(OH)4]+NH 的平衡常数K=
的平衡常数K=___________ 。(已知:Ga3++4OH— [Ga(OH)4]
[Ga(OH)4]  )
)

已知: Ga(OH)3是两性氢氧化物,其酸式电离和碱式电离的方程式如下:

25℃时,Ga(OH)3的溶度积Ksp[ Ga(OH)3 ]=1.6×10-34,Kb(NH3·H2O) ≈2.0×10-5
回答下列问题:
(1)“浆化”过程将砷化镓废料转变为悬浊液,目的是
(2)“碱浸1”过程,砷化镓转化为NaGaO2和Na3AsO4,该反应的离子方程式:
(3)滤渣1的成份主要是
(4)“电解”是指用传统的方法将Ga(OH)3溶解到NaOH溶液中,电解得到金属镓。电解时,GaO
 在阴极放电的电极反应式:
在阴极放电的电极反应式:(5)向“调pH”后得到的滤液中加入足量NaOH溶液,使pH大于12,经
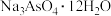 。
。(6)为探究Ga(OH)3在氨水中能否溶解,计算反应Ga(OH)3+NH3·H2O
 [Ga(OH)4]+NH
[Ga(OH)4]+NH 的平衡常数K=
的平衡常数K= [Ga(OH)4]
[Ga(OH)4]  )
)
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】硫酸肼(N2H4·H2SO4)又名硫酸联氨,在医药、染料、农业上用途广泛。
已知:①Cl2与NaOH溶液的反应为放热反应,Cl2与热的NaOH溶液反应会生成NaClO3
②利用尿素法生产水合肼的原理:CO(NH2)2+2NaOH+NaClO=N2H4·H2O+Na2CO3+NaCl
③硫酸肼的制备原理:N2H4·H2O+H2SO4=N2H4·H2SO4+H2O
回答下列问题:
Ⅰ.制备NaClO溶液
实验制备装置如图甲所示:
(1)欲配制220mL6mol/L的盐酸,则需要密度为1.2g/mL,质量分数为36.5%的浓盐酸体积为____ mL,此过程所需玻璃仪器有:量筒、烧杯、玻璃棒、胶头滴管和____ 。
(2)甲图装置C试管内发生主要化学反应的离子方程式为____ 。
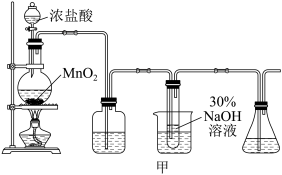
Ⅱ.乙图是尿素法生产水合肼的装置
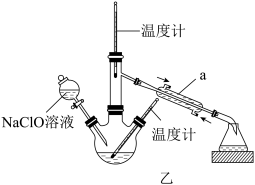
(3)把Ⅰ制得的NaClO溶液注入到图乙装置的分液漏斗中,三颈烧瓶内装入一定量的尿素和NaOH溶液,应采用____ 的方式降温,并控制低温(低于20℃)进行反应。温度高时水合肼会被氧化成无色无味的气体,该气体在标准状况下的密度为1.25g·L-1,其反应的化学方程式为_____ 。反应结束后,收集108~1149℃馏分。
(4)测定馏分中水合肼的含量。称取馏分5.0g,加入适量NaHCO3固体(调节溶液的pH保持在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.30mol·L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)。实验测得消耗I2溶液体积的平均值为20.00mL,则馏分中水合肼(N2H4H2O)的质量分数为____ 。(保留两位有效数字)
Ⅲ.硫酸肼的性质、制备
已知:硫酸肼(又可以表示为:N2H6SO4)是一种重要的化工原料,硫酸肼属于离子化合物,易溶于水,溶液呈酸性,水解原理与(NH4)2SO4类似。
(5)将水合肼转移到烧杯中,滴加一定量浓硫酸,控制温度,得硫酸肼沉淀。洗涤硫酸肼时用无水乙醇而不用水洗涤的原因是____ 。
(6)①写出硫酸肼第二步水解反应的离子方程式:____ 。
②硫酸肼水溶液中离子浓度关系表达正确的是____ (填英文字母)。
A.c(SO )=c(N2H
)=c(N2H )+c(N2H
)+c(N2H )+c(N2H4·H2O)
)+c(N2H4·H2O)
B.c(SO )>c([N2H5·H2O]+)>c(H+)>c(OH-)
)>c([N2H5·H2O]+)>c(H+)>c(OH-)
C.2c(N2H )+c([N2H5·H2O]+)=c(H+)+c(OH-)
)+c([N2H5·H2O]+)=c(H+)+c(OH-)
D.c(SO )>c(N2H
)>c(N2H )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
已知:①Cl2与NaOH溶液的反应为放热反应,Cl2与热的NaOH溶液反应会生成NaClO3
②利用尿素法生产水合肼的原理:CO(NH2)2+2NaOH+NaClO=N2H4·H2O+Na2CO3+NaCl
③硫酸肼的制备原理:N2H4·H2O+H2SO4=N2H4·H2SO4+H2O
回答下列问题:
Ⅰ.制备NaClO溶液
实验制备装置如图甲所示:
(1)欲配制220mL6mol/L的盐酸,则需要密度为1.2g/mL,质量分数为36.5%的浓盐酸体积为
(2)甲图装置C试管内发生主要化学反应的离子方程式为

Ⅱ.乙图是尿素法生产水合肼的装置

(3)把Ⅰ制得的NaClO溶液注入到图乙装置的分液漏斗中,三颈烧瓶内装入一定量的尿素和NaOH溶液,应采用
(4)测定馏分中水合肼的含量。称取馏分5.0g,加入适量NaHCO3固体(调节溶液的pH保持在6.5左右),加水配成250mL溶液,移取25.00mL置于锥形瓶中,并滴加2~3滴淀粉溶液,用0.30mol·L-1的碘标准溶液滴定(已知:N2H4·H2O+2I2=N2↑+4HI+H2O)。实验测得消耗I2溶液体积的平均值为20.00mL,则馏分中水合肼(N2H4H2O)的质量分数为
Ⅲ.硫酸肼的性质、制备
已知:硫酸肼(又可以表示为:N2H6SO4)是一种重要的化工原料,硫酸肼属于离子化合物,易溶于水,溶液呈酸性,水解原理与(NH4)2SO4类似。
(5)将水合肼转移到烧杯中,滴加一定量浓硫酸,控制温度,得硫酸肼沉淀。洗涤硫酸肼时用无水乙醇而不用水洗涤的原因是
(6)①写出硫酸肼第二步水解反应的离子方程式:
②硫酸肼水溶液中离子浓度关系表达正确的是
A.c(SO
 )=c(N2H
)=c(N2H )+c(N2H
)+c(N2H )+c(N2H4·H2O)
)+c(N2H4·H2O)B.c(SO
 )>c([N2H5·H2O]+)>c(H+)>c(OH-)
)>c([N2H5·H2O]+)>c(H+)>c(OH-)C.2c(N2H
 )+c([N2H5·H2O]+)=c(H+)+c(OH-)
)+c([N2H5·H2O]+)=c(H+)+c(OH-)D.c(SO
 )>c(N2H
)>c(N2H )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】 对神经元有明显的保护作用,在医疗上可用于减轻急性低氧所致的某些神经电流变化。由含钴矿(
对神经元有明显的保护作用,在医疗上可用于减轻急性低氧所致的某些神经电流变化。由含钴矿( 元素主要以
元素主要以 、
、 的形式存在,还含有
的形式存在,还含有 、
、 、
、 、
、 、
、 、
、 元素)制取氯化钴晶体的一种工艺流程如下:
元素)制取氯化钴晶体的一种工艺流程如下:
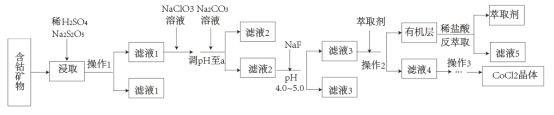
已知:①焦亚硫酸钠( )是食品中常见的还原剂。
)是食品中常见的还原剂。
②25℃时,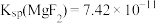 ,
,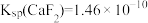 。
。
③部分金属阳离子形成氢氧化物的 见下表:
见下表:
回答下列问题:
(1)操作①的名称为___________ ,浸取时加入Na2S2O5的离子方程式为___________ 。
(2)滤液1中加入 用作氧化剂,
用作氧化剂, 在流程中还具有的作用是
在流程中还具有的作用是___________ 。
(3)加入 溶液调节
溶液调节 至
至 ,若
,若 的范围是3.2~4.0时,则加入
的范围是3.2~4.0时,则加入 溶液生成滤渣2的主要离子方程式为
溶液生成滤渣2的主要离子方程式为___________ 。
(4)滤渣3的主要成分为 和
和 ,则滤液3中
,则滤液3中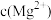 与
与 的比值为
的比值为___________ 。
(5)经过萃取和反萃取操作,溶液5中的阳离子主要含有 和
和 、
、 ,滤液4经过操作3可制备
,滤液4经过操作3可制备 晶体,操作3中包含3个基本实验操作,它们是
晶体,操作3中包含3个基本实验操作,它们是___________ 、___________ 、___________ 。
(6)上述流程中可循环使用的物质是___________ 。
(7)在上述新工艺中,用“稀硫酸和氯酸钠”代替原工艺中“盐酸与硝酸”,其主要优点是___________ 。
 对神经元有明显的保护作用,在医疗上可用于减轻急性低氧所致的某些神经电流变化。由含钴矿(
对神经元有明显的保护作用,在医疗上可用于减轻急性低氧所致的某些神经电流变化。由含钴矿( 元素主要以
元素主要以 、
、 的形式存在,还含有
的形式存在,还含有 、
、 、
、 、
、 、
、 、
、 元素)制取氯化钴晶体的一种工艺流程如下:
元素)制取氯化钴晶体的一种工艺流程如下:
已知:①焦亚硫酸钠(
 )是食品中常见的还原剂。
)是食品中常见的还原剂。②25℃时,
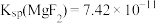 ,
,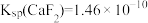 。
。③部分金属阳离子形成氢氧化物的
 见下表:
见下表: |  |  |  |  |  | 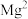 | |
开始沉淀 | 0.3 | 5.5 | 2.7 | 7.2 | 7.6 | 7.6 | 9.6 |
完全沉淀 | 1.1 | 6.6 | 3.2 | 9.2 | 9.6 | 9.2 | 11.1 |
回答下列问题:
(1)操作①的名称为
(2)滤液1中加入
 用作氧化剂,
用作氧化剂, 在流程中还具有的作用是
在流程中还具有的作用是(3)加入
 溶液调节
溶液调节 至
至 ,若
,若 的范围是3.2~4.0时,则加入
的范围是3.2~4.0时,则加入 溶液生成滤渣2的主要离子方程式为
溶液生成滤渣2的主要离子方程式为(4)滤渣3的主要成分为
 和
和 ,则滤液3中
,则滤液3中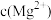 与
与 的比值为
的比值为(5)经过萃取和反萃取操作,溶液5中的阳离子主要含有
 和
和 、
、 ,滤液4经过操作3可制备
,滤液4经过操作3可制备 晶体,操作3中包含3个基本实验操作,它们是
晶体,操作3中包含3个基本实验操作,它们是(6)上述流程中可循环使用的物质是
(7)在上述新工艺中,用“稀硫酸和氯酸钠”代替原工艺中“盐酸与硝酸”,其主要优点是
您最近一年使用:0次



