由化学能产生热能是目前人类使用能源的主要途径。回答下列问题:
(1)图1表示反应 的能量变化。
的能量变化。
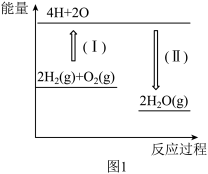
已知断开1molH-H键、1molO=O键和1molH-O键分别需要消耗436kJ、496kJ和460kJ的能量。则反应过程(II)中生成2mol (g)时
(g)时_______ (填“吸收”或“放出”)_______ kJ能量。
(2)由 和NO反应生成
和NO反应生成 和
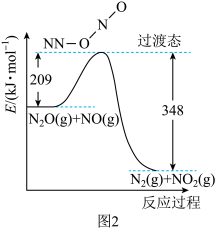
和 的能量变化如图2所示。其正反应的活化能为
的能量变化如图2所示。其正反应的活化能为_______  ,若反应生成
,若反应生成 ,其
,其
_______  。
。
(3)已知某温度时,反应I:
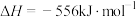 ;
;
反应II: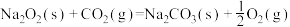
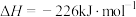 。
。
CO(g)与 (s)反应生成
(s)反应生成 (s),该反应的热化学方程式为
(s),该反应的热化学方程式为_______ 。
(4)I.
II.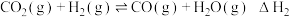
反应 的
的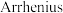 经验公式的实验数据如图中曲线
经验公式的实验数据如图中曲线 所示,已知
所示,已知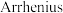 经验公式为
经验公式为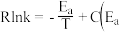 为活化能,
为活化能, 为速率常数,
为速率常数, 和
和 为常数
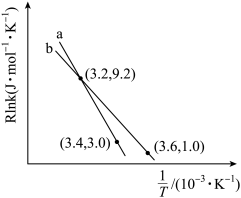
为常数 。则该反应的活化能Ea=
。则该反应的活化能Ea=______ kJ/mol。当改变外界条件时,实验数据如图中的曲线 所示,则实验可能改变的外界条件是
所示,则实验可能改变的外界条件是_______ 。
(1)图1表示反应
 的能量变化。
的能量变化。
已知断开1molH-H键、1molO=O键和1molH-O键分别需要消耗436kJ、496kJ和460kJ的能量。则反应过程(II)中生成2mol
 (g)时
(g)时(2)由
 和NO反应生成
和NO反应生成 和
和 的能量变化如图2所示。其正反应的活化能为
的能量变化如图2所示。其正反应的活化能为 ,若反应生成
,若反应生成 ,其
,其
 。
。
(3)已知某温度时,反应I:

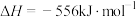 ;
;反应II:
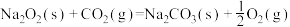
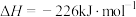 。
。CO(g)与
 (s)反应生成
(s)反应生成 (s),该反应的热化学方程式为
(s),该反应的热化学方程式为(4)I.

II.
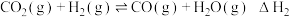
反应
 的
的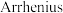 经验公式的实验数据如图中曲线
经验公式的实验数据如图中曲线 所示,已知
所示,已知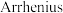 经验公式为
经验公式为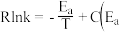 为活化能,
为活化能, 为速率常数,
为速率常数, 和
和 为常数
为常数 。则该反应的活化能Ea=
。则该反应的活化能Ea= 所示,则实验可能改变的外界条件是
所示,则实验可能改变的外界条件是
更新时间:2022-11-07 11:08:21
|
相似题推荐
【推荐1】乙二醇(沸点:197.3℃)是一种重要的基础化工原料。由煤基合成气(主要成分CO、H2)与氧气先制备得到草酸二甲酯(沸点:164.5℃),再加氢间接合成乙二醇,具有反应条件温和、环境污染小等优点。反应过程如下:
反应I:4NO(g)+4CH3OH(g)+O2(g) 4CH3ONO(g)+2H2O(g) △H1 =a kJ·mol-1
4CH3ONO(g)+2H2O(g) △H1 =a kJ·mol-1
反应II:2CO(g)+2CH3ONO(g) CH3OOCCOOCH3(l) + 2NO(g) △H2=b kJ·mol-1
CH3OOCCOOCH3(l) + 2NO(g) △H2=b kJ·mol-1
反应III:CH3OOCCOOCH3(1)+4H2(g) HOCH2CH2OH(1)+2CH3OH(g) △H3 =c kJ·mol-1
HOCH2CH2OH(1)+2CH3OH(g) △H3 =c kJ·mol-1
请回答下列问题:
(1)煤基合成气间接合成乙二醇的总热化学方程式是_____________________________ ,已知该反应在较低温条件下能自发进行。说明该反应的△H ______ 0(填“>”“<”或“=”)。
(2)CO、CH3ONO各0.4mol在恒温、容积恒定为2 L的密闭容器中发生反应II,达到平衡时CO的体积分数与NO的体积分数相等,计算该反应的化学平衡常数K=_____________ 。若此时向容器中再通入0.4 mol NO,一段时间后,达到新平衡时NO 的体积分数与原平衡时相比______ (填“增大”“相等”“减小”或“不能确定”)。
(3)温度改变对反应II的催化剂活性有影响,评价催化剂的活性参数——空时收率和CO的选择性可表示如下:
空 时收率=CH3OOCCOOCH3质量/反应时间×催化剂的体积
CO的选择性=合成[CH3OOCCOOCH3所消耗的CO的物质的量/反应掉的CO 的物质的量]×100%
在不同温度下,某学习小组对四组其他条件都相同的反应物进行研究,经过相同时间th,测得空时收率、CO的选择性数据如下表所示。
下列说法正确的是________ (填字母代号)。
A.温度升高,空时收率先增大后减小,说明△H2>0
B.温度升高,催化剂活性逐渐减弱,对CO 的选择性逐渐降低
C.综合考虑空时收率和CO的选择性,工业生成CH3OOCCOOCH3时,选择140℃效果最好
D.130℃时,CO的选择性最高,说明CO生成CH3OOCCOOCH3的转化率最高
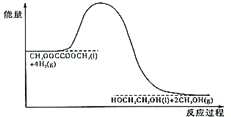
(4)120℃、常压时,CH3OOCCOOCH3 +4H2 HOCH2CH2OH+2CH3OH 反应过程中的能量变化如图所示。画出180℃、常压时,加入催化剂,该反应过程中的能量变化图。
HOCH2CH2OH+2CH3OH 反应过程中的能量变化如图所示。画出180℃、常压时,加入催化剂,该反应过程中的能量变化图。________
(5)研究证实,乙二醇、氧气可以在碱性溶液中形成燃料电池,负极的电极反应式是________________ 。
反应I:4NO(g)+4CH3OH(g)+O2(g)
 4CH3ONO(g)+2H2O(g) △H1 =a kJ·mol-1
4CH3ONO(g)+2H2O(g) △H1 =a kJ·mol-1反应II:2CO(g)+2CH3ONO(g)
 CH3OOCCOOCH3(l) + 2NO(g) △H2=b kJ·mol-1
CH3OOCCOOCH3(l) + 2NO(g) △H2=b kJ·mol-1反应III:CH3OOCCOOCH3(1)+4H2(g)
 HOCH2CH2OH(1)+2CH3OH(g) △H3 =c kJ·mol-1
HOCH2CH2OH(1)+2CH3OH(g) △H3 =c kJ·mol-1请回答下列问题:
(1)煤基合成气间接合成乙二醇的总热化学方程式是
(2)CO、CH3ONO各0.4mol在恒温、容积恒定为2 L的密闭容器中发生反应II,达到平衡时CO的体积分数与NO的体积分数相等,计算该反应的化学平衡常数K=
(3)温度改变对反应II的催化剂活性有影响,评价催化剂的活性参数——空时收率和CO的选择性可表示如下:
空 时收率=CH3OOCCOOCH3质量/反应时间×催化剂的体积
CO的选择性=合成[CH3OOCCOOCH3所消耗的CO的物质的量/反应掉的CO 的物质的量]×100%
在不同温度下,某学习小组对四组其他条件都相同的反应物进行研究,经过相同时间th,测得空时收率、CO的选择性数据如下表所示。
| 反应温度(℃) | 空时收率(g·mL-1·h-1) | CO的选择性(%) |
| 130 | 0.70 | ①72.5 |
| 140 | 0.75 | ②71.0 |
| 150 | 0.71 | ③55.6 |
| 160 | 0.66 | ④63.3 |
A.温度升高,空时收率先增大后减小,说明△H2>0
B.温度升高,催化剂活性逐渐减弱,对CO 的选择性逐渐降低
C.综合考虑空时收率和CO的选择性,工业生成CH3OOCCOOCH3时,选择140℃效果最好
D.130℃时,CO的选择性最高,说明CO生成CH3OOCCOOCH3的转化率最高
(4)120℃、常压时,CH3OOCCOOCH3 +4H2
 HOCH2CH2OH+2CH3OH 反应过程中的能量变化如图所示。画出180℃、常压时,加入催化剂,该反应过程中的能量变化图。
HOCH2CH2OH+2CH3OH 反应过程中的能量变化如图所示。画出180℃、常压时,加入催化剂,该反应过程中的能量变化图。
(5)研究证实,乙二醇、氧气可以在碱性溶液中形成燃料电池,负极的电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】( N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池, NO2 的二聚体 N2O4 则是火箭中常用氧化剂。试回答下列问题
(1)肼的结构式为____________ 。
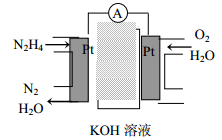
(2)肼燃料电池原理如图所示,左边电极上发生的电极反应式为_________________ 。
(3)火箭常用 N2O4 作氧化剂,肼作燃料,已知:
N2(g)+2O2(g)=2NO2(g) △H=-67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.0kJ·mol-1
2NO2(g) N2O4(g) △H=-52.7kJ·mol-1
N2O4(g) △H=-52.7kJ·mol-1
写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:_________________ 。
(4)联氨的工业生产常用氨和次氯酸钠为原料获得,也可在催化剂作用下,用尿素[CO(NH2)2]和次氯酸钠与氢氧化钠的混合溶液反应获得,尿素法反应的离子方程式为_________________ 。
(1)肼的结构式为
(2)肼燃料电池原理如图所示,左边电极上发生的电极反应式为

(3)火箭常用 N2O4 作氧化剂,肼作燃料,已知:
N2(g)+2O2(g)=2NO2(g) △H=-67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.0kJ·mol-1
2NO2(g)
 N2O4(g) △H=-52.7kJ·mol-1
N2O4(g) △H=-52.7kJ·mol-1写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:
(4)联氨的工业生产常用氨和次氯酸钠为原料获得,也可在催化剂作用下,用尿素[CO(NH2)2]和次氯酸钠与氢氧化钠的混合溶液反应获得,尿素法反应的离子方程式为
您最近一年使用:0次
【推荐3】I.在25 ℃、101 kPa下:①2Na(s)+ O2(g)=Na2O(s) ΔH1=-414 kJ·mol-1;②2Na(s)+O2(g)=Na2O2(s) ΔH2=-511 kJ·mol-1;25℃、101 kPa下,Na2O2(s)与Na(s)反应生成Na2O(s)的热化学方程式为
O2(g)=Na2O(s) ΔH1=-414 kJ·mol-1;②2Na(s)+O2(g)=Na2O2(s) ΔH2=-511 kJ·mol-1;25℃、101 kPa下,Na2O2(s)与Na(s)反应生成Na2O(s)的热化学方程式为______ 。
II.在2L密闭容器内,800℃时反应:2NO(g)+O2(g)⇌2NO2(g)体系中,n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=______ 。
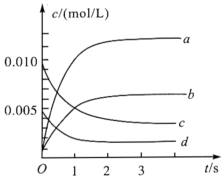
(2)如图中表示NO2的变化的曲线是______ 。用O2表示从0~2s内该反应的平均速率v=______
(3)能说明该反应已达到平衡状态的是______ 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)某同学查阅资料得知,该反应K300℃>K350℃;25℃时,生成1molNO2,热量变化为56.4kJ。但是该同学由于疏忽,忘记注明“+”、“-”。根据题目信息,该反应的热化学方程式为______ 。
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的是______ 。
a.及时分离除NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
 O2(g)=Na2O(s) ΔH1=-414 kJ·mol-1;②2Na(s)+O2(g)=Na2O2(s) ΔH2=-511 kJ·mol-1;25℃、101 kPa下,Na2O2(s)与Na(s)反应生成Na2O(s)的热化学方程式为
O2(g)=Na2O(s) ΔH1=-414 kJ·mol-1;②2Na(s)+O2(g)=Na2O2(s) ΔH2=-511 kJ·mol-1;25℃、101 kPa下,Na2O2(s)与Na(s)反应生成Na2O(s)的热化学方程式为II.在2L密闭容器内,800℃时反应:2NO(g)+O2(g)⇌2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=
(2)如图中表示NO2的变化的曲线是

(3)能说明该反应已达到平衡状态的是
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)某同学查阅资料得知,该反应K300℃>K350℃;25℃时,生成1molNO2,热量变化为56.4kJ。但是该同学由于疏忽,忘记注明“+”、“-”。根据题目信息,该反应的热化学方程式为
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离除NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】能量以多种不同的形式存在,并能相互转化。
I.化学反应伴随能量变化。
(1)NH4HCO3和CH3COOH反应过程的能量变化如图所示,___________ 代表反应活化能(填“E1”或“E2”)。
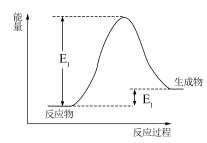
(2)某实验小组设计了三套实验装置(如图),不能用来证明“NH4HCO3和CH3COOH反应能量变化情况”的是___________ (填序号)。
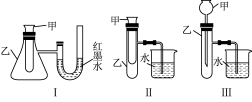
(3)NH4HCO3和CH3COOH反应的离子方程式为___________ 。
II.合成氨反应为放热反应,在化工生产中具有重要意义。
(4)N2和H2在催化剂表面合成気的微观历程如图所示,用 、
、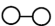 、
、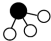 分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
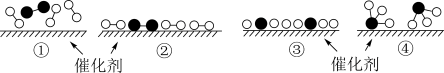
III.电池的发明是储能和供能技术的巨大进步,如图所示的原电池装置,插入电解质溶液前Cu和Fe电极质量相等。
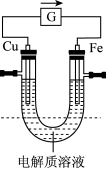
(5)电解质溶液为FeCl3时,图中箭头的方向表示___________ (填“电子”或“电流”)的流向,铁片上的电极反应式为___________ 。
(6)电解质溶液更换为X时,电极质量变化曲线如图所示。
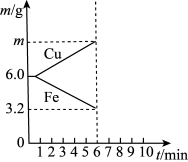
①X可以是___________ (填字母)。
A.稀硫酸 B.CuSO4溶液 C.稀盐酸 D.FeSO4溶液
②6 min时Cu电极的质量a为___________ g。
I.化学反应伴随能量变化。
(1)NH4HCO3和CH3COOH反应过程的能量变化如图所示,

(2)某实验小组设计了三套实验装置(如图),不能用来证明“NH4HCO3和CH3COOH反应能量变化情况”的是

(3)NH4HCO3和CH3COOH反应的离子方程式为
II.合成氨反应为放热反应,在化工生产中具有重要意义。
(4)N2和H2在催化剂表面合成気的微观历程如图所示,用
 、
、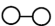 、
、 分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)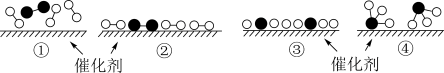
| A.反应过程存在非极性共价键的断裂和形成 |
| B.催化剂仅起到吸附N2和H2的作用,对化学反应速率没有影响 |
| C.②→③过程吸热 |
| D.反应物断键吸收的总能量小于生成物成键释放的总能量 |
III.电池的发明是储能和供能技术的巨大进步,如图所示的原电池装置,插入电解质溶液前Cu和Fe电极质量相等。

(5)电解质溶液为FeCl3时,图中箭头的方向表示
(6)电解质溶液更换为X时,电极质量变化曲线如图所示。

①X可以是
A.稀硫酸 B.CuSO4溶液 C.稀盐酸 D.FeSO4溶液
②6 min时Cu电极的质量a为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】甲醛(HCHO)在化工、医药、农药等方面有广泛的应用。
(1)甲醇脱氢法可制备甲醛,反应方程式为CH3OH⇌HCHO+H2。
①发生反应时的过程如图所示,从热效应角度判断,该反应为____ 反应。

②下列方法中能加快反应速率的是___ (填字母)。
a.使用催化剂 b.升高温度 c.降低反应物浓度
(2)甲醛超标会危害人体健康,需对甲醛含量检测及处理。
①某甲醛气体探测仪利用燃料电池工作原理,其结构如图所示。电极a为___ (填“正”或“负”)极,在电极b上发生的反应类型为___ 反应。(填“氧化”或“还原”)

②探测仪工作时,电子从__ 极流出(填“a”或“b”),总反应方程式为____ 。
(1)甲醇脱氢法可制备甲醛,反应方程式为CH3OH⇌HCHO+H2。
①发生反应时的过程如图所示,从热效应角度判断,该反应为

②下列方法中能加快反应速率的是
a.使用催化剂 b.升高温度 c.降低反应物浓度
(2)甲醛超标会危害人体健康,需对甲醛含量检测及处理。
①某甲醛气体探测仪利用燃料电池工作原理,其结构如图所示。电极a为

②探测仪工作时,电子从
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】“绿水青山就是金山银山”,运用化学反应原理缓解环境污染、能源危机具有重要意义。
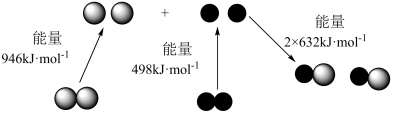
(1)汽车是近代重要的交通运输工具,随着汽车量的激增,汽车尾气造成的环境污染也日益严重。汽车尾气中的有害成分主要有CO、NO、SO2、颗粒物和臭氧等。汽车尾气中NO生成过程中的能量变化如上图所示。1molN2和1molO2完全反应生成NO会___________ (填“吸收”或“放出”)___________ kJ能量。
(2)煤燃烧排放的烟气中含有SO2和NO2,会形成酸雨,污染大气。
①NaClO2溶液在碱性条件下可对烟气进行脱硫、脱硝,效果非常好。脱硝过程生成Cl-、 ,写出烟气脱硝过程的离子方程式:
,写出烟气脱硝过程的离子方程式:___________
②针对含SO2的工业废气可以采用“钙基固硫法”。例如将生石灰与含硫的煤混合后再燃烧,可以将SO2最终转化为CaSO4,请写出生石灰将SO2转化为CaSO4的反应的化学方程式___________
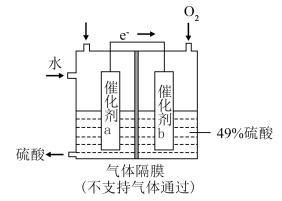
③将SO2转化为重要的化工原料H2SO4的原理示意图如图。催化剂a表面的电极反应式为___________ 。若得到的硫酸质量分数仍为49%,则理论上参加反应的SO2与加入的H2O的质量比为___________ 。

(1)汽车是近代重要的交通运输工具,随着汽车量的激增,汽车尾气造成的环境污染也日益严重。汽车尾气中的有害成分主要有CO、NO、SO2、颗粒物和臭氧等。汽车尾气中NO生成过程中的能量变化如上图所示。1molN2和1molO2完全反应生成NO会
(2)煤燃烧排放的烟气中含有SO2和NO2,会形成酸雨,污染大气。

①NaClO2溶液在碱性条件下可对烟气进行脱硫、脱硝,效果非常好。脱硝过程生成Cl-、
 ,写出烟气脱硝过程的离子方程式:
,写出烟气脱硝过程的离子方程式:②针对含SO2的工业废气可以采用“钙基固硫法”。例如将生石灰与含硫的煤混合后再燃烧,可以将SO2最终转化为CaSO4,请写出生石灰将SO2转化为CaSO4的反应的化学方程式
③将SO2转化为重要的化工原料H2SO4的原理示意图如图。催化剂a表面的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】学习小组利用草酸 溶液与
溶液与 溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行如下实验:
溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行如下实验:
已知:
回答下列问题:
(1)通过实验①、②,可探究_____ 的改变对化学反应速率的影响,其中
_____ ,
_____ 。
(2)通过实验_____ (填实验序号)可探究 变化对化学反应速率的影响,由此可以得出的实验结论是
变化对化学反应速率的影响,由此可以得出的实验结论是_____ 。
(3)实验③中, 内
内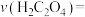
_____ (忽略溶液体积的变化,结果保留小数点后两位)。
(4)草酸溶液与酸性高锰酸钾溶液反应机理如图所示。 反应的离子方程式为
反应的离子方程式为_____ ;为验证催化剂对反应速率的影响,实验⑤中试剂 最好选用
最好选用_____ (填序号)。
a.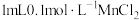 溶液
溶液
b. 溶液
溶液
c. 粉末
粉末
d. 粉末
粉末
 溶液与
溶液与 溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行如下实验:
溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行如下实验:| 实验序号 | 试验温度/K | 有关物质 | 紫色褪去所需时间 | ||||
  溶液 溶液 |   溶液 溶液 |   溶液 溶液 |  | 试剂X | |||
 |  |  |  | ||||
| ① | 298 | 2 | 4 | 1 | 1 | 无 |  |
| ② |  | 2 | 3 | 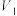 |  | 无 |  |
| ③ | 313 | 2 | 4 | 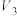 | 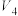 | 无 | 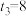 |
| ④ | 313 | 2 | 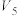 | 2 |  | 无 | 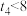 |
| ⑤ | 313 | 2 | 4 | 1 | 1 | 有 | 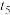 |

回答下列问题:
(1)通过实验①、②,可探究


(2)通过实验
 变化对化学反应速率的影响,由此可以得出的实验结论是
变化对化学反应速率的影响,由此可以得出的实验结论是(3)实验③中,
 内
内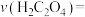
(4)草酸溶液与酸性高锰酸钾溶液反应机理如图所示。
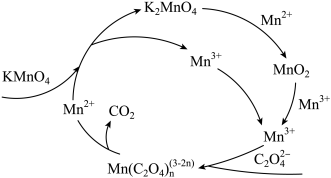
 反应的离子方程式为
反应的离子方程式为 最好选用
最好选用a.
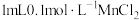 溶液
溶液b.
 溶液
溶液c.
 粉末
粉末d.
 粉末
粉末
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】作为一种绿色消毒剂, 在公共卫生事业中发挥了重要的作用。已知反应:
在公共卫生事业中发挥了重要的作用。已知反应: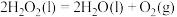 的能量变化如图。回答问题:
的能量变化如图。回答问题:

(1)该反应是_______ 反应(填“放热”或“吸热”)。
(2) 的电子式为
的电子式为____ , 对大多数致病菌和病毒具有消杀功能是因为其具有
对大多数致病菌和病毒具有消杀功能是因为其具有_____ 性。用3%医用 对传染病房喷洒消毒时,地板上有气泡冒出,该气体是
对传染病房喷洒消毒时,地板上有气泡冒出,该气体是_____ 。
(3)纯 可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下,
可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下, 剧烈分解:
剧烈分解: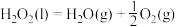 ,产生大量气体,驱动火箭升空。已知上图中
,产生大量气体,驱动火箭升空。已知上图中 的数值为196kJ,则每消耗34g
的数值为196kJ,则每消耗34g ,理论上放出热量
,理论上放出热量_______ 98kJ(填“大于”、“小于”或“等于”)。
(4)向 稀溶液中滴加数滴含Mn2+的溶液,即有气泡快速逸出,反应中Mn2+起
稀溶液中滴加数滴含Mn2+的溶液,即有气泡快速逸出,反应中Mn2+起_______ 作用。某组实验数据如下:
0-30min 反应的平均速率v=
反应的平均速率v=_______  。
。
(5)用10% 和
和 的
的 混合溶液将铜粉溶解,反应的离子方程式为
混合溶液将铜粉溶解,反应的离子方程式为_______ 。测得不同温度下铜的平均溶解速率如下表:
由表中数据可知,当温度高于40℃时,铜的平均溶解速率随着温度的升高而下降,其主要原因是_______ 。
 在公共卫生事业中发挥了重要的作用。已知反应:
在公共卫生事业中发挥了重要的作用。已知反应: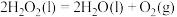 的能量变化如图。回答问题:
的能量变化如图。回答问题:
(1)该反应是
(2)
 的电子式为
的电子式为 对大多数致病菌和病毒具有消杀功能是因为其具有
对大多数致病菌和病毒具有消杀功能是因为其具有 对传染病房喷洒消毒时,地板上有气泡冒出,该气体是
对传染病房喷洒消毒时,地板上有气泡冒出,该气体是(3)纯
 可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下,
可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下, 剧烈分解:
剧烈分解: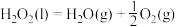 ,产生大量气体,驱动火箭升空。已知上图中
,产生大量气体,驱动火箭升空。已知上图中 的数值为196kJ,则每消耗34g
的数值为196kJ,则每消耗34g ,理论上放出热量
,理论上放出热量(4)向
 稀溶液中滴加数滴含Mn2+的溶液,即有气泡快速逸出,反应中Mn2+起
稀溶液中滴加数滴含Mn2+的溶液,即有气泡快速逸出,反应中Mn2+起| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
c( )/mol·L-1 )/mol·L-1 | 0.70 | 0.49 | 0.35 | 0.25 | 0.17 | 0.12 |
 反应的平均速率v=
反应的平均速率v= 。
。(5)用10%
 和
和 的
的 混合溶液将铜粉溶解,反应的离子方程式为
混合溶液将铜粉溶解,反应的离子方程式为| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
铜的平均溶解速率( ) ) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】I、2021年1月7日,我国首个探明储量超千亿方的深层页岩气田——中国石化西南石油局威荣页岩气田一期项目全面建成,对促进成渝地区双城经济圈建设具有重要意义。回答下列问题:
(1)页岩气的主要成分是甲烷。已知25℃,101kPa时甲烷的燃烧热为890.3 kJ·mol-1。请写出表示甲烷燃烧热的热化学方程式:______________________________________________ 。
(2)用甲烷可以合成乙烯:2CH4(g) C2H4(g) + 2H2(g) ΔH=+202 kJ·mol-1,该反应在
C2H4(g) + 2H2(g) ΔH=+202 kJ·mol-1,该反应在______ 下自发进行(填“高温”、“低温”或“任何温度”)。
II、在催化剂作用下由CO2和H2可直接合成乙烯:2CO2(g) + 6H2(g)⇌C2H4(g) + 4H2O(g) ΔH
(3)关于该反应,下列叙述正确的是 (填字母序号) 。
(4)在体积为2 L的恒容密闭容器中,加入2 mol CO2和6 mol H2,在催化剂作用下发生乙烯直接合成反应,测得温度对CO2的平衡转化率影响如图所示。
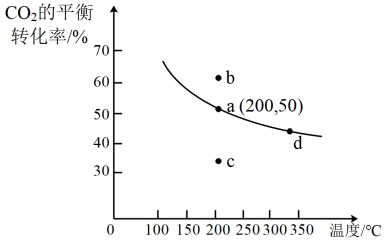
①已知在200℃下,10 min时反应达到平衡状态。则0~10min内用CO2表示的平均反应速率为_____ 。
②该反应的ΔH______ 0(填 “<”、“>” 或 “=”),请结合平衡移动原理简述理由_________________ 。
③若不使用催化剂,则200℃ 时CO2的平衡转化率位于图中的_____ 点(填“a”、“b”、“c”或“d”)。
(1)页岩气的主要成分是甲烷。已知25℃,101kPa时甲烷的燃烧热为890.3 kJ·mol-1。请写出表示甲烷燃烧热的热化学方程式:
(2)用甲烷可以合成乙烯:2CH4(g)
 C2H4(g) + 2H2(g) ΔH=+202 kJ·mol-1,该反应在
C2H4(g) + 2H2(g) ΔH=+202 kJ·mol-1,该反应在II、在催化剂作用下由CO2和H2可直接合成乙烯:2CO2(g) + 6H2(g)⇌C2H4(g) + 4H2O(g) ΔH
(3)关于该反应,下列叙述正确的是 (填字母序号) 。
| A.恒容下达平衡状态时,再充入少量氦气,正逆反应速率不变 |
| B.当混合气体的平均摩尔质量不再发生变化时,反应达平衡状态 |
| C.当反应达平衡状态时,3v正(H2) = 2v逆(H2O) |
| D.恒温下缩小容器体积,反应物的活化分子百分数增大 |

①已知在200℃下,10 min时反应达到平衡状态。则0~10min内用CO2表示的平均反应速率为
②该反应的ΔH
③若不使用催化剂,则200℃ 时CO2的平衡转化率位于图中的
您最近一年使用:0次



