下列事实能用勒夏特列原理解释的是。
| A.用排饱和食盐水的方法收集氯气 |
B.向 溶液中加入 溶液中加入 ,单位时间内产生 ,单位时间内产生 的量增多 的量增多 |
C. ,平衡后缩小容器体积气体颜色变深 ,平衡后缩小容器体积气体颜色变深 |
D.盛有 与稀 与稀 混合溶液的试管浸入热水中,溶液迅速变浑浊 混合溶液的试管浸入热水中,溶液迅速变浑浊 |
更新时间:2022-11-16 13:37:03
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列事实,不能用勒夏特列原理解释的是
| A.氯水中有下列平衡Cl2+H2 O⇌HCl + HClO,当加入AgNO3溶液后,溶液颜色变浅 |
| B.对2HI(g)⇌H2(g)+I2 (g),平衡体系增大压强可使颜色变深 |
| C.反应CO+NO2⇌CO2+NO ΔH <0,升高温度可使平衡向逆反应方向移动 |
| D.合成NH3反应,为提高NH3的产率,理论上应采取降低温度的措施 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列不能用勒夏特列原理解释的事实是
| A.红棕色的NO2加压后颜色先变深后变浅 |
| B.氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深 |
| C.黄绿色的氯水光照后颜色变浅 |
| D.向含有Fe(SCN)3的红色溶液中加铁粉,振荡,溶液红色变浅或褪去 |
您最近一年使用:0次

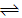 CO2(g)+NO(g) ΔH<0,升高温度可使平衡向逆反应方向移动
CO2(g)+NO(g) ΔH<0,升高温度可使平衡向逆反应方向移动

