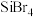主族元素N、F、Si、As、Se、Cl、Ti等的某些化合物对工农业生产意义重大,回答下列问题:
(1)Si3N4陶瓷是世界上最坚硬的物质之一,具有高强度、低密度、耐高温等性质,其属于_______ 晶体;高纯硅制备过程中会有SiHCl3、SiCl4等中间产物生成。沸点:SiHCl3_______ SiCl4(填“>”或“<”),SiCl4中Si采取的杂化类型为_______ 。
(2)O、F、Cl电负性由大到小的顺序为_______ ;OF2分子的空间构型为_______ ;OF2的熔、沸点低于Cl2O,原因是_______ 。
(3)Se元素基态原子的原子核外电子排布式为_______ ;As的第一电离能比Se的第一电离能大的原因为_______ 。
(4)时速600公里的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图) ,晶胞参数(晶胞边长)为aD(1D= 10 -10m) ,TiN的相对分子质量为M,该氮化钛晶体的密度_______ g· cm-3(列出计算式即可)。

(1)Si3N4陶瓷是世界上最坚硬的物质之一,具有高强度、低密度、耐高温等性质,其属于
(2)O、F、Cl电负性由大到小的顺序为
(3)Se元素基态原子的原子核外电子排布式为
(4)时速600公里的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图) ,晶胞参数(晶胞边长)为aD(1D= 10 -10m) ,TiN的相对分子质量为M,该氮化钛晶体的密度

更新时间:2022-11-03 15:11:42
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】Fe—Cr—Si系合金是一种新型耐磨耐腐蚀的材料,具有较好的发展前景。按要求回答下列问题。
(1)基态Cr2+与Fe的未成对电子数之比为___ 。试从电子排布角度分析水溶液中Fe2+具有强还原性___ 。若是形成将其转化为(NH4)2Fe(SO4)2,在空气中相对稳定, 的空间构型为
的空间构型为___ 。
(2)由环戊二烯(C5H6,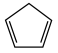 )与FeCl2在一定条件下反应得到二茂铁[双环戊二烯基合亚铁,Fe(C5H5)2],已知
)与FeCl2在一定条件下反应得到二茂铁[双环戊二烯基合亚铁,Fe(C5H5)2],已知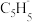 的空间构型为所有碳原子一定处于同一平面,指出碳原子的杂化形式为
的空间构型为所有碳原子一定处于同一平面,指出碳原子的杂化形式为___ ,结构中的大π键可用符号表示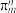 ,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为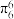 )。则
)。则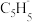 结构中含有的大π键可表示为
结构中含有的大π键可表示为___ 。
(3)某含铬配合物,[Cr3O(CH3COO)6(H2O)3]Cl·8H2O,指出其中Cr的化合价为___ 。几种Cr的卤化物的部分性质如表所示:
试预测CrBr3的熔点范围___ 。
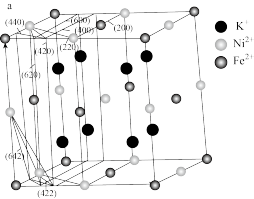
(4)某晶体中含有K+、Ni2+、Fe2+、CN-,其部分微粒在晶胞结构的位置如图所示。1个晶胞中含有CN-___ 个。该物质常用于吸附Cs+,将取代晶胞中的K+,取代后的物质的化学式为___ 。
(1)基态Cr2+与Fe的未成对电子数之比为
 的空间构型为
的空间构型为(2)由环戊二烯(C5H6,
 )与FeCl2在一定条件下反应得到二茂铁[双环戊二烯基合亚铁,Fe(C5H5)2],已知
)与FeCl2在一定条件下反应得到二茂铁[双环戊二烯基合亚铁,Fe(C5H5)2],已知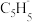 的空间构型为所有碳原子一定处于同一平面,指出碳原子的杂化形式为
的空间构型为所有碳原子一定处于同一平面,指出碳原子的杂化形式为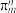 ,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为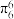 )。则
)。则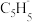 结构中含有的大π键可表示为
结构中含有的大π键可表示为(3)某含铬配合物,[Cr3O(CH3COO)6(H2O)3]Cl·8H2O,指出其中Cr的化合价为
| 卤化物 | CrCl3 | CrBr3 | CrI3 |
| 熔点/℃ | 1150 | 600 |
(4)某晶体中含有K+、Ni2+、Fe2+、CN-,其部分微粒在晶胞结构的位置如图所示。1个晶胞中含有CN-

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
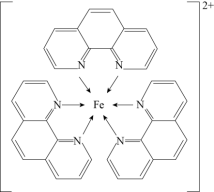
【推荐2】碳元素在自然界中分布很广,是存在形式最复杂的元素。实验室可用邻二氮菲(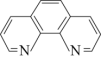 )与
)与 形成的红色配合物(如下图)测定铁的含量。
形成的红色配合物(如下图)测定铁的含量。
回答下列问题:
(1)基态Fe原子的价层电子排布式为_______ 。
(2)红色配合物中非金属元素的电负性从大到小的顺序为_______ 。
(3)邻二氮菲分子中C和N元素原子的杂化方式分别为_______ 、_______ 。
(4)红色配合物的中心原子的配位数为_______ 。
(5)上世纪末,科学家合成了硬度超过金刚石的 晶体,该晶体的硬度比金刚石大的原因是
晶体,该晶体的硬度比金刚石大的原因是_______ 。
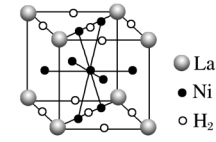
(6)如图是一种镍基合金储氢后的晶胞结构示意图。该合金储氢后,含1 mol La的合金含有Ni的数目为_______ 。
 )与
)与 形成的红色配合物(如下图)测定铁的含量。
形成的红色配合物(如下图)测定铁的含量。
回答下列问题:
(1)基态Fe原子的价层电子排布式为
(2)红色配合物中非金属元素的电负性从大到小的顺序为
(3)邻二氮菲分子中C和N元素原子的杂化方式分别为
(4)红色配合物的中心原子的配位数为
(5)上世纪末,科学家合成了硬度超过金刚石的
 晶体,该晶体的硬度比金刚石大的原因是
晶体,该晶体的硬度比金刚石大的原因是(6)如图是一种镍基合金储氢后的晶胞结构示意图。该合金储氢后,含1 mol La的合金含有Ni的数目为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】晶体氟化铅(PbF2)可用作红外线分光材料,其一种合成反应为2HF+PbCO3=PbF2+H2O+CO2↑。回答下列问题:
(1)Pb与C位于同一主族,其最外层电子排布式为___________ ;基态氟原子核外电子的运动状态有___________ 种。
(2)C、O、F的电负性由大到小的顺序为___________ ,理由为___________ 。
(3)CO2和 的杂化类型分别为
的杂化类型分别为___________ ;与 互为等电子体的分子和离子为
互为等电子体的分子和离子为___________ (填化学式,各写一种)。
(4)CO2与CH4均为含碳非极性分子,在水中的溶解度CO2___________ CH4(填“>”或“<”),原因为___________ 。
(5)PbF2晶体的堆积方式如图a,其中Pb原子的配位数为___________ ;图b为沿晶胞对角面取得的截图,已知,截面对角线为lnm,阿伏加德罗常数的值为NA,PbF2的密度为___________ (用含l和NA的代数式表示。)

(1)Pb与C位于同一主族,其最外层电子排布式为
(2)C、O、F的电负性由大到小的顺序为
(3)CO2和
 的杂化类型分别为
的杂化类型分别为 互为等电子体的分子和离子为
互为等电子体的分子和离子为(4)CO2与CH4均为含碳非极性分子,在水中的溶解度CO2
(5)PbF2晶体的堆积方式如图a,其中Pb原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】2019年1月3日,中国“嫦娥四号”探测器成功着陆在月球背面的预选着陆区,实现了人类探测器首次月被软着陆。“嫦娥四号”降落月球时的第一眼画面,由探测器搭载的降落相机拍摄。这个降落相机镜筒由钛合金制作。回答下列问题:
(1)Ti(BH4)2是一种储氢材料。
①基态Ti2+的价电子排布图(轨道表达式)为__________ ;钛元素位于周期表的_______ 区。
②BH4-的空间构型是_______________ ,B原子的杂化方式___________ 。
③BH4-中,含有___________ (填标号)。
a.σ键b.π键c.氢键d.配位键e.离子键
(2)与钛同周期的ⅡB族和ⅢA族两种元素中第一电离能较大的是___________ (写元素符号),原因是_________________________________ 。
(3)—种以金红石(主要成分TiO2)为原料生产金属钛的步骤主要有:在高温下,向金红石与焦炭的泡合物中通入Cl2,得到TiCl4和一种可燃性气体;然后在稀有气体氛围和加热的条件下,用镁与TiCl4反应可得到钛。
①请写出上述制备过程的化学方程式:___________________ 、_________________ 。
②中间产物TiCl4是一种洛剂,常温下呈液态,分子结构与CCl4相似,也能与CCl4均匀混合,请解释TiCl4与CCl4均匀混合的原因:_____________________________ 。
(4)单质钛与单质Zn、Mg的堆积方式相同,这种堆积方式称为:__________________ 。若钛原子半径为rpm,NA表示阿伏伽德罗常数的值,钛的密度为___________ g•cm-3(列出计算式)
(1)Ti(BH4)2是一种储氢材料。
①基态Ti2+的价电子排布图(轨道表达式)为
②BH4-的空间构型是
③BH4-中,含有
a.σ键b.π键c.氢键d.配位键e.离子键
(2)与钛同周期的ⅡB族和ⅢA族两种元素中第一电离能较大的是
(3)—种以金红石(主要成分TiO2)为原料生产金属钛的步骤主要有:在高温下,向金红石与焦炭的泡合物中通入Cl2,得到TiCl4和一种可燃性气体;然后在稀有气体氛围和加热的条件下,用镁与TiCl4反应可得到钛。
①请写出上述制备过程的化学方程式:
②中间产物TiCl4是一种洛剂,常温下呈液态,分子结构与CCl4相似,也能与CCl4均匀混合,请解释TiCl4与CCl4均匀混合的原因:
(4)单质钛与单质Zn、Mg的堆积方式相同,这种堆积方式称为:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】请完成下列各题的填空:
(1)氢化钠(NaH)电子式为_________ ,氢负离子的离子结构示意 图为_________
(2)元素X的最外层电子数是次外层电子数的3倍,该元素名称是_________ ,该元素核外电子排布式为_________ ,画出该元素的外围电子排布图_________
(3)前四周期元素中,未成对电子数为5的元素符号是_________ ,该元素在周期表中的位置为第_________ 周期,_________ 族、_________ 区
(4)C、N、O的第一电离能由大到小的顺序为_________ 。由这三种元素和氢原子共同组成的离子化合物的化学式为_________ (只写一件)
(5)碳酸根离子( )的VSEPR模型为
)的VSEPR模型为_________ ,其中心原子的轨道杂化方式为_________ 。
(1)氢化钠(NaH)电子式为
(2)元素X的最外层电子数是次外层电子数的3倍,该元素名称是
(3)前四周期元素中,未成对电子数为5的元素符号是
(4)C、N、O的第一电离能由大到小的顺序为
(5)碳酸根离子(
 )的VSEPR模型为
)的VSEPR模型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】硅烷广泛应用在现代高科技领域。制备硅烷的反应为 。
。
(1)①基态硅原子的价层电子轨道表示式为_______ 。
② 中,硅的化合价为+4价。硅显正化合价的原因是
中,硅的化合价为+4价。硅显正化合价的原因是_______ 。
③下列说法正确的是_______ (填序号)。
a. 的热稳定性比
的热稳定性比 的差
的差
b. 中4个
中4个 的键长相同,
的键长相同, 的键角为
的键角为
c. 中硅原子以4个
中硅原子以4个 杂化轨道分别与4个氢原子的
杂化轨道分别与4个氢原子的 轨道重叠,形成4个
轨道重叠,形成4个
 键
键
④ 的沸点(
的沸点(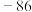 ℃)高于
℃)高于 的沸点(
的沸点( ℃),原因是
℃),原因是_______ 。
(2) 的晶胞结构如图所示,晶胞的体积为
的晶胞结构如图所示,晶胞的体积为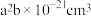 。
。
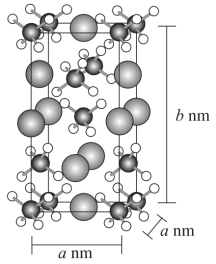
① 的VSEPR模型名称为
的VSEPR模型名称为_______ 。
②用 表示阿伏加德罗常数的值。
表示阿伏加德罗常数的值。 晶体密度为
晶体密度为_______  (用含a、b、
(用含a、b、 的代数式表示)。
的代数式表示)。
③ 是一种具有应用潜能的储氢材料,其释氢过程可用化学方程式表示为:
是一种具有应用潜能的储氢材料,其释氢过程可用化学方程式表示为: 。掺杂
。掺杂 替换晶体中部分
替换晶体中部分 ,更利于
,更利于 中H的解离,使体系更容易释放氢。从结构的角度推测其可能原因:
中H的解离,使体系更容易释放氢。从结构的角度推测其可能原因:_______ 。
 。
。(1)①基态硅原子的价层电子轨道表示式为
②
 中,硅的化合价为+4价。硅显正化合价的原因是
中,硅的化合价为+4价。硅显正化合价的原因是③下列说法正确的是
a.
 的热稳定性比
的热稳定性比 的差
的差b.
 中4个
中4个 的键长相同,
的键长相同, 的键角为
的键角为
c.
 中硅原子以4个
中硅原子以4个 杂化轨道分别与4个氢原子的
杂化轨道分别与4个氢原子的 轨道重叠,形成4个
轨道重叠,形成4个
 键
键④
 的沸点(
的沸点(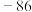 ℃)高于
℃)高于 的沸点(
的沸点( ℃),原因是
℃),原因是(2)
 的晶胞结构如图所示,晶胞的体积为
的晶胞结构如图所示,晶胞的体积为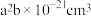 。
。
①
 的VSEPR模型名称为
的VSEPR模型名称为②用
 表示阿伏加德罗常数的值。
表示阿伏加德罗常数的值。 晶体密度为
晶体密度为 (用含a、b、
(用含a、b、 的代数式表示)。
的代数式表示)。③
 是一种具有应用潜能的储氢材料,其释氢过程可用化学方程式表示为:
是一种具有应用潜能的储氢材料,其释氢过程可用化学方程式表示为: 。掺杂
。掺杂 替换晶体中部分
替换晶体中部分 ,更利于
,更利于 中H的解离,使体系更容易释放氢。从结构的角度推测其可能原因:
中H的解离,使体系更容易释放氢。从结构的角度推测其可能原因:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是______ (填元素符号),其中C原子的核外电子排布式为__________ 。
(2)单质A有两种同素异形体,其中沸点高的是_____ (填分子式),原因是_______ ;
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为______ ,中心原子的杂化轨道类型为______ 。
(4)化合物D2A的立体构型为___ ,中心原子的价层电子对数为______ ,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为_________ 。
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm,晶胞中A原子的配位数为_________ ;列式计算晶体F的密度(g.cm-3)_____ 。

(1)四种元素中电负性最大的是
(2)单质A有两种同素异形体,其中沸点高的是
(3)C和D反应可生成组成比为1:3的化合物E,E的立体构型为
(4)化合物D2A的立体构型为
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数,a=0.566nm,晶胞中A原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】
翡翠的主要成分为 NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅。
(1) NaAlSi2O6所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物是___________ (写化学式)
(2)基态Cr3+的核外电子排布式为_____________________ 。
(3)配合物K[Cr(C2O4)2(H2O)中的配体是___________ ,C2O42-中碳原子的杂化轨道类型是___________ ,与H2O互为等电子体的离子是___________ (任写一种)
(4)一种铝镍合金的晶胞结构如图所示,与其结构相似的化合物是___________ (填标号)。

a.氟化钙 b.金刚石 c.钠 d.氯化铯
(5)Ca、O、Gr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中Ca2+,O2-采用面心立方最密堆积方式。
①该晶体的化学式为___________ 。
②已知钙离子、氧离子半径分别为100pm、140pm,该晶胞的参数(边长)为___________ pm。
③阿伏伽德罗常数的值为NA,该晶体密度的计算表达式为___________ g·cm-3;晶胞中Cr4+位于O2-所形成的正八面体的体心,该正八面体的边长为___________ pm。
翡翠的主要成分为 NaAlSi2O6,还含有其他多种金属阳离子,其中Cr3+的含量决定其绿色的深浅。
(1) NaAlSi2O6所含元素中,第一电离能最小的元素和电负性最大的元素组成的含有两种化学键的化合物是
(2)基态Cr3+的核外电子排布式为
(3)配合物K[Cr(C2O4)2(H2O)中的配体是
(4)一种铝镍合金的晶胞结构如图所示,与其结构相似的化合物是

a.氟化钙 b.金刚石 c.钠 d.氯化铯
(5)Ca、O、Gr可以形成一种具有特殊导电性的复合氧化物,晶胞结构如图所示,其中Ca2+,O2-采用面心立方最密堆积方式。
①该晶体的化学式为
②已知钙离子、氧离子半径分别为100pm、140pm,该晶胞的参数(边长)为
③阿伏伽德罗常数的值为NA,该晶体密度的计算表达式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
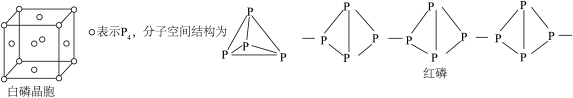
【推荐3】磷的单质及其化合物用途非常广泛。回答下列问题:
(1)白磷晶胞属于面心立方最密堆积,每个 周围距离最近的
周围距离最近的 个数为
个数为___________ ;白磷隔绝空气加热转化为红磷,红磷是巨型分子,无定型结构,能证明白磷是晶体的实验验证方法是___________ 。
(2)黑磷晶体是一种新型材料,其中正交型黑磷具有类似石墨的片层结构。每一层内P原子形成六元环彼此相接,每个空间六元环中平均含有的P原子个数为___________ 。白磷和正交型黑磷相比,熔点较高的是___________ ,原因是___________ 。
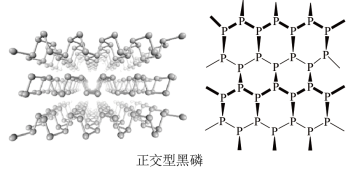
(3)BP是一种超硬耐磨涂层材料,晶胞结构与金刚石晶胞相似,其晶胞可看作金刚石晶胞内部的C原子被B原子替代,顶点和面心的C原子被P原子替代,晶胞参数为apm。沿z轴从上往下俯视的晶胞投影图如下所示。
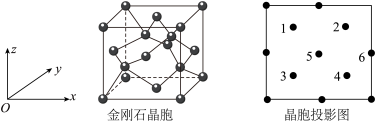
①投影图中原子5代表___________ 原子(填“P”或“B”)。
②若投影图中原子1的分数坐标是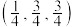 ,则原子6的分数坐标是
,则原子6的分数坐标是___________ ,原子1、6之间的距离为___________ pm。
(1)白磷晶胞属于面心立方最密堆积,每个
 周围距离最近的
周围距离最近的 个数为
个数为
(2)黑磷晶体是一种新型材料,其中正交型黑磷具有类似石墨的片层结构。每一层内P原子形成六元环彼此相接,每个空间六元环中平均含有的P原子个数为

(3)BP是一种超硬耐磨涂层材料,晶胞结构与金刚石晶胞相似,其晶胞可看作金刚石晶胞内部的C原子被B原子替代,顶点和面心的C原子被P原子替代,晶胞参数为apm。沿z轴从上往下俯视的晶胞投影图如下所示。

①投影图中原子5代表
②若投影图中原子1的分数坐标是
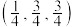 ,则原子6的分数坐标是
,则原子6的分数坐标是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】ⅣA族元素及其化合物在材料等方面有重要用途。回答下列问题:
(1)碳的一种单质的结构如图(a)所示。该单质的晶体类型为________ ,依据电子云的重叠方式,原子间存在的共价键类型有________ ,碳原子的杂化轨道类型为________ 。
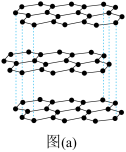
(2)石墨烯是从石墨材料中剥离出来的、由单质碳原子组成的二维晶体。将氢气加入石墨烯中可制得一种新材料石墨烷。下列判断错误的是________ (填字母)。
a.石墨烯是一种强度很高的材料
b.石墨烯是电的良导体而石墨烷则为绝缘体
c.石墨烯与石墨烷均为高分子化合物
d.石墨烯与H2制得石墨烷的反应属于加成反应
(3)CH4、SiH4、GeH4的熔、沸点依次________ (填“增大”或“减小”),其原因是_________ 。
(4)SiO2比CO2熔点高的原因是____________________________________________________ 。
(5)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图(b)所示。
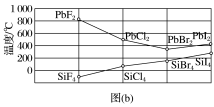
①SiX4的沸点依F、Cl、Br、I次序升高的原因是_____________________________________ 。
②结合SiX4的沸点和PbX2的熔点的变化规律,可推断:依F、Cl、Br、I次序,PbX2中的化学键的离子性________ 、共价性________ 。(填“增强”“不变”或“减弱”)
(6)水杨酸第一级电离形成离子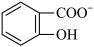 ,相同温度下,水杨酸的Ka2
,相同温度下,水杨酸的Ka2________ (填“>”“=”或“<”)苯酚(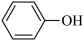 )的Ka,其原因是
)的Ka,其原因是__________________________ 。
(7)碳的另一种单质C60可以与钾形成低温超导化合物,晶体结构如图(c)所示,K位于立方体的棱上和立方体的内部,此化合物的化学式为________ ;其晶胞参数为1.4 nm,阿伏加 德罗常数用NA表示,则晶体的密度为__________ g·cm-3。(只需列出式子)
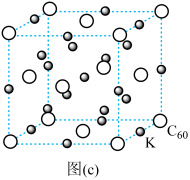
(1)碳的一种单质的结构如图(a)所示。该单质的晶体类型为

(2)石墨烯是从石墨材料中剥离出来的、由单质碳原子组成的二维晶体。将氢气加入石墨烯中可制得一种新材料石墨烷。下列判断错误的是
a.石墨烯是一种强度很高的材料
b.石墨烯是电的良导体而石墨烷则为绝缘体
c.石墨烯与石墨烷均为高分子化合物
d.石墨烯与H2制得石墨烷的反应属于加成反应
(3)CH4、SiH4、GeH4的熔、沸点依次
(4)SiO2比CO2熔点高的原因是
(5)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图(b)所示。

①SiX4的沸点依F、Cl、Br、I次序升高的原因是
②结合SiX4的沸点和PbX2的熔点的变化规律,可推断:依F、Cl、Br、I次序,PbX2中的化学键的离子性
(6)水杨酸第一级电离形成离子
 ,相同温度下,水杨酸的Ka2
,相同温度下,水杨酸的Ka2 )的Ka,其原因是
)的Ka,其原因是(7)碳的另一种单质C60可以与钾形成低温超导化合物,晶体结构如图(c)所示,K位于立方体的棱上和立方体的内部,此化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】硅和卤素单质反应可以得到 。
。
 的熔沸点
的熔沸点
(1)①沸点依次升高的原因是______ ,②气态 分子的空间构型是
分子的空间构型是______ ;
(2) 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应的键角如图甲所示。
的空间结构和相应的键角如图甲所示。 中P的杂化类型是
中P的杂化类型是______ 。
② 的沸点比
的沸点比 的
的______ (高或者低),原因是______ 。
(3)① 的空间构型为
的空间构型为______ (用文字描述);抗坏血酸的分子结构如图乙所示,分子中碳原子的轨道杂化类型为②______ ;③推测抗坏血酸在水中的溶解性______ (填“难溶于水”或“易溶于水”)。
 。
。 的熔沸点
的熔沸点
|
|
|
| |
熔点/K | 183.0 | 203.2 | 278.6 | 393.7 |
沸点/K | 187.2 | 330.8 | 427.2 | 560.7 |
(1)①沸点依次升高的原因是
 分子的空间构型是
分子的空间构型是(2)
 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应的键角如图甲所示。
的空间结构和相应的键角如图甲所示。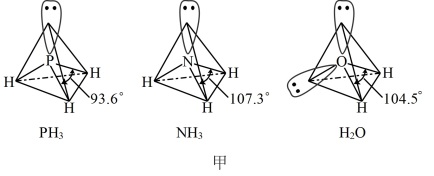
 中P的杂化类型是
中P的杂化类型是②
 的沸点比
的沸点比 的
的(3)①
 的空间构型为
的空间构型为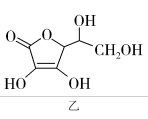
您最近一年使用:0次
【推荐3】已知A、B、C、D、E、F都是元素周期表前四周期的元素,它们的核电荷数:B<A<C<D<E<F。B、C两种元素都能引起水体富营养化。E原子得到一个电子后3p轨道全充满。A+比E原子形成的离子少1个电子层。D可以形成两种氧化物,其中一种氧化物是形成酸雨的主要气体之一。F的原子序数为26。请回答下列问题:
(1)C、D、E的第一电离能由小到大的顺序为________ (用元素符号表示)。
(2)写出B的氢化物与水反应的离子方程式:________________ ,B的氢化物极易溶于水的原因是____________________________________________________________ 。
(3)化合物BE3的分子空间构型为________________ 。
(4)F元素原子的核外电子排布式为________ 。F的一种常见化合物F(CO)5在常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,则F(CO)5的晶体类型为__________________ 。
(5)将FE3的饱和溶液滴入沸水中,请写出有关反应的离子方程式:___________________________ 。
(6)比较B、C两种元素的氢化物稳定性并说明理由:____________________ 。
(1)C、D、E的第一电离能由小到大的顺序为
(2)写出B的氢化物与水反应的离子方程式:
(3)化合物BE3的分子空间构型为
(4)F元素原子的核外电子排布式为
(5)将FE3的饱和溶液滴入沸水中,请写出有关反应的离子方程式:
(6)比较B、C两种元素的氢化物稳定性并说明理由:
您最近一年使用:0次