设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A. 苯乙烯( 苯乙烯(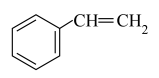 )含有 )含有 键数目为 键数目为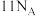 |
B. 中心原子上的价层电子对数目为 中心原子上的价层电子对数目为 |
C.在氢氧碱性燃料电池中,当正极上消耗 气体时,转移的电子数为 气体时,转移的电子数为 |
D. 由 由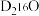 和 和 组成的混合物中含有的电子数为 组成的混合物中含有的电子数为 |
22-23高三上·辽宁沈阳·阶段练习 查看更多[2]
更新时间:2022-11-15 09:02:23
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】NA为阿伏伽德罗常数的值。参阅表中数据,下列判断在标准状况下正确的是
| NO2 | HF | |
| 熔点/℃ | -11.2 | -83.6 |
| 沸点/℃ | 21.0 | 19.52 |
| A.2.0gHF中含电子数目为l.0NA |
| B.12g石墨烯(单层石墨)中含有六元环个数为NA |
| C.6.72LNO2与水反应后,转移的电子数为0.2NA |
| D.NO和O2各2.24L充分反应后所得混合物体系中含分子数为0.1NA |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】用NA表示阿伏加 德罗常数的值。下列叙述正确的是
| A.标准状态下,33.6L氟化氢中含有1.5NA个氟化氢分子 |
| B.电解精炼铜时,若转移了NA个电子,则阴极析出32g铜 |
| C.在反应KClO3+6HCl===KCl+3Cl2↑+3H2O中,每生成3molCl2转移的电子数为6NA |
| D.25℃时,pH=13的氢氧化钡溶液中含有0.1NA个氢氧根离子 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】用NA表示阿伏伽德罗常数的值,下列叙述正确的是
| A.0.5mol/L MgCl2溶液,含有Cl-离子数为NA |
| B.在常温常压下,1g H2含有的分子数为0.5NA |
| C.含有NA个氦原子的氦气在标准状况下的体积为11.2L |
| D.标准状况下,11.2 L 酒精含有的分子数为0.5 NA |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】过二硫酸钾( ,其中S为
,其中S为 价)是工业上一种重要的消毒剂和织物漂白剂,可通过电解
价)是工业上一种重要的消毒剂和织物漂白剂,可通过电解 溶液制备。它在100℃下能发生分解反应:
溶液制备。它在100℃下能发生分解反应: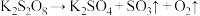 (未配平),设
(未配平),设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 ,其中S为
,其中S为 价)是工业上一种重要的消毒剂和织物漂白剂,可通过电解
价)是工业上一种重要的消毒剂和织物漂白剂,可通过电解 溶液制备。它在100℃下能发生分解反应:
溶液制备。它在100℃下能发生分解反应: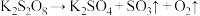 (未配平),设
(未配平),设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.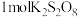 中含有非极性共价键的数目为 中含有非极性共价键的数目为 |
B. 分解,生成 分解,生成 的分子数为 的分子数为 |
C.标准状况下,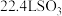 含有的原子数为 含有的原子数为 |
D.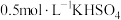 溶液中的离子总数为 溶液中的离子总数为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】向含 的溶液中通入一定体积的
的溶液中通入一定体积的 使其充分反应,再向所得溶液中逐滴滴加稀盐酸。测得产生
使其充分反应,再向所得溶液中逐滴滴加稀盐酸。测得产生 的物质的量随加入
的物质的量随加入 的物质的量变化如图所示。则下列说法错误的是
的物质的量变化如图所示。则下列说法错误的是
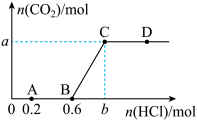
 的溶液中通入一定体积的
的溶液中通入一定体积的 使其充分反应,再向所得溶液中逐滴滴加稀盐酸。测得产生
使其充分反应,再向所得溶液中逐滴滴加稀盐酸。测得产生 的物质的量随加入
的物质的量随加入 的物质的量变化如图所示。则下列说法错误的是
的物质的量变化如图所示。则下列说法错误的是
A.A点之前发生的离子反应为 |
B.图中的 |
C.在D点对应的溶液中, 不能大量共存 不能大量共存 |
D.向氢氧化钠溶液中通入 的体积为 的体积为 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在下列物质中,其物质的量为0.2mol的是
| A.4.4gCO2 | B.49gH2SO4 | C.3.2gO2 | D.3.6gH2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】在一定条件下活性铁粉与氨气反应合成半导体材料:8Fe(s)+2NH3(g) 2Fe4N(s)+3H2(g),下列有关NH3、H2的推断正确的是
2Fe4N(s)+3H2(g),下列有关NH3、H2的推断正确的是
 2Fe4N(s)+3H2(g),下列有关NH3、H2的推断正确的是
2Fe4N(s)+3H2(g),下列有关NH3、H2的推断正确的是| A.上述参加反应的NH3和生成H2的体积之比为3∶2 |
| B.同温同压下,NH3、H2的密度之比为2∶17 |
| C.相同质量的NH3、H2分子数之比为17∶2 |
| D.同温同体积下,相同质量NH3、H2的压强之比为2∶17 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】我国科学家最近成功合成了世界上首个五氮阴离子盐 (用R代表)。经X射线衍射测得化合物R的晶体局部结构如图所示(已知
(用R代表)。经X射线衍射测得化合物R的晶体局部结构如图所示(已知 是平面结构)。下列说法不正确的是
是平面结构)。下列说法不正确的是
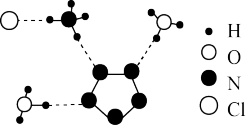
 (用R代表)。经X射线衍射测得化合物R的晶体局部结构如图所示(已知
(用R代表)。经X射线衍射测得化合物R的晶体局部结构如图所示(已知 是平面结构)。下列说法不正确的是
是平面结构)。下列说法不正确的是
| A.化合物R中存在极性键和非极性键 |
| B.化合物R中存在氢键 |
C. 中氧原子采取 中氧原子采取 杂化, 杂化, 中氮原子采取 中氮原子采取 杂化 杂化 |
D.阴离子 中氮原子是 中氮原子是 杂化 杂化 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】观察下列模型并结合信息,判断有关说法错误的是
| 晶体硼结构单元(有12个B原子) |  |  分子 分子 | HCN | |
| 结构模型示意图 |
|
|
|
|
A.晶体硼的结构单元中含有30个 键,含20个正三角形 键,含20个正三角形 |
B. 结构中键角1、2、3由大到小的顺序:3>1>2 结构中键角1、2、3由大到小的顺序:3>1>2 |
C.固态硫 中S原子为 中S原子为 杂化 杂化 |
D. 的结构式为 的结构式为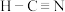 |
您最近一年使用:0次

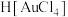 ),其化学方程式为:
),其化学方程式为: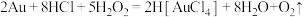 。设
。设
 分子数为
分子数为
 ,产物中形成的配位键数目为
,产物中形成的配位键数目为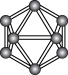

 的价电子对分布的几何构型与分子的空间结构不一致
的价电子对分布的几何构型与分子的空间结构不一致

