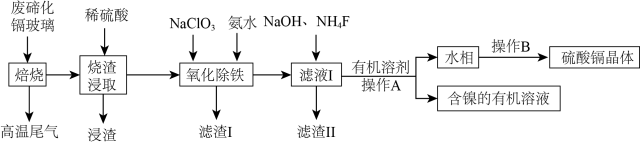
碲化镉玻璃中主要含有CdTe(其中含有少量Fe、Ni、Mg、Si、O等元素组成的化合物),工业上利用废弃碲化镉(CdTe)玻璃回收其中金属的工艺流程如下。
已知:①常温时,有关物质的 如下表。
如下表。
②当溶液中离子浓度小于 时,可认为沉淀完全。
时,可认为沉淀完全。
回答下列问题:
(1)在“焙烧”时为提高效率可采用的措施有_______ (答出一条即可)。写出“浸渣”的工业用途:_______ 。
(2)实验室中,“操作A”需要的玻璃仪器有_______ 。“高温尾气”中的 在水溶液中可用
在水溶液中可用 将其还原为Te单质,写出该反应的化学方程式:
将其还原为Te单质,写出该反应的化学方程式:_______ 。
(3)“氧化除铁”步骤中可以先调节pH为5,然后再加入 ,则此时
,则此时 被氧化的离子方程式为
被氧化的离子方程式为_______ 。
(4)测得“滤液I”中 浓度为
浓度为 ,取1L滤液,则至少加入
,取1L滤液,则至少加入_______ g 固体才能使
固体才能使 沉淀完全。
沉淀完全。

已知:①常温时,有关物质的
 如下表。
如下表。 |  |  |  |  |
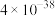 | 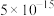 | 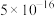 |  | 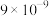 |
②当溶液中离子浓度小于
 时,可认为沉淀完全。
时,可认为沉淀完全。回答下列问题:
(1)在“焙烧”时为提高效率可采用的措施有
(2)实验室中,“操作A”需要的玻璃仪器有
 在水溶液中可用
在水溶液中可用 将其还原为Te单质,写出该反应的化学方程式:
将其还原为Te单质,写出该反应的化学方程式:(3)“氧化除铁”步骤中可以先调节pH为5,然后再加入
 ,则此时
,则此时 被氧化的离子方程式为
被氧化的离子方程式为(4)测得“滤液I”中
 浓度为
浓度为 ,取1L滤液,则至少加入
,取1L滤液,则至少加入 固体才能使
固体才能使 沉淀完全。
沉淀完全。
更新时间:2022-11-30 19:36:50
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】电子工业中,可用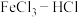 溶液作为印刷电路铜板刻蚀液。某探究小组设计如下线路处理废液和资源回收:
溶液作为印刷电路铜板刻蚀液。某探究小组设计如下线路处理废液和资源回收:
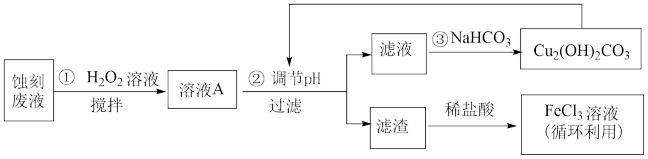
回答下列问题:
(1)把 溶液蒸干、灼烧,最后得到的主要固体产物是
溶液蒸干、灼烧,最后得到的主要固体产物是___________ 。(填写化学式)
(2) 蚀刻液中加入盐酸的目的是
蚀刻液中加入盐酸的目的是___________ 。
(3)步骤①中加入 溶液的目的是(用离子方程式表示)
溶液的目的是(用离子方程式表示)___________ 。
(4)已知:生成氢氧化物沉淀的pH如下表。
根据表中数据推测调节pH的范围是___________ 。
(5)上述流程路线中,除 溶液外,还可用于循环利用的物质是
溶液外,还可用于循环利用的物质是___________ 。
(6)在25℃下,向浓度均为 的
的 溶液中逐滴加入氨水,此离子沉淀完全(离子浓度≤
溶液中逐滴加入氨水,此离子沉淀完全(离子浓度≤ )时溶液的pH为
)时溶液的pH为___________ (已知25℃时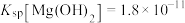 )。
)。
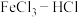 溶液作为印刷电路铜板刻蚀液。某探究小组设计如下线路处理废液和资源回收:
溶液作为印刷电路铜板刻蚀液。某探究小组设计如下线路处理废液和资源回收:
回答下列问题:
(1)把
 溶液蒸干、灼烧,最后得到的主要固体产物是
溶液蒸干、灼烧,最后得到的主要固体产物是(2)
 蚀刻液中加入盐酸的目的是
蚀刻液中加入盐酸的目的是(3)步骤①中加入
 溶液的目的是(用离子方程式表示)
溶液的目的是(用离子方程式表示)(4)已知:生成氢氧化物沉淀的pH如下表。
 |  |  | |
| 开始沉淀时 | 4.7 | 7.0 | 1.9 |
| 沉淀完全时 | 6.7 | 9.0 | 3.2 |
(5)上述流程路线中,除
 溶液外,还可用于循环利用的物质是
溶液外,还可用于循环利用的物质是(6)在25℃下,向浓度均为
 的
的 溶液中逐滴加入氨水,此离子沉淀完全(离子浓度≤
溶液中逐滴加入氨水,此离子沉淀完全(离子浓度≤ )时溶液的pH为
)时溶液的pH为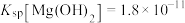 )。
)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】资源的合理利用,有利于社会的可持续发展。 的回收的工艺流程可以锌锰废电池中碳包(含碳粉、Fe、Cu、Ag和
的回收的工艺流程可以锌锰废电池中碳包(含碳粉、Fe、Cu、Ag和 等物质)为原料:
等物质)为原料:
I.将碳包中物质烘干,用足量稀 溶解金属单质,过滤,得滤渣a;
溶解金属单质,过滤,得滤渣a;
II.将滤渣a在空气中灼烧,得到粗 ;
;
III.向粗 中加入酸性
中加入酸性 溶液,
溶液, 溶解生成
溶解生成 ,有气体生成;
,有气体生成;
IV.向III所得溶液(pH约为6)中缓慢滴加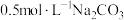 溶液(pH约为12),过滤,得滤渣b,其主要成分为
溶液(pH约为12),过滤,得滤渣b,其主要成分为 ;
;
V.滤渣b经洗涤、干燥、灼烧,制得较纯的 。
。
(1)I:Ag与足量稀 反应生成NO的化学方程式为
反应生成NO的化学方程式为_______ 。
(2)II:灼烧的目的是为了除去_______ 。
(3)III: 溶解的离子方程式为
溶解的离子方程式为_______ 。溶解一定量的 时,
时, 的实际消耗量比理论值高,用化学方程式解释原因:
的实际消耗量比理论值高,用化学方程式解释原因:_______ 。
(4)IV:若实验条件改为“向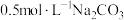 溶液中缓慢滴加III所得溶液”,滤渣b中可能会混有较多的
溶液中缓慢滴加III所得溶液”,滤渣b中可能会混有较多的_______ 杂质(填化学式)。
(5)V: 在空气中灼烧的化学方程式为
在空气中灼烧的化学方程式为_______ 。
 的回收的工艺流程可以锌锰废电池中碳包(含碳粉、Fe、Cu、Ag和
的回收的工艺流程可以锌锰废电池中碳包(含碳粉、Fe、Cu、Ag和 等物质)为原料:
等物质)为原料:I.将碳包中物质烘干,用足量稀
 溶解金属单质,过滤,得滤渣a;
溶解金属单质,过滤,得滤渣a;II.将滤渣a在空气中灼烧,得到粗
 ;
;III.向粗
 中加入酸性
中加入酸性 溶液,
溶液, 溶解生成
溶解生成 ,有气体生成;
,有气体生成;IV.向III所得溶液(pH约为6)中缓慢滴加
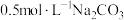 溶液(pH约为12),过滤,得滤渣b,其主要成分为
溶液(pH约为12),过滤,得滤渣b,其主要成分为 ;
;V.滤渣b经洗涤、干燥、灼烧,制得较纯的
 。
。(1)I:Ag与足量稀
 反应生成NO的化学方程式为
反应生成NO的化学方程式为(2)II:灼烧的目的是为了除去
(3)III:
 溶解的离子方程式为
溶解的离子方程式为 时,
时, 的实际消耗量比理论值高,用化学方程式解释原因:
的实际消耗量比理论值高,用化学方程式解释原因:(4)IV:若实验条件改为“向
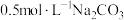 溶液中缓慢滴加III所得溶液”,滤渣b中可能会混有较多的
溶液中缓慢滴加III所得溶液”,滤渣b中可能会混有较多的(5)V:
 在空气中灼烧的化学方程式为
在空气中灼烧的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】穿甲弹的弹芯用钨合金制造。工业上以黑钨矿(主要成分是FeWO4、MnWO4,含少量的Fe2O3、SiO2)为原料冶炼钨的流程如图所示。
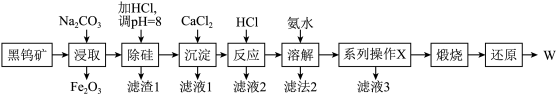
已知:钨酸H2WO4难溶于水。
回答下列问题:
(1)浸取在加热、通空气条件下进行,FeWO4转化为Na2WO4的化学方程式为________________ 。
(2)“滤渣1”的成分为________ 。除硅时,加入稀盐酸调节pH时,如果pH太低,钨的产率会降低,其原因是________________ 。
(3)“系列操作X”的目的是去除部分氨,使(NH4)2WO4转化为仲钨酸铵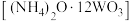 析出并分离,则该系列操作是
析出并分离,则该系列操作是________________ 。
(4)已知:含大量钨酸钙固体的溶液中存在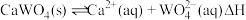 。
。 时,
时,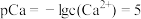 ,当温度升高至
,当温度升高至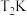 时,
时, ,则
,则
________ (填“ ”“
”“ ”或“
”或“ ”)0。
”)0。

已知:钨酸H2WO4难溶于水。
回答下列问题:
(1)浸取在加热、通空气条件下进行,FeWO4转化为Na2WO4的化学方程式为
(2)“滤渣1”的成分为
(3)“系列操作X”的目的是去除部分氨,使(NH4)2WO4转化为仲钨酸铵
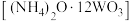 析出并分离,则该系列操作是
析出并分离,则该系列操作是(4)已知:含大量钨酸钙固体的溶液中存在
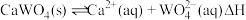 。
。 时,
时,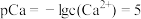 ,当温度升高至
,当温度升高至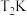 时,
时, ,则
,则
 ”“
”“ ”或“
”或“ ”)0。
”)0。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
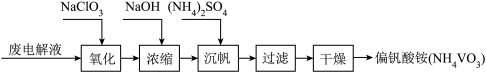
【推荐1】钒电池是一种新型酸性硫酸盐二次电池,钒电池失效后,废电解液回收利用的一种工艺如下:
已知:a.+5价钒在溶液中存在如下平衡: 。
。
b.部分含钒物质在水中的溶解性见下表:
(1)氧化工序中,其他价态的钒全部氧化成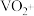 ,完成
,完成 氧化的离子方程式:
氧化的离子方程式:
_________ V2++_________ ClO3-+ _________ =_________ VO2+__________ C1-+ __________ NaClO和NaClO3均可作氧化剂,该工序中不选择NaClO作氧化剂的理由是_________ 。
(2)浓缩工序中,加入NaOH的作用是_________ 。
(3)沉钒工序的化学方程式为_________ 。
(4)煅烧偏钒酸铵时,固体(取234g NH4VO3)质量的减少量随温度变化的曲线如图所示,100~200℃时产生的一种气体的电子式为________ ,300~350℃时发生反应的化学方程式为__________ 。

已知:a.+5价钒在溶液中存在如下平衡:
 。
。b.部分含钒物质在水中的溶解性见下表:
| 物质 | VOSO4 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 易溶 |
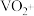 ,完成
,完成 氧化的离子方程式:
氧化的离子方程式:(2)浓缩工序中,加入NaOH的作用是
(3)沉钒工序的化学方程式为
(4)煅烧偏钒酸铵时,固体(取234g NH4VO3)质量的减少量随温度变化的曲线如图所示,100~200℃时产生的一种气体的电子式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】某工厂利用制革工业污泥[含Cr(III)]制取CrOH(H2O)5SO4的工艺流程如下:
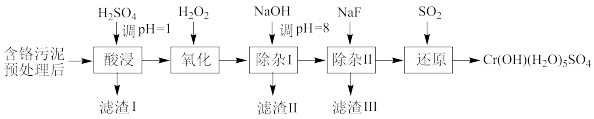
已知:酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+等。
(1)酸浸时,为了提高浸取率可采取的措施有_______ 。
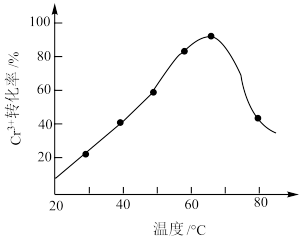
(2)H2O2的作用是将滤液中的Cr3+转化为Cr2O ,控制其他条件不变,在相同时间内,测得温度对Cr3+转化率的影响如图所示。请分析温度超过70°C时,Cr3+转化率下降的原因是
,控制其他条件不变,在相同时间内,测得温度对Cr3+转化率的影响如图所示。请分析温度超过70°C时,Cr3+转化率下降的原因是_______ 。
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
①滤渣II的主要成分为_______ (填化学式)。
②用NaOH调节溶液的pH不能超过8,其理由是_______ 。
(4)在“除杂II”中,当溶液中镁离子和钙离子沉淀完全时,所得溶液中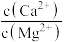 =
=_______ 。(已知:Ksp(CaF2)=1.48×10-10,Ksp(MgF2)=7.40×10-11)
(5)上述流程中,加入NaOH溶液后,溶液呈碱性,Cr2O 气转化为CrO
气转化为CrO ,写出上述流程中的“还原”过程生成CrOH(H2O)5SO4沉淀的离子方程式
,写出上述流程中的“还原”过程生成CrOH(H2O)5SO4沉淀的离子方程式_______ 。

已知:酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+等。
(1)酸浸时,为了提高浸取率可采取的措施有
(2)H2O2的作用是将滤液中的Cr3+转化为Cr2O
 ,控制其他条件不变,在相同时间内,测得温度对Cr3+转化率的影响如图所示。请分析温度超过70°C时,Cr3+转化率下降的原因是
,控制其他条件不变,在相同时间内,测得温度对Cr3+转化率的影响如图所示。请分析温度超过70°C时,Cr3+转化率下降的原因是
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
| 阳离子 | Fe3+ | Al3+ | Mg2+ | Ca2+ |
| 开始沉淀时的pH | 1.5 | 3.4 | 8.9 | 11.9 |
| 沉淀完全时的pH | 2.8 | 4.7(>8溶解) | 10.9 | 14 |
②用NaOH调节溶液的pH不能超过8,其理由是
(4)在“除杂II”中,当溶液中镁离子和钙离子沉淀完全时,所得溶液中
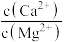 =
=(5)上述流程中,加入NaOH溶液后,溶液呈碱性,Cr2O
 气转化为CrO
气转化为CrO ,写出上述流程中的“还原”过程生成CrOH(H2O)5SO4沉淀的离子方程式
,写出上述流程中的“还原”过程生成CrOH(H2O)5SO4沉淀的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某化学小组利用 与
与 制取无水
制取无水 (夹持装置和部分加热装置略),同时产生光气(
(夹持装置和部分加热装置略),同时产生光气( )。
)。
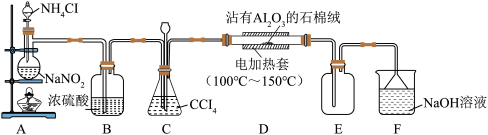
已知: 是白色粉末;
是白色粉末; 是淡黄色粉末,易吸水,熔点为190℃;
是淡黄色粉末,易吸水,熔点为190℃; 沸点为76.8℃,易挥发;
沸点为76.8℃,易挥发; 是有毒气体,易水解,易与碱反应。
是有毒气体,易水解,易与碱反应。
回答下列问题:
(1)装置A的作用是___________ ,上述装置存在的缺陷是___________ 。
(2)仪器药品准备完毕后进行的步骤为:①点燃A处酒精灯,一段时间后将A处酒精灯熄灭;
②……
③加热装置D至玻璃管中固体全部变为淡黄色;
④……
⑤一段时间后停止所有热源,装置冷却至室温后,拆卸装置,获得产品。
步骤②中要获得平稳的 气流,可采取的措施为
气流,可采取的措施为___________ ;步骤④为___________ 。
(3)F中发生反成的化学方程式为___________ 。
(4)为了检测产品为纯的无水 ,设计实验方案如下:
,设计实验方案如下:
①称取产品m g,溶于水,
②加足量硝酸酸化的 溶液,充分反应,
溶液,充分反应,
③……,
④称得固体为n g。
步骤③用到的仪器___________ (填标号),若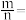
________ (保留小数点后两位),则产品纯净。

 与
与 制取无水
制取无水 (夹持装置和部分加热装置略),同时产生光气(
(夹持装置和部分加热装置略),同时产生光气( )。
)。
已知:
 是白色粉末;
是白色粉末; 是淡黄色粉末,易吸水,熔点为190℃;
是淡黄色粉末,易吸水,熔点为190℃; 沸点为76.8℃,易挥发;
沸点为76.8℃,易挥发; 是有毒气体,易水解,易与碱反应。
是有毒气体,易水解,易与碱反应。回答下列问题:
(1)装置A的作用是
(2)仪器药品准备完毕后进行的步骤为:①点燃A处酒精灯,一段时间后将A处酒精灯熄灭;
②……
③加热装置D至玻璃管中固体全部变为淡黄色;
④……
⑤一段时间后停止所有热源,装置冷却至室温后,拆卸装置,获得产品。
步骤②中要获得平稳的
 气流,可采取的措施为
气流,可采取的措施为(3)F中发生反成的化学方程式为
(4)为了检测产品为纯的无水
 ,设计实验方案如下:
,设计实验方案如下:①称取产品m g,溶于水,
②加足量硝酸酸化的
 溶液,充分反应,
溶液,充分反应,③……,
④称得固体为n g。
步骤③用到的仪器

您最近一年使用:0次



